|
ГАСТРОЭНТЕРОЛОГИЯ
ГЛАВА 12. ЯЗВЕННАЯ БОЛЕЗНЬ И HELICOBACTER PYLORI 1. Что такое Helicobacter pylori? Helicobacter pylori (прежнее название Campylobacterpylori) — это спиралевидная грам-отрицательная бактерия шириной 0,5 микрон и длиной от 2 до 6,5 микрон. Основные отличительные особенности H. pylori — многослойная оболочка, униполярный жгутик (с одной стороны) и выраженная уреазная активность. Форма микроорганизма и наличие жгутика позволяют ему проникать через барьер слизистой оболочки желудка. Высокая уреазная активность H. pylori в значительной степени способствует ее колонизации и выживаемости. Наличие уреазы представляет собой основу для проведения различных диагностических тестов с целью обнаружения H. pylori. Бактерии, вегетирующие в желудке, описаны у человека еще в начале XX столетия, но роль H. pylori в развитии язвенной болезни установлена лишь в 1980-х гг. Впервые H. pylori была высеяна в лаборатории в 1982 г. Маршаллом (Marshall) и Уорреном (Warren). 2. Вызывают ли язвенную болезнь другие микроорганизмы, похожие на Helicobacter pylori? На слизистой оболочке желудочно-кишечного тракта выделены четыре других микроорганизма спиралевидной формы — Я. cinadei, Я. fennelliae, Flexispira rappni и Gastrospirillum hominis. Считается, что G. hominis передается при контакте с кошками и собаками и является одной из причин развития хронического гастрита у людей. Вызывают ли остальные из этих микроорганизмов заболевания желудочно-кишечного тракта, в настоящее время остается неясным. 3. Где более всего распространен Helicobacter pylori? Географическое распределение H. pylori обусловлено степенью социального и экономического развития тех или иных областей. В развивающихся странах H. pylori может поражать 80—90 % людей, достигших 20-летнего возраста. В более старших возрастных группах сохраняется примерно такая же частота. В развитых странах показатель инфицирования H. pylori составляет приблизительно 20 % у 25-летних, однако увеличиваясь с возрастом в среднем на 1 % в год, достигает уровня 50-60 % у 70-летних жителей. Данные о частоте распространения H. pylori в развивающихся странах свидетельствуют о том, что она также непостоянна у разных возрастных групп. Первичное инфицирование происходит в детстве; у новорожденных вероятность развития инфекции становится все меньше. Внутри географических областей распространение H. pylori зависит от расовых и этнических факторов. Например, в США афро-американцы и испанцы инфицируются H. pylori в раннем детстве и значительно чаще, чем выходцы с Кавказа. 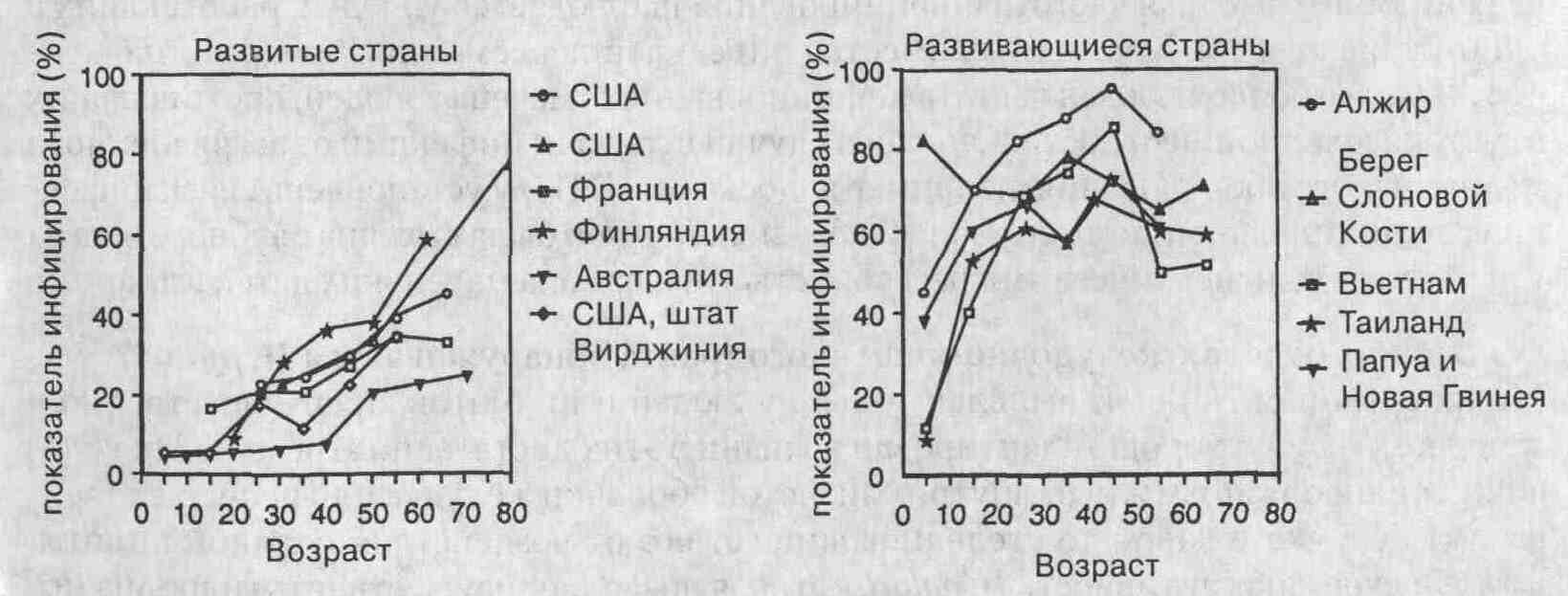
Распространение Н. pylori в развитых и развивающихся странах. (Из: Marshall et al. (eds). H. pylori in Peptic Ulceration and Gastritis. Boston, Blackwell, 1991, 46-58.)
4. Поражает ли Н. pylori детей? Как было указано выше, чаще всего инфицирование H. pylori людей происходит в детстве. Установлено, что у детей в возрасте от 8 до 16 лет Н. pylori вызывают некоторые клинические симптомы, например тошноту, рвоту, боли в животе, рвоту с кровью и дегтеобразный стул (мелену). При наличии поноса детей необходимо изолировать, как при инфекционном заболевании. Хотя у новорожденных обнаруживаются антитела против H. pylori, скорее всего это материнские антитела, которые проникли через плацентарный барьер. Первичное инфицирование детей до 2 лет происходит редко. Родители и сибсы (родные братья и сестры) инфицированных детей вероятнее всего тоже инфицированы. 5. Какие существуют факторы риска поражения Н. pylori? Основные факторы риска поражения H. pylori — низкий социально-экономический статус, большая скученность людей и плохие санитарные условия. Более высокий риск поражения H. pylori существует у гастроэнтерологов, по-видимому вследствие контакта с инфицированным желудочным соком и эндоскопическим оборудованием. Такой путь передачи возбудителя, однако, не очень характерен, потому что большая часть медицинского персонала, принимающая участие в проведении эндоскопических исследований, инфицируется не чаще, чем остальные жители региона. Отсутствуют данные о наличии какой-либо связи Н. pylori с полом, курением, приемом алкоголя или особеностями питания. 6. Каким способом происходит инфицирование Н. pylori? Истинный способ передачи инфекции в настоящее время неизвестен. Однако большинство данных говорят в пользу фекально-орального и орально-орального путей передачи. Более высокая частота инфицирования наблюдается у людей, работающих в одном учреждении. Кроме того, имеется определенная семейная предрасположенность. Также более высокая частота инфицирования отмечена у людей, проживающих в густонаселенной местности. Описаны случаи передачи инфекции от загрязненного медицинского оборудования, например эндоскопов. В Перу установлена связь инфекции с муниципальной системой водоснабжения. Н. pylori была высеяна с зубного налета у пациентов с диспептическими расстройствами и из кала маленьких детей с диареей. 7. В каких отделах желудочно-кишечного тракта обнаруживается Н. pylori? Микроорганизм H. pylori выявлен только у людей и приматов, преимущественно в желудке. H. pylori хорошо адаптирован к жизни в этих достаточно агрессивных условиях. Микроорганизм живет внутри слизистой оболочки желудка или непосредственно под ней, что в какой-то степени защищает его от воздействия соляной килоты. Высокая уреазная активность Н. pylori, которая позволяет осуществлять гидролиз мочевины до аммиака и гидрокарбонатов, повышает сопротивляемость микроорганизмов к низкому рН внутрижелудочной среды. H. pylori распознает и связывается со специальными рецепторами клеток желудочного эпителия, за счет чего плотно прилипает к поверхности эпителиальных клеток. Н. pylori выявлен также на эктопиро-ванном желудочном эпителии по всему желудочно-кишечному тракту, например в пищеводе (в пищеводе Барретта), двенадцатпипрерстной кишке (в участках желудочной метаплазии), тонкой кишке (в дивертикуле Меккеля [Meckel]) и прямой кишке (в эктопических очагах слизистой оболочки желудка). 8. Какой метод обнаружения Н. pylori в клинической практике считается самым лучшим? Во избежание траты лишних
денег имеющиеся диагностические тесты необходимо использовать таким образом,
чтобы получить ответы на конкретно поставленные вопросы. Если диагностическая
эндоскопия показана для установления клинического диагноза, то наиболее
предпочтительным методом для выявления H. pylori считается
биопсия тканей и исследование их уреазной активности. Стоимость исследования
уреазной активности тканей ненамного увеличит стоимость эндоскопического
исследования. Также можно выполнить и гистологическое исследование взятого
биопсий-ного материала, но фиксация и окраска тканей и собственно гистопатологическое
исследование увеличат стоимость диагностического процесса. Что касается
исследования уреазной активности тканей, то полностью этот анализ выполняется
за 24 ч, хотя результаты могут быть получены уже в течение 1 ч. Фиксация
и окраска препарата для гистологического иследования обычно занимает несколько
дней. Как было отмечено ранее, посев бактериальной культуры показан довольно
редко. Если клинический диагноз установлен ранее, во время фиброгастроэндоскопии
или рентгеноскопии желудка, методом выбора для выявления инфицирования
Н.
pylori является серологический тест. Данный метод неинвазивный, достаточно
простой в исполнении и относительно недорогой.
9. Можно ли обнаружить Н. pylori при помощи эндоскопии? Если да, то каким образом? Впервые Н. pylori был
высеян из участков слизистой оболочки желудка, полученных во время эндоскопического
иследования. Высевание данного микроорганизма представляет собой достаточно
трудоемкий процесс и требует наличия специальной обогащенной среды и продолжительной
инкубации (3-5 дней) в особых контролируемых микроаэрофильных условиях,
поэтому посев H. pylori нечасто используется в клинической
практике для диагностики. Как правило, его применяют в каких-либо особых
обстоятельствах, например для выявления чувствительности антибиотиков при
лечении устойчивых форм заболеваний.
Диагностические тесты для обнаружения Н. pylori
* Включая стоимость эндоскопического исследования. 10. Есть ли необходимость в выполнении эндоскопии для диагностики инфициро-вания Н. pylori ? Неэндоскопические методы обнаружения H. pylori включают серологический и дыхательный тесты. Антитела к IgG или IgA, связывающие различные бактериальные антигены, могут быть выявлены при помощи ферментозависимой иммуносвязываю-щей реакции (ELISA). Кроме того, в настоящее время в клинической практике имеются и несколько других серологических методик. Чувствительность и специфичность серологических методов, позволяющих обнаружить признаки первичного инфицирования H. pylori у нелеченных пациентов, составляют более 90 %. Хотя уровень антител после успешного лечения снижается, он тем не менее остается повышенным достаточно длительное время (до 3 лет). Этот своеобразный "серологический рубец" ограничивает возможности применения серологических исследований для оценки результатов лечения и диагностики повторного инфицирования. Дыхательный тест с мочевиной — еще один неинвазивный метод диагностики инфицирования H. pylori. Этот тест идеально подходит для оценки результатов лечения и диагностики повторного инфицирования, поскольку он бывает положителен только при наличии активной инфекции. Пациент принимает внутрь небольшое количество мочевины, меченной радиоактивным изотопом. Уреаза H. pylori расщепляет мочевину и высвобождает меченную двуокись углерода, которая выделяется с дыханием. Меченная радиоактивным изотопом двуокись углерода собирается вместе с выдыхаемым воздухом, после чего и определяется ее количество. Чувствительность и специфичность дыхательного теста составляют более 95 %. Сегодня дыхательные тесты с мочевиной почти не используются в клинической практике — пока еще не получено официальное разрешение на их широкое применение. 11. Каким образом Н. pylori повреждает слизистую оболочку желудочно-кишечного тракта? Существует несколько механизмов повреждающего действия H. pylori на слизистую оболочку. Непосредственное прилипание микроорганизмов к эпителиальным клеткам, аммиак, выделяемый в результате деятельности фермента уреазы, и бактериальные цитотоксины могут повреждать мембраны эпителиальных клеток. Другие бактериальные ферменты разрушают защитный слизистый барьер, в результате чего соляная кислота оказывает свое агрессивное действие на незащищенную слизистую оболочку. Последующее присоединение местной и системной воспалительной реакции приводит к более глубокому повреждению стенки желудка. 12. Вызывает ли инфекция Н. pylori какие-либо физиологические нарушения в организме? H. pylori вызывает повышение уровня сывороточного гастрина, который, в свою очередь, повышает продукцию соляной килоты. Хотя данный механизм действия H. pylori в настоящее время еще недостаточно изучен, имеются сообщения, свидетельствующие о том, что при этом возникает определенное ингибиторное действие соматоста-тина, вырабатываемого D-клетками антрального отдела желудка, на гастрин-продуцирующие G-клетки. После успешного лечения и эрадикации из организма бактерий H. pylori происходит постепенная нормализация физиологических функций желудка. 13. Какая существует связь между Н. pylori и гастритом? Известно, что инфекция Н. pylori приводит к развитию активного хронического гастрита. При гистологическом исследовании в эпителии и интерстициальном пространстве слизистой оболочки стенки желудка кроме лимфоцитов и плазматических клеток обнаруживаются нейтрофилы. У большинства пациентов эти изменения ограничены антральным отделом желудка. Однако в некоторых случаях заболевание может прогрессировать и поражать слизистую оболочку всего желудка. У пациентов только с антральным гастритом в последующем чаще развивается язва двенадцатиперстной кишки, тогда как у пациентов с пангастритом, особенно связанным с атрофией слизистой оболочки и кишечной метаплазией, существует повышенный риск возникновения язвы желудка и аденокарциномы. 14. Какая существует связь между HP-инфекцией и язвой двенадцатиперстной кишки? Между гастритом, вызванным H. pylori, и язвой двенадцатиперстной кишки имеется самая тесная связь. Почти 95 % пациентов с язвой двенадцатиперстной кишки инфицированы H. pylori. 15. Каковы механизмы развития язвы двенадцатиперстной кишки при инфициро-вании желудка Н. pylori? Как было отмечено выше, инфекция H. pylori может вызвать избыточную продукцию соляной кислоты в желудке. Соляная кислота вместе с другими пока не известными факторами, в течение длительного времени воздействуя на слизистую оболочку двенадцатиперстной кишки, приводит к ее повреждению, влекущему за собой возникновение в двенадцатиперстной кишке очагов желудочной метаплазии. Метаплазиро-ванный желудочный эпителий, пораженный H. pylori, способствует развитию дуоденита и затем язвы двенадцатиперстной кишки. Таким образом, профилактика развития язвы двенадцатиперстной кишки состоит либо в устранении избыточной продукции соляной килоты (традиционными способами), либо в эрадикации H. pylori. 16. Играет ли роль H. pylori в развитии язвы желудка? В большинстве случаев (60-90 %) язва желудка развивается на фоне гастрита, вызванного H. pylori. Как отмечалось ранее, H. pylori посредством различных механизмов делает слизистую оболочку желудка более чувствительной к агрессивному воздействию соляной кислоты. 17. Имеются ли другие причины развития язвенной болезни, кроме инфицирова-ния Я. pylori? Язвы двенадцатиперстной кишки, развивающиеся без H. pylori, встречаются достаточно редко. Как правило, это язвы, индуцированные приемом нестероидных противовоспалительных препаратов, возникшие на фоне гиперсекреторного состояния при синдроме Золлингера-Эллисона или проявляющиеся необычными симптомами некоторых заболеваний желудочно-кишечного тракта, например болезни Крона. Истинные идиопатические язвы двенадцатиперстной кишки обусловлены генетическими факторами и характеризуются повышенной секрецией соляной кислоты и быстрым опорожнением желудка. Они трудно поддаются традиционному лечению и часто сопровождаются осложнениями. Хотя большая часть язв желудка, развившихся без инфицирования H. pylori, связаны с приемом нестероидных противовоспалительных препаратов, у всех пациентов с язвой желудка необходимо исключить аденокарциному и лимфому желудка. 18. Могут ли у пациентов, инфицированных H. pylori, развиваться какие-либо клинические симптомы при отсутствии язвенной болезни? Неязвенная диспепсия представляет собой патологическое состояние, вызываемое множественными причинами, которое трудно выявить клиническими методами. Сведения, что гастрит, вызванный H. pylori, может приводить к развитию диспепсии при отсутствии язвы, требуют доказательств, поскольку не существует каких-либо специфических симптомов, отличающих диспепсию, связанную с поражением H. pylori, от других форм неязвенной диспепсии. Кроме того, эффект лечения инфекции H. pylori при наличии симптомов неязвенной диспепсии достаточно высок. Тем не менее у отдельных пациентов с неязвенной диспепсией имеются симптомы, связанные с инфекцией H. pylori, которые поддаются специфическому лечению. К сожалению, в настоящее время нельзя с большой степенью надежности выделить таких пациентов в отдельную группу. 19. Почему клинические симптомы заболевания развиваются лишь у небольшого числа лиц, инфицированных H. pylori? У всех инфицированных пациентов наблюдаются гистологические признаки активного хронического гастрита, однако клинически выраженные симптомы заболевания развиваются только у некоторых из них. Являются ли причиной тому какие-либо факторы макроорганизма (например, состояние иммунной системы), либо генетическая предрасположенность, либо наличие особых штаммов бактерий H. pylori с повышенной вирулентностью в настоящее время остается неясным. 20. Что происходит с хронической язвой после эрадикации H. pylori? Ежегодная частота рецидивов хронической язвы двенадцатиперстной кишки составляет приблизительно 75 %. Эта цифра может быть снижена до 25 % при проведении постоянной поддерживающей противоязвенной терапии. После полной эрадикации H. pylori, ежегодный рецидив хронической язвы двенадцатиперстной кишки уменьшается до 5 %. Язвы желудка, не связанные с приемом нестероидных противовоспалительных средств, после эрадикации H. pylori также рецидивируют достаточно редко. 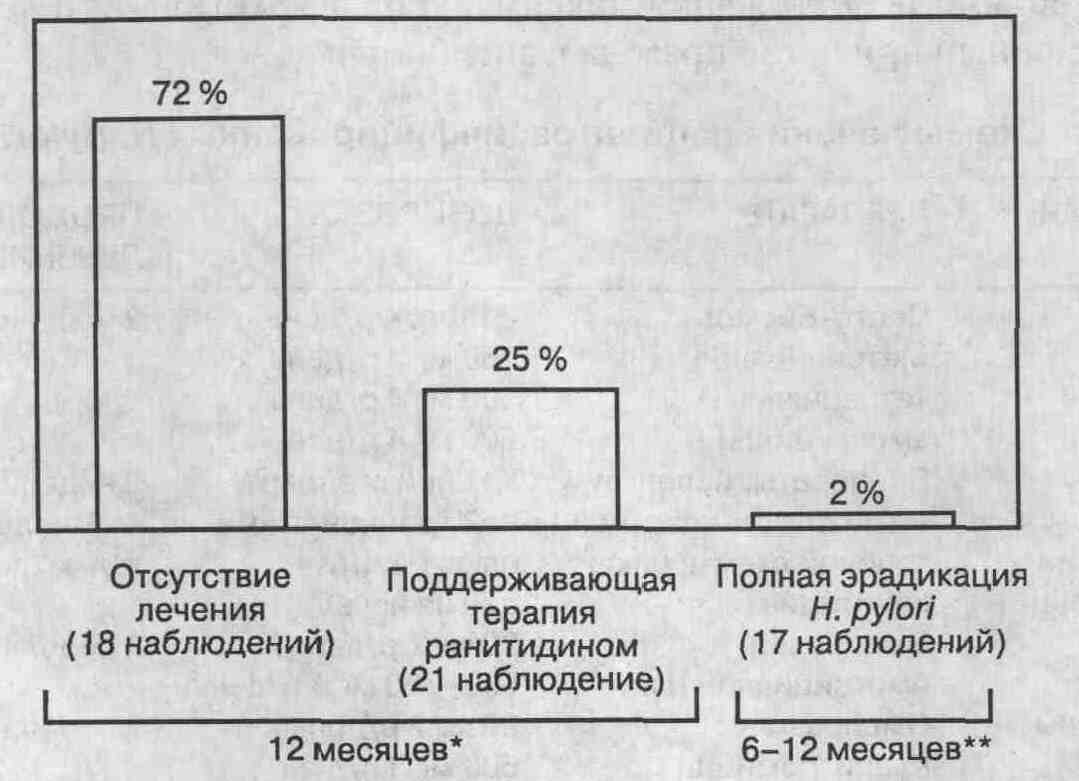
Частота рецидивов язвы двенадцатиперстной
кишки при различных тактиках лечения
21. В каких случаях необходимо проводить антибактериальное лечение, направленное на подавление H. pylori? В феврале 1994 г. на Итоговой Конференции Национального Института Здоровья рекомендовано проводить лечение пациентов с язвенной болезнью, инфицированных Н.pylori, антибактериальными и противоязвенными препаратами с самого начала заболевания или при возникновении рецидива. Кроме того, у пациентов с язвенной болезнью, инфицированных H. pylori, которым проводится поддерживающая терапия только антисекреторными препаратами, необходимо эту терапию прервать и осуществлять полноценное антибактериальное лечение. Антибактериальное лечение показано также пациентам, инфицированным Н. pylori, которые принимают нестероидные противовоспалительные препараты. Имеющихся в настоящее время данных недостаточно для того, чтобы для предотвращения развития язвенной болезни или новообразований желудка рекомендовать антибактериальное лечение всем пациентам с неязвенной диспепсией или пациентам, инфицированным Н.pylori, при отсутствии у них клинических симптомов заболевания. 22. Какие схемы антибактериальной терапии используются при лечении пациентов, инфицированных H. pylori? Двухнедельный курс так называемой тройной схемы лечения, в которую входят препараты висмута, метронидазол и либо тетрациклин, либо амоксициллин, позволяют излечить инфекцию у 75-90 % пациентов. Тройная терапия менее эффективна у пациентов с метронидазолрезистентными микроорганизмами. Кроме того, она достаточно сложна, связана с неудобным режимом приема лекарств и характеризуется наличием побочного действия препаратов. Альтернативная схема лечения представляет собой двухнедельный курс приема ингибиторов протонной помпы, например омепразола, и либо амоксициллина, либо кла-ритромицина. Двойная терапия сопровождается меньшим числом побочных эффектов, чем тройная, но и эффективность ее также ниже. Показатель эрадикации HP составляет 70-80 /6. Для достижения максимальной эффективности лечения необходим одновременный прием омепразола и антибиотика. Схемы лечения пациентов, инфицированных Н. pylori
В настоящее время появилась
тенденция к использованию непродолжительных курсов лечения, направленных
на эрадикацию Н. pylori. Некоторые из них представлены в таблице.
Примечание. Составлено по данным:
23. Какова роль антибактериальной терапии, направленной на подавление Н. pylori, в лечении осложненных форм язвенной болезни? Осложнения язвенной болезни (например, кровотечение из хронической язвы) связаны с длительными сроками лечения пациентов и сопровождаются высокой летальностью. Имеющиеся данные говорят о том, что, назначаемая после достижения заживления осложненной хронической язвы, поддерживающая антисекреторная терапия снижает вероятность рецидива осложнений. Предварительные результаты исследований показывают, что лечение, направленное на подавление H. pylori, также может быть эффективным методом профилактики развития осложнений язвенной болезни. Однако до тех пор пока эти данные не получат подтверждения, необходимо проводить поддерживающую антисекреторную терапию у пациентов с осложненными формами язвенной болезни даже после эрадикации Н. pylori. 24. Часто ли возникает реинфицирование Н. pylori? Показатель частоты повторного инфицирования после полной эрадикации H. pylori зависит от географических и социальных факторов. В развивающихся странах он может достигать 15 %. Однако в развитых странах, например в США, частота реин-фекции после полного уничтожения H. pylori достаточно низкая — 0,5-3 %. 25. Какова экономическая выгода от излечения пациентов от НР-инфекции? До настоящего времени не проводилось каких-либо специальных исследований, где бы подвергалась рассмотрению стоимость лечения язвенной болезни с применением антибактериальной терапии и без таковой. Однако обработка данных о прямой и косвенной стоимости различных видов лечения показала, что антибиотикотерапия является наименее дорогим методом. Такой вывод основан на анализе различных сторон этой проблемы, в т. ч. частоте полной эрадикации Н.pylori, показателе повторного инфицирования и общей стоимости лечения. 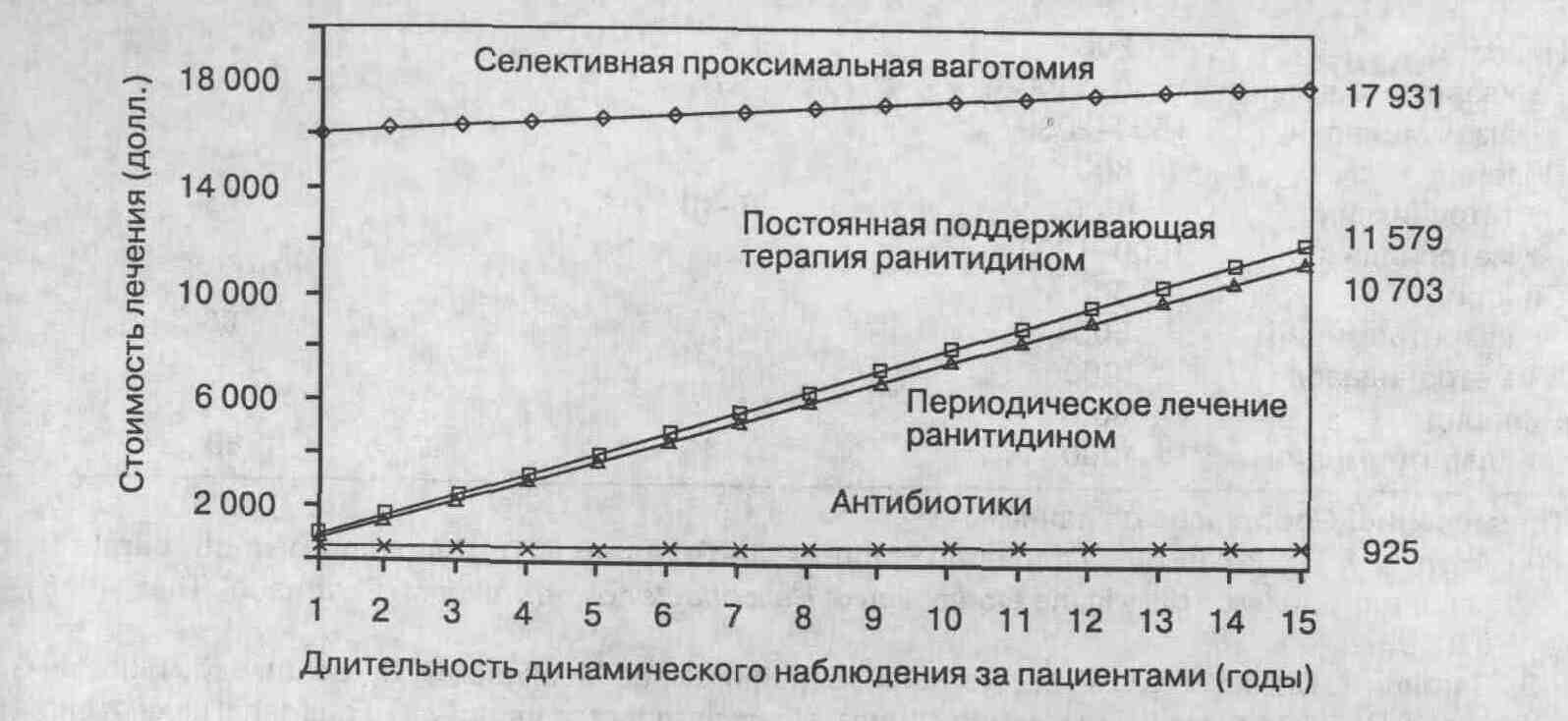
Предположительная стоимость лечения хронической язвы двенадцатиперстной кишки (по данным Итоговой конференции Национального института здоровья, 1993.) |