ГАСТРОЭНТЕРОЛОГИЯ
1. Одинаковы ли все раковые опухоли пищевода? Нет. Рак пищевода подразделяется на плоскоклеточный рак и аденокарциному. В норме пищевод на всем протяжении выстлан неороговевающим многослойным плоским эпителием. Раньше надолго плоскоклеточного рака приходилось 95 % всех злокачественных опухолей пищевода, однако в последние 10-15 лет заболеваемость аденокарциномой пищевода значительно возросла. В настоящее время аденокарцинома составляет более одной трети всех случаев злокачественных новообразований пищевода. Наиболее часто рак развивается в местах кишечной дисплазии (где имеются участки гетеротопического однослойного цилиндрического эпителия, эпителия Барретта). Возможно также развитие рака из цилиндрического эпителия слизистых желез пищевода. Рак пищевода — одно из заболеваний, наиболее часто приводящих к летальному исходу. Отдаленный прогноз крайне неблагоприятный. Пятилетняя выживаемость составляет всего лишь 3-6 % и не зависит от гистологического типа опухоли и степени ее дифференцировки. Плохой прогноз обусловлен несколькими причинами: (1) клинические симптомы, как правило, возникают на поздних стадиях развития опухоли; (2) даже маленькие опухоли пищевода быстро метастазируют по лимфатическим сосудам, густо пронизывающим подслизистый слой стенки пищевода; (3) поскольку пищевод, в отличие от других трубчатых органов пищеварительного тракта, не имеет серозной оболочки, нередко наблюдается прямое прорастание опухоли в органы средостения и окружающие ткани. 2. Как часто встречается рак пищевода? Рак пищевода — одно из наиболее распространенных злокачественных новообразований во всем мире, за исключением Северной Америки и Западной Европы. В США ежегодно выявляется более 10 000 новых пациентов, у которых обнаруживается рак пищевода. Рак пищевода является причиной смерти 4 % всех больных с онкологическими заболеваниями. Его распространенность широко варьирует в зависимости от половой и расовой принадлежности, а также от географического положения. В США соотношение заболеваемости раком пищевода у мужчин и женщин составляет 3:1. У представителей негроидной расы риск развития плоскоклеточного рака пищевода в 4 раза выше, чем у представителей европеоидной расы. Однако у представителей европеоидной расы чаще встречается аденокарцинома. Во Франции соотношение заболеваемости раком пищевода у мужчин и женщин составляет 20 : 1, в то время как в других странах —1:1. Распространенность рака пищевода колеблется от 5 до 7 новых случаев на 100 000 человек среди популяций высокого риска (жители Ирана, Китая и Шри-Ланки). В Шри-Ланке рак пищевода является самым частым злокачественным заболеванием пищеварительного тракта, в то время как в Северной Америке наиболее распространен рак ободочной кишки. В Азии (Иран, Афганистан, Монголия и северо-запад Китая) отмечается крайне высокая заболеваемость раком пищевода. 3. Назовите факторы, способствующие развитию рака пищевода. Злоупотребление алкоголем и курение — наиболее известные факторы риска. Каждый из этих факторов по отдельности увеличивает риск развития рака пищевода, но их сочетание дает синергический эффект, создавая добавочный риск. Известна также роль пищевых факторов, таких как недостаточность витамина А и рибофлавина. Цинк и молибден — микроэлементы, являющиеся кофакторами нитратредуктазы,— способны оказывать защитное действие на слизистую оболочку пищевода. Роль других антиоксидантов, в том числе витаминов С и Е, недостаточно изучена. Пищевые канцерогены, например нитрозамины и афлатоксины, также могут способствовать развитию рака пищевода. В провинции Линзань (Китай), где заболеваемость раком пищевода очень высока, существует обычай готовить маринованные овощи с большим количеством специй. Установлено, что частое употребление в пищу курицы с маринованными овощами также увеличивает риск возникновения рака пищевода. Вероятность развития рака пищевода увеличивается и при некоторых других патологических состояниях, к которым относятся химические ожоги или стриктуры пищевода; тилоз (редкое, аутосомно-доминантное заболевание, характеризующееся гиперкератозом ладоней и стоп); синдром Пламмера-Винсона (Plummer-Vinson), включающий триаду симптомов, а именно: железодефицитную анемию, ахлоргидрию и стриктуру верхнего отдела пищевода; длительно существующая нелеченная ахалазия; предшествующее облучение средостения; целиакия и хронический нерефлюксный эзо-фагит (в Азии). 4. Каковы клинические проявления рака пищевода? Дисфагия — самый частый симптом рака пищевода. Дисфагия обычно возникает и прогрессирует постепенно, сначала при употреблении твердой пищи, а затем — и при приеме жидкостей. На ранних стадиях заболевания приступы дисфагии преимущественно наблюдается при употреблении мяса, хлеба и яблок. Многие пациенты изменяют свои вкусовые привычки и по мере прогрессирования заболевания переходят ко все более "мягким" продуктам и жидкостям. Нередко отмечается значительное снижение массы тела. Наличие одинофагии (боли при глотании) обусловлено, по-видимому, суперинфекцией или лекарственным эзофагитом. Наблюдаемая в некоторых случаях постоянная боль за грудиной, в эпигастральной области и спине — признак прорастания опухоли в органы средостения. Икота свидетельствует о вовлечении в патологический процесс диафрагмы. Гиперсаливация может возникать в результате прогрессирующего стеноза пищевода. Охриплость голоса — более редкий симптом, имеющий место при поражении возвратного гортанного нерва. Симптомы поражения нервной системы и мышц являются следствием гиперкальциемии (как проявления паранеопластических реакций) или метастазов в кости. Поражение легких в большинстве случаев наблюдается на поздних стадиях заболевания и характеризуется рецидивирующими легочными инфекциями, развивающимися вследствие аспирации или образования пищеводно-бронхиального свища. Рвота кровью возникает в результате распада опухоли (рвота кофейной гущей) или эрозии сосудов пищевода (наличие неизмененной крови в рвотных массах). 5. Какие лабораторные исследования могут помочь в диагностике рака пищевода? Абсолютно специфичных лабораторных тестов для диагностики рака пищевода не существует. Анемия может быть нормохромной и нормоцитарной (вследствие хронического заболевания), микроцитарной (вследствие дефицита железа) или макроцитарной (отражая лежащее в основе заболевания злоупотребление алкоголем). Гипоальбуминемия встречается при недостаточности питания. Уровень печеночных ферментов повышается при метастатическом поражении печени или у пациентов, злоупотребляющих алкоголем. Онкомаркеров, специфичных для рака пищевода, не существует. 6. Могут ли другие заболевания имитировать клинические проявления рака пищевода? Этот вопрос можно перефразировать так: с какими заболеваниями следует проводить дифференциальную диагностику у пациентов с дисфагией? Дисфагия никогда не бывает проявлением психосоматических нарушений. При возникновении дисфагии у пациента старше 40 лет к нему следует относиться как к больному с опухолью пищевода, до тех пор пока не будет доказано обратное. Наиболее частая причина дисфагии, имитирующей клинические проявления рака пищевода,— пептическая стриктура пищевода. Обычно дисфагия прогрессирует медленно и связана с частыми приступами изжоги в анамнезе. Пищеводные кольца и мембраны обычно вызывают перемежающуюся дисфагию в течение длительного периода времени. Эзофагит также может являться причиной дисфагии, которая возникает только при приеме твердой пищи; для эзофагита характерно наличие в анамнезе частых приступов изжоги и регургитации. Ахалазия и другие нарушения двигательной активности пищевода — еще одна причина дисфагии, однако в этом случае она не прогрессирует и не сопровождается снижением массы тела. Внимательное изучение анамнеза, как правило, позволяет дифференцировать эти состояния от рака пищевода. 7. Каким образом ставится диагноз рака пищевода? Метод двойного контрастирования пищевода с бариевой взвесью позволяет выявить рак пищевода у большинства пациентов. Изменения, характерные для злокачественного поражения пищевода, включают наличие узловых утолщений в стенке пищевода и неравномерных или асимметричных сужений просвета, изъязвления, резкие перегибы пищевода, а также выявление ригидных или неперистальтирующих участков при рентгеноскопии или просмотре видеозаписи (см. рис. А на следующей странице). Пептические стриктуры пищевода в большей части случаев характеризуются симметричными, ровными и конусообразнобразными сужениями. Проксимальнее места локализиции опухоли пищевод может быть расширен, однако дилатация при этом выражена в меньшей степени, чем при пептических стриктурах или ахалазии пищевода. Эндоскопия является более чувствительным методом, чем рентгено-контрастная эзофагография и позволяет выполнить биопсию для последующего гистологического исследования (см. рис. В). Необходимо определить распространенность поражения стенки пищевода; при заборе биопсийного материала по меньшей мере из 7 участков слизистой оболочки точность диагностики достигает 98 %. Незначительные изменения слизистой оболочки пищевода, выявляемые при проведении эндоскопического исследования, могут свидетельствовать о наличии поверхностной карциномы или ранней стадии опухоли. Этот метод позволяет также производить забор материала для цитологического исследования (щеточная биопсия), что существенно увеличивает диагностические возможности. 8. Каковы стадии развития рака пищевода? Принятая в настоящее время классификация по системе TNM (tumor — regional nodes — metastasis = опухоль — метастазы в регионарные лимфоузлы — отдаленные метастазы), разработанная Американским Объединенным Комитетом по Раку в 1987 г., представляет собой классификацию, в основе которой лежит стадийность опухолевого процесса. Согласно этой классификации, Tis — это карцинома in situ, которая не распространяется через базальную мембрану; Т1 — вовлечение в процесс собственной пластинки слизистой оболочки или подслизистого слоя; Т2 — поражение собственной мышечной оболочки; ТЗ — поражение адвентиций и Т4 — распространение процесса на окружающие органы и ткани. М и N оцениваются как 1 (положительно), О (отрицательно) или X (нет данных). 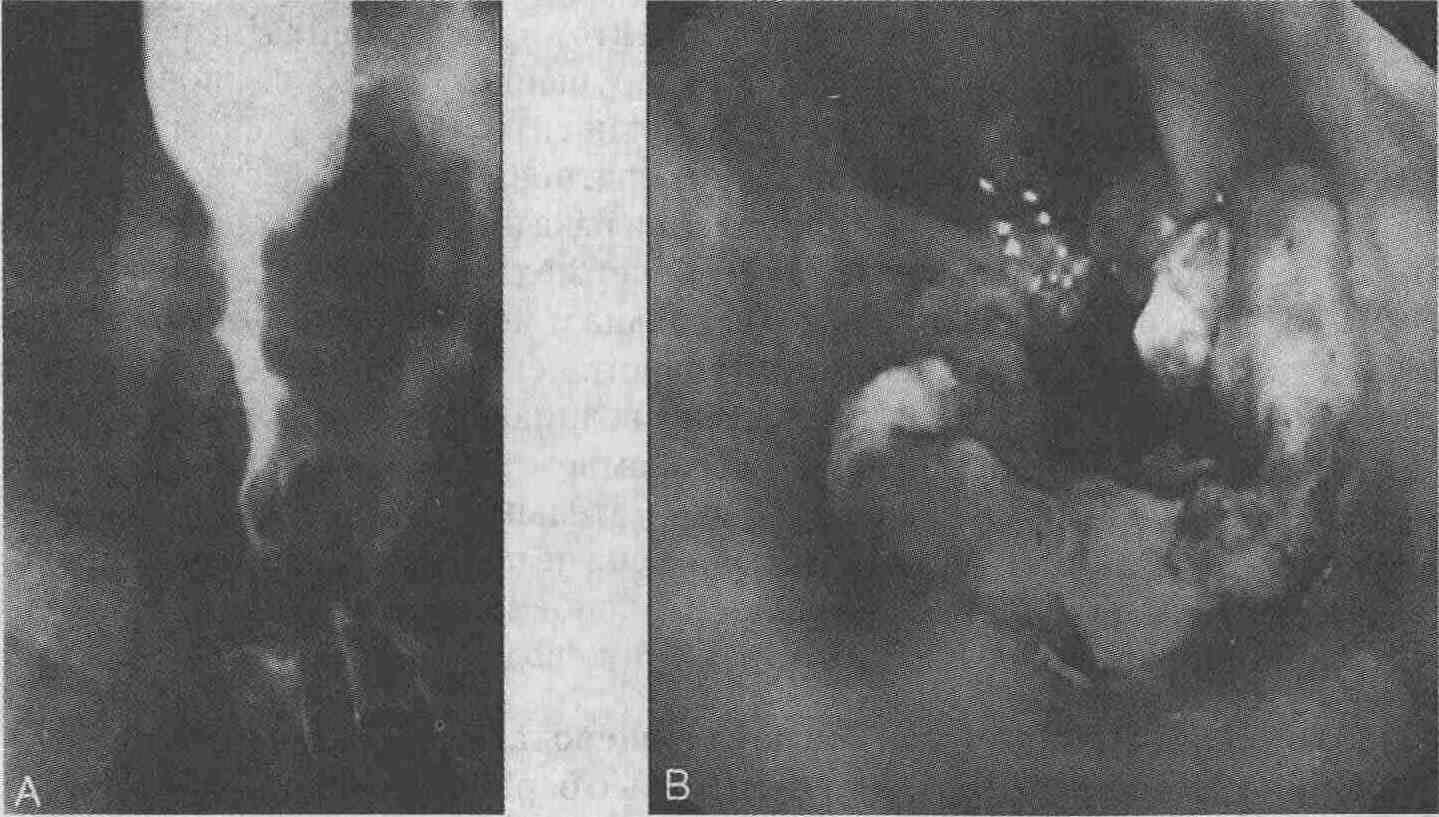 9. Какова тактика лечения после установления диагноза рака пищевода? После установления диагноза рака пищевода (по результатам морфологического исследования) необходимо определить, показано ли больному хирургическое вмешательство. Если состояние пациента позволяет выполнить ему эзофагэктомию, уточняют распространенность злокачественного поражения. Хотя четкой схемы обследования в данном случае не существует, пациенту, по меньшей мере, следует назначить рентгенографию грудной клетки и компьютерную томографию органов брюшной полости. Эти исследования показывают степень вовлечения в патологический процесс легких и органов средостения, а также увеличение абдоминальных лимфатических узлов и наличие метастазов в печени. Эндоскопическое ультразвуковое исследование (ЭУЗИ) — наиболее чувствительный и точный метод, позволяющий определить стадию первичной опухоли пищевода. Данное исследование технически трудно выполнимо и доступно далеко не всем, однако для более полного предоперационного обследования пациента его следует, по возможности, применять в сочетании с такими методами, как компьютерная томография. Другими методами, информативными в отдельных случаях, являются: бронхоскопия (для исключения поражения дыхательных путей), медиастиноскопия и лапароскопия (для исключения карциноматозного поражения печени и брюшины). Если у пациента нет противопоказаний к оперативному вмешательству, особое внимание следует уделить его питанию. Выраженные нарушения питания требуют коррекции (при необходимости кормление больного проводится через назогастральный зонд или парентеральным путем). Необходима оценка и коррекция нарушений дыхания, поскольку многие пациенты с опухолью пищевода — курильщики. По той же причине необходимо тщательное обследование ЛОР-органов; у 10-15 % пациентов, страдающих раком пищевода, параллельно выявляются злокачественные опухоли головы, шеи или бронхиального дерева. 10. Какие факторы позволяют прогнозировать выживаемость пациентов с опухолью пищевода? К основным признакам, позволяющим прогнозировать выживаемость, относятся размер первичной опухоли на момент установления диагноза и вовлечение в опухолевый процесс других органов и систем. Совершенно очевидно, что опухоль, сопровождающаяся клиническими симптомами, характеризуется неблагоприятным прогнозом. Пятилетняя выживаемость среди таких пациентов составляет не более 2-8 %. При появлении клинических симптомов заболевания у 30-40 % пациентов имеет место далеко зашедший местный процесс или выявляются отдаленные метастазы опухоли; оперативное лечение неэффективно. Как правило, после определения стадии заболевания операбельными считаются 50-60 % пациентов, однако лишь у 10 % из них возможно выполнить резекцию пищевода. Опухоль более 5 см в диаметре обычно дает метастазы в регионарные лимфоузлы. У пациентов с опухолью менее 5 см в диаметре без поражения лимфатических узлов прогноз более благоприятный. Глубина поражения стенки пищевода определяет, является ли процесс местным или распространенным, а поэтому считается основным фактором, влияющим на выживаемость пациентов. Если опухоль распространяется не далее подслизистого слоя, пятилетняя выживаемость составляет более 60 %. Если в опухолевый процесс вовлечена собственная мышечная оболочка стенки пищевода, пятилетняя выживаемость снижается до 30 %, а при поражении адвентициальной оболочки — до 10 %. При наличии ранних стадий опухоли или поверхностного инвазивного рака (ограниченного слизистой оболочкой и подслизистым слоем) хирургическое вмешательство весьма эффективно; пятилетняя выживаемость у таких пациентов высокая — 85 % (по данным китайских исследователей). В США пациенты с плоскоклеточным раком пищевода, выявленным на ранней стадии, составляют очень небольшой процент. Прорастание опухолью сосудов делает прогноз неблагоприятным и, несмотря на небольшой размер или поверхностное расположение первичной опухоли, обычно связано с метастазированием в регионарные лимфатические узлы. Стенка пищевода не имеет серозной оболочки, поэтому рак пищевода относительно легко прорастает в близлежащие органы, например в трахею, бронхи, легкие, плевру, сосуды и диафрагму. Чаще всего плоскоклеточный рак поражает среднюю треть пищевода, реже — нижнюю треть; в очень редких случаях — верхнюю треть пищевода. Гистологическое строение опухоли (например, аденокарцинома или плоскоклеточный рак) и степень дифференцировки ее не имеют прогностического значения. Существует предположение о наличии прямой связи между степенью анэуплоидии ДНК и прогнозом заболевания (по крайней мере, у жителей Азии). 11. Какова тактика лечения пациентов с опухолью пищевода? Хирургические методы лечения
рака пищевода имеют наилучшие результаты, однако их применение должно быть
обоснованным. Наиболее часто выполняется эзофагэктомия с наложением желудочно-глоточного
анастомоза и перемещением желудка в грудную полость. Иногда, по техническим
причинам, возникает необходимость в замещении резецированной части пищевода
отрезком толстой или тонкой кишки. В случае выполнения операции опытным
специалистом послеоперационная смертность составляет 3-30 %, но может быть
и выше в клиниках общего профиля. Данное вмешательство чревато многими
осложнениями.
12. Какова роль химиотерапии в лечении рака пищевода? Применение в предоперационном периоде химиотерапии (цисплатина) в сочетании с лучевой терапией для уменьшения массы опухоли в значительной мере увеличивает эффективность хирургического вмешательства. У таких пациентов выживаемость после эзофагэктомии гораздо выше. При невозможности выполнения эзофагэктомии необходимо проводить комбинированную терапию (цисплатином в сочетании с лучевой терапией), результаты которой лучше, нежели таковые при лучевой терапии. Пятилетняя выживаемость после курса комбинированной терапии у пациентов с плоскоклеточным раком составляет 18 %, с аденокарциномой пищевода — не более 3 лет. 13. Какие эндоскопические методы лечения применяются у пациентов с опухолью пищевода в качестве паллиативных вмешательств? Выраженная дисфагия значительно снижает качество жизни. Бужирование пищевода под эндоскопическим или рентгенологическим контролем может использоваться как паллиативное вмешательство, однако положительный эффект при этом сохраняется кратковременно. Другие методы, используемые для лечения больных с опухолью, растущей в просвет пищевода, такие как биполярная каутеризация опухоли и эндоскопическая лазеротерапия, характеризуются более длительным эффектом, но сопровождаются более высоким риском; к тому же их стоимость гораздо выше. Фотодинамическая терапия заключается во внутривенном введении фотосенсибилизи-рующих препаратов (например, гематопорфирина), селективно накапливающихся в опухолевой ткани. После введения препарата опухоль из просвета пищевода облучают низкоэнергетическим лазером с определенной длиной волны, который избирательно убивает опухолевые клетки. К ограничениям данного метода относят фоточувствительность кожных покровов, а также его малую доступность в настоящее время. Установка в пищевод пластикового или металлического стента является методом выбора при пищеводно-бронхиальном свище. Дисфагию также лечат с помощью стентов, однако данный метод содержит много спорных моментов и характеризуется высокой степенью риска. При этом нередко возникают тяжелые осложнения (например, пищеводно-аортальный свищ), особенно у пациентов, которым предварительно был проведен курс лучевой терапии. Чрескожную эндоскопическую гастростомию выполняют для осуществления питания пациентов с выраженной дисфагией, не поддающихся лечению другими методами. |