Опубликовано в журнале:
, Неонаталогия. Март, 2008ДИАГНОСТИКА ВРОЖДЕННЫХ БРОНХОЛЕГОЧНЫХ ЗАБОЛЕВАНИЙ У ДЕТЕЙ, ПЕРЕНЕСШИХ ИВЛ В НЕОНАТАЛЬНОМ ПЕРИОДЕ
Г.В. Яцык, И.В. Давыдова, Е.Н. Цыгина, О.В. Кустова, М.А. Басаргина, ГУ Научный центр здоровья детей РАМН
По данным разных авторов, у больных с хроническими заболеваниями легких частота пороков развития колеблется от 1,4-10% до 20-50%, что объясняется нечеткостью не только клинико-рентгенологических, но и патоморфологических критериев диагностики некоторых пороков развития, особенно осложненных хроническим воспалением и фиброзными изменениями.
Необходимо уточнить, что врожденные дефекты бронхолегочных структур, обычно не проявляющиеся клинически и не влияющие на функциональные показатели, считаются аномалиями развития (например, аномалия ветвления бронхов), тогда как врожденные пороки развития сопровождаются функциональными нарушениями и/или проявлениями болезни [3].
Наиболее распространенными врожденными пороками развития органов дыхания являются:
аномалии ветвления бронхов; агенезия, аплазия, гипоплазия легкого или его долей; распространенные пороки развития стенки трахеи и бронхов (трахеобронхомаляция, синдром Вильямса-Кемпбелла, бронхиолэктатическая эмфизема Лешке); ограниченные пороки развития стенки трахеи и бронхов (стеноз трахеи, врожденная лобарная эмфизема, трахео-пищеводные и бронхо-пищеводные свищи); кисты и секвестрация легких; пороки развития легочных сосудов [4]. Особо следует отметить такие наследственные заболевания, как муковисцидоз и синдром Картагенера, при которых респираторная патология в виде хронического бронхита является составной частью симптомокомплекса, имеющего в своей основе в первом случае генетически обусловленный дефект транспортного белка хлоридного канала в эпителиальных клетках эндокринных желез, а во втором - нарушение мукоцилиарного клиренса за счет дефекта ресничек мерцательного эпителия. В типичных случаях диагностика этих патологических состояний не вызывает затруднений, а в случае с муковисцидозом потовый тест (определение уровня хлоридов пота) в настоящее время включен в скрининговую систему новорожденных.
Диагностика же врожденных пороков развития стенки трахео-бронхиального дерева у новорожденных, особенно недоношенных детей, зачастую вызывает определенные трудности в связи с тяжестью состояния пациентов и схожестью с другими патологическими состояниями симтоматики в виде бронхообструктивного синдрома, сопровождающегося дыхательной недостаточностью. Катамнестическое наблюдение в течение первого года жизни, а при необходимости и в дальнейшем, позволяет уточнить характер бронхолегочной патологии, что приводит к увеличению вдвое количества верифицированных диагнозов "врожденный порок развития бронхолегочной системы" [1, 11, 13, 21]. В пользу врожденного генеза бронхолегочного поражения свидетельствуют аномалии и пороки других органов, а также явные аномалии в том же или другом легком [3, 4].
КЛИНИЧЕСКОЕ ИССЛЕДОВАНИЕ
Под нашим наблюдением находилось 122 недоношенных ребенка, которым с рождения проводилась искусственная вентиляция легких (ИВЛ) по поводу респираторного дистресс-синдрома и/или внутриутробной пневмонии. Длительность ИВЛ составляла от 2 до 82 дней. В группу вошло 80 мальчиков и 42 девочки с гестационным возрастом 25-36 недель и массой тела при рождении от 695 до 2700 г. Срок катамнестического наблюдения составлял от 6 месяцев до 7 лет. 102 ребенка из наблюдаемой группы сформировали бронхолегочную дисплазию (БЛД) к 36 неделям постконцептуального возраста, верифицированную согласно клинико-рентгенологическим критериям диагностики [5, 6, 15, 16, 17]:
ИВЛ в течение 3 и более суток на первой неделе жизни и/или проведение респираторной терапии с постоянным положительным давлением в дыхательных путях через носовые катетеры (nCPAP); терапия кислородом (более 21%) в возрасте 28 дней и старше; симптомы дыхательной недостаточности, бронхиальной обструкции в возрасте 28 дней и старше; вздутие легких, повышение прозрачности/буллы, фиброз или интерстициальный отек на рентгенограмме органов грудной клетки. По степени тяжести БЛД дети наблюдаемой группы распределялись следующим образом: легкое течение - 16 детей (15%); средне-тяжелое течение - 41 ребенок (40%); тяжелое течение - 45 детей (45%). Высокий процент формирования тяжелых вариантов течения БЛД связан с особым контингентом больных, поступающих на 2-й этап выхаживания в отделение новорожденных и недоношенных детей ГУ НЦЗД РАМН. Среди наблюдаемых больных преобладали глубоконедоношенные дети с гестационным возрастом 25-30 недель (52%) с низкой и экстремально низкой массой тела при рождении (до 1500 г - 70 %), получавшие прологированную ИВЛ на фоне выраженной морфо-функциональной незрелости и тяжелых дыхательных расстройств в периоде новорожденности, что согласуется с литературными данными [2, 19, 20].
Следует отметить, что еще Нортвей, в 1967 году давший клинико-рентгенологическую и морфологическую характеристику заболевания и впервые предложивший термин "бронхолегочная дисплазия", отмечал, что в патологический процесс вовлечены все составляющие легочной ткани, что сближает это приобретенное заболевание с пороками развития. Однако по механизму и срокам формирования данные процессы не могут быть отождествлены. Определение БЛД со временем претерпело значительное изменения [8, 9, 10].
Под бронхолегочной дисплазией на современном этапе понимают хроническое заболевание легких детей первых двух лет жизни, возникающее в перинатальном периоде главным образом у глубоконедоношенных детей, получающих респираторную терапию в неонатальном периоде. БЛЛ протекает с преимущественным поражением бронхиол и паренхимы легких, развитием эмфиземы, фиброза и/или нарушением репликации альвеол; проявляется кислородозависимостью в возрасте 28 суток жизни и старше, дыхательной недостаточностью, бронхообструктивным синдромом, рентгенографическими изменениями; и характеризуется регрессом клинических проявлений по мере роста ребенка [6, 23]. Речь может идти лишь о сочетании двух патологических состояний, когда БЛД формируется после пролонгированной ИВЛ у ребенка с врожденным пороком развития бронхолегочной системы. Подобная точка зрения на патогенез БЛД как последствие продленной ИВЛ в раннем неонатальном периоде по поводу различных острых патологических состояний у недоношенных детей доминирует в отечественной и зарубежной литературе [7, 11, 12, 18]. Причем, являясь поначалу осложнением реанимационных мероприятий, БЛД в дальнейшем может стать основным заболеванием, особенно у детей с наследственной предрасположенностью к гиперреактивности соединительной ткани дыхательных путей [2, 14, 22, 24].
При катамнестическом наблюдении детей с БЛД от 6 месяцев до 7 лет (52 ребенка) на фоне стабилизации состояния, позволившей провести такие высокотехнологичные методы обследования, как рентгенография органов грудной полости (52 ребенка), мультислайдовая компьютерная томография (50 детей) и бронхоскопия (3 ребенка), удалось диагностировать врожденные пороки развития бронхолегочной системы у 9 детей: простую (2) и кистозную гипоплазию (4) 1-3 долей легких (рис. 1), врожденную лобарную эмфизему (1), панлобулярную эмфизему (1) (рис. 2) и трахеобронхомаляцию (1).
Рисунок 1. Компьютерная томограмма ребенка С. (7 мес) с БЛД на фоне врожденного порока развития легких - кистозной гипоплазии верхней и средней доли правого и нижней доли левого легкого
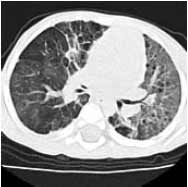
Рисунок 2. Компьютерная томограмма ребенка Ч. (2 мес) с БЛД на фоне врожденного порока развития легкого - панлобулярной эмфиземы
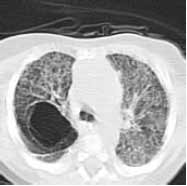
Летальность в наблюдаемой группе больных с БЛД (102 ребенка) составила 10% (10 детей). Все умершие дети имели тяжелое течение заболевания в сочетании с выраженными постгипоксическими изменениями ЦНС и умерли до 6-месячного возраста. При патоморфологическом исследовании у 4 детей данных, указывающих на врожденные пороки развития бронхолегочной системы, выявлено не было.
Как уже упоминалось, после 2-летнего возраста диагноз БЛД считается неправомочным, и мы можем говорить лишь об исходах данного заболевания. У 15 детей, наблюдаемых нами до 3-7-летнего возраста, отмечены следующие исходы:
рецидивирующий обструктивный бронхит (7 детей); бронхиальная астма (3 ребенка); хронический бронхит (2 ребенка); клиническое выздоровление (3 ребенка). Отсутствие вновь выявленных врожденных пороков развития у наблюдаемых детей старше 2-летнего возраста свидетельствует о том, что обычно такие тяжелые изменения манифестируют в более раннем возрасте. Таким образом, в группе недоношенных новорожденных, получавших пролонгированную ИВЛ по поводу различных острых патологических состояний, сопровождавшихся выраженной дыхательной недостаточностью (в основном по поводу респираторного дистресссиндрома), особенно у глубоко недоношенных детей с экстремально низкой массой тела при рождении, высок риск формирования БЛД, как последствия токсического воздействия кислорода и баротравмы на незрелые легочные структуры. Однако в ряде случаев, когда вентиляционная поддержка необходима детям с врожденными пороками развития бронхо-легочной системы, БЛД не является самостоятельным заболеванием, а усугубляет течение основного заболевания. Причиной необходимости возможно более ранней диагностики врожденных изменений дыхательной системы, протекающих под маской БЛД, является принципиальная разница в течении и прогнозе этих патологических состояний.
Тяжесть общего состояния, выраженность дыхательных расстройств, низкая масса тела при рождении и невозможность проведения сложных и инвазивных диагностических исследований являются факторами, осложняющими диагностический поиск у недоношенных детей. Только в процессе катамнестического наблюдения пульмонологом до 2-летнего возраста, а при необходимости и старше, возможно проведение всего диагностического комплекса для верификации диагноза и комплексного лечения этой категории больных.
Список использованной литературы находится в редакции.
Сведения об авторах:
Галина Викторовна Яцык, профессор, главный научный сотрудник отделения для новорожденных и недоношенных детей ГУ НЦЗД РАМН, д-р мед. наук Ирина Владимировна Давыдова, ведущий научный сотрудник отделения наследственных и врожденных болезней органов дыхания ГУ НЦЗД РАМН, канд. мед. наук Елена Николаевна Цыгина, руководитель рентгеновского отделения ГУ НЦЗД РАМН, канд. мед. наук Ольга Владимировна Кустова, сотрудник отделения компьютерной диагностики ГУ НЦЗД РАМН Милана Александровна Басаргина, сотрудник отделения для недоношенных детей ГУ НЦЗД РАМН
| Июнь 2008 г. |