Комплекс из натуральных волокон снижает вес при избыточной массе тела и ожирении: двойное-слепое, рандомизированное, плацебо-контролируемое исследование
Барбара Грубе1, Пи-Вин Чонг2, Кей-Цзиа Лау2 и Ханс-Дитер Орцеховски3
1Общая медицинская практика, Берлин, Германия; 2Отдел исследований и разработки, «ИнКьюФарм Юроп Лтд.», Лондон, Великобритания; 3Институт клинической фармакологии и токсикологии, университетский медицинский комплекс Шарите, Берлин, Германия. Переписка: Пи-Вин Чонг (
Получено 22 ноября 2011 года; принято 20 мая 2012 года; предварительная он-лайн публикация 26 июля 2012 года, doi: 10.1038/oby.2012.165
В доклинических исследованиях и в исследованиях на человеке было показано, что патентованный комплекс из натуральных волокон (литрамин IQP G-002AS), полученный из опунции индийской {Opuntia ficus-indica) и стандартизованный в отношении липофильной активности, понижает всасывание жира, содержащегося в пище, посредством связывания жиров в желудочно-кишечном тракте (ЖКТ). В настоящей работе мы изучали эффективность и безопасность применения IQP G-002AS для снижения веса. В исследовании участвовали сто двадцать пять взрослых пациентов с избыточным весом и ожирением. Участникам исследования была рекомендована физическая нагрузка, кроме того пациентам давали рекомендации в отношении питания, включая планы гипокалорийной диеты (30% калорий из жиров и дефицит в 500 ккал/день). По окончании 2-недельной вводной фазы приема плацебо участники исследования были случайным образом распределены по группам лечения и получали IQP G-002AS (далее IQ) или плацебо по 3 г/день. Первичным ожидаемым результатом являлось изменение массы тела по сравнению с исходным значением; вторичные ожидаемые результаты включали дополнительные показатели ожирения и параметры безопасности. Сто двадцать три участника завершили фазу лечения продолжительностью 12 недель (все пациенты, начавшие получать лечение (ITT): 30 мужчин и 93 женщин; средний индекс массы тела (ИТМ): 29,6 ± 2,8 кг/м2 и средний возраст: 45,4 ± 11,3 лет). Среднее изменение массы тела относительно исходного значения составило 3,8 ± 1,8 кг в группе принимавших IQ в сравнении с 1,4 ± 2,6 кг в группе принимавших плацебо (Р < 0,001). В группе принимавших IQ зарегистрировано больше участников, массе тела которых уменьшилась, по меньшей мере, на 5% в сравнении с исходной массой, чем в группе принимавших плацебо (Р = 0,027). Кроме того, в сравнении с группой плацебо в группе наблюдалось значимо большее уменьшение ИМТ, содержания жира в организме и окружности талии. Комплекс IQ хорошо переносился, его прием не сопровождался нежелательными побочными реакциями. Полученные результаты позволяют заключить, что комплекс из натуральных волокон литрамин IQP G-002AS эффективно стимулирует снижение массы тела.
«06ecumu»/Obesity (2012) doi:10.1038/oby.2012.165
Введение
Ожирение, которое занимает пятое место в мире среди рисков смертности, определяется как избыточное накопление жира, связанное с хроническими заболеваниями и уменьшающее ожидаемую продолжительность жизни, (1). Ожирение возникает вследствие уровня потребления калорий, который превышает расход энергии. Ожирение и избыточный вес отмечаются в 44% случаев сахарного диабета, в 23% случаях ишемической болезни сердца и в 7-41% случаев некоторых видов рака, таких как рак толстой кишки и рак молочной железы (1). Ожирение признано эпидемической проблемой здравоохранения, которая не зависит от пола, этнической принадлежности и возраста и поражает одного из десяти взрослых во всем мире (2). В настоящее время в США насчитывается 100 миллионов людей (взрослых) с избыточным весом или ожирением, а по оценкам, произведенным в рамках проекта Многонационального мониторинга тенденция и факторов развития сердечнососудистых заболеваний (MONICA), ожирением страдает, по меньшей мере, 15% мужчин и 22% женщин в станах Европы. Аналогичные данные получены во многих развивающихся странах (включая Китай, Малайзию и часть Северной Америки). В отличие от развитых стран, социально-экономический статус этих развивающихся стран положительно коррелирует с широким распространением ожирения, которое рассматривается как показатель благосостояния (3).
Широкое распространение и увеличение частоты случаев ожирения в последние два десятилетия бросает тень на социально-экономическое положение стран мира (4). Ожирение связано с депрессией (5-7), которая может быть обусловлена низкой оценкой телесного образа и отрицательной эмоциональной реакцией на соблюдение диеты (8). Согласно исследованию 2010 года, в Соединенных штатах общие прямые и косвенные годовые затраты, связанные с ожирением, составили, по меньшей мере, 215 миллиардов долларов США (9); а в 15 странах Европейской комиссии общие прямые и косвенные годовые затраты, связанные с ожирением, в 2002 году составили примерно 32,8 миллиарда евро (10).
В то же время уменьшение общего употребления калорий может предотвратить развитие ожирения и появление избыточного веса. Ранее проведенные исследования показали, что помимо высокого потребления углеводов, обильное употребление присутствующих в рационе жиров (наряду с недостаточной физической активностью) играет большую роль в развитии ожирения (11). Таким образом, средства, понижающие усвоение в кишечнике содержащихся в пище жиров остается эффективным подходом к регулированию веса.
Вместе с тем, выбор эффективных и безопасных средств уменьшения всасывания жиров, содержащихся в пище, весьма ограничен. Ингибиторы липазы, как правило, регистрируются органами здравоохранения как средства, способствующие снижению веса, уменьшая всасывание жиров, содержащихся в пище, путем ингибирования панкреатической липазы (12-15). Подобная фармакотерапия, однако, связана с побочными эффектами со стороны желудочно-кишечного тракта (ЖКТ), такими как недержание кала, метеоризм с выделениями, маслянистые выделения (13, 16, 17) и поражение печени (18). Между тем, интерес к нефармакологическим средствам, таким как прием пищевых волокон, продолжает расти. Однако ненадлежащее определение характеристик продуктов и недостаток данных клинических исследований ставят под вопрос эффективность пищевых продуктов.
Литрамин IQP G-002AS представляет собой комплекс из натуральных волокон, полученный из опунции индийской {Opuntia ficus-indica), обогащенный растворимыми волокнами акации {Acacia spp.) Показано, что комплекс IQP G-002AS, стандартизованный в отношении липофильной активности, понижает всасывание жира, содержащегося в пище, посредством связывания жиров в желудочно-кишечном тракте. Липофильный комплекс IQP G-002AS связывается с жирами пищи, образуя комплексы жир-волокно, которые не всасываются в кишечнике и поэтому выводятся из организма (19).
Ранее в исследованиях на in vitro моделях ЖКТ, в исследованиях на животных и на человеке была показана эффективность IQP G-002AS в отношении связывания с жирами, при этом уменьшение всасывания жиров, содержащихся в пище, после приема IQP G-002AS составляло до 27% (19). В настоящем исследовании мы изучали эффективность и безопасность IQP G-002AS в рандомизированном, контролируемом исследовании, целью которого являлась проверка гипотезы, согласно которой прием IQP G-002AS способствует увеличению потери веса в сравнении с плацебо при избыточной массе тела и умеренном ожирении у человека.
Методы и процедуры Участники
Участников исследования набирали через объявления в местной прессе. К числу подходящих участников относились мужчины и женщины с ожирением и избыточным весом (25 < ИМТ < 35) в возрасте от 18 до 60 лет. Женщин детородного возраста включали в исследование только после согласия использовать подходящие средства контроля беременности на протяжении всего исследования. Участники с известной чувствительностью к ингредиентам исследуемых средств были исключены из исследования. Другими критериями исключения являлись наличие любого заболевания ЖКТ, расстройство питания в анамнезе, прием препаратов против ожирения, применение препаратов, оказывающих влияние на функцию ЖКТ, злоупотребление алкоголем, отказ от курения в течение предыдущих 6 месяцев, заболевания сердца в анамнезе, заболевания почек в анамнезе, участие в аналогичных исследованиях или в программах снижения веса в течение 6 месяцев до начала настоящего исследования, а также беременность и грудное вскармливание.
Все участники добровольно подписали форму информированного согласия. Клиническое исследование было одобрено комитетом по этике университетского медицинского комплекса Шарите в Берлине и проводилось в соответствии с европейской нормой Международной организации по стандартизации EN ISO 14155, Хельсинской декларацией (Сомерсет, 1996)
Всемирной медицинской ассоциации и руководством по надлежащей клинической практике (CPMP/ICH/135/95).
Исследуемое вмешательство
Данное двойное-слепое, рандомизированное, плацебо-контролируемое клиническое исследование проводилось в двух исследовательских центрах Германии с августа 2010 года по декабрь 2010 года. Германия является одной из европейских стран, значительная часть населения которой имеет избыточный вес или страдает ожирением; в Германии у 61,7% мужчин и 45,2% женщин ИМТ >25 кг/ м2 (20).
Исследование включало вводную фазу приема плацебо продолжительностью 2 недели и фазу лечения продолжительностью 12 недель. Предполагалось, что вводная фаза поможет оценить соблюдение инструкций по приему исследуемого препарата (на основании совокупного приема таблеток плацебо) и режима питания. По завершении 2-недельной вводной фазы участники, которые соблюдали инструкции, по меньшей мере, на 80%, масса тела которых уменьшилась, и участники, суточный прием калорий у которых отклонялся менее, чем на 20% от предписанного, были случайным образом распределены по группам приема IQP G-002AS (IQ) или плацебо, при этом соблюдалось соотношение 1:1. Рандомизация производилась с использованием блоков размером 4 независимым биостатистиком, использовавшим рандомизационную схему BIAS для Windows, версия 9.2 ().
Во время 12-недельного периода лечения участники получали две таблетки IQP G-002AS по 500 мг или такие же таблетки плацебо, три раза в день. Участников просили принимать исследуемый препарат после завтрака, ланча и обеда. Таблетка плацебо, внешне идентичная таблетке IQP G-002AS, содержала 500 мг микрокристаллической целлюлозы вместо активных ингредиентов. Таблетки были упакованы во флаконы и промаркированы независимым фармацевтом для каждого участника в соответствии со схемой рандомизации. Все участники и занятый в исследовании персонал не были информированы относительно распределения по группам.
Всех участников просили соблюдать сбалансированную и слегка гирокалорийную диету на протяжении 2-недельной вводной фазы и 12-недельной фазы лечения. План слегка гипокалорийной диеты был разработан Институтом сердца Германии, Берлин Германия. В соответствии с диетой 30% калорий были получены с жирами, 55% калорий были получены с углеводами и 15% калорий были получены с белками. Норма суточного приема калорий оценивалась (для каждого участника) в соответствии с уравнением Института медицины (ЮМ) Национальной академии на основании возраста, пола, массы тела и интенсивности физической нагрузки (21). Калории, содержащиеся в слегка гипокалорийной диете, были эквиваленты оцененной суточной потребности в калориях минус 500 ккал. Кроме того, участникам рекомендовали постепенно повышать физическую нагрузку (30 минут физической нагрузки умеренной эффективности, такой как ходьба или поездки на велосипеде). Планы диеты были розданы всем участникам перед началом исследования, каждые 4 недели в течение 12 недель лечения участники получали дальнейшие инструкции. Перед началом исследования, через 4 и 8 недель участники получали дневники, которые оценивались во время каждого визита, за исключение исходного.
Скрининг
Скрининговый визит включал сбор анамнеза, общее физикальное обследование и измерение кровяного давления, частоты сердечных сокращений, массы тела, роста, окружности талии и содержания жира в организме. Производился забор крови для биохимического анализа, общего анализа крови, определения липидного профиля и теста на беременность. Анализ образцов крови производился централизованно (Институт медицинской диагностики, Берлин, Германия).
Параметры эффективности
Первичным параметром эффективности являлось изменение массы тела (кг) на 12 неделе в сравнении с исходной массой. Масса тела измерялась исходное и каждые 4 недели в течение 12 недель лечения с использованием калиброванных весов (Tanita ВС-420 SMA; «Танита», Токио, Япония), при этом участники исследовании были в нижнем белье и без обуви. К вторичным параметрам эффективности относились доля участников, потерявших, по меньшей мере, 5 и 10% от исходной массы тела; уменьшение среднего ИМТ; уменьшение средней окружности талии, которую измеряли не уровне середины расстояния между боковой нижней границей ребер и гребнем подвздошной кости; изменение содержания жира в организме (в кг и %), которое измерялось методом анализа биоэлектрического сопротивления с применением валидизированных электронных весов Tanita ВС-420 SMA. Указанные параметры определялись исходно и каждые 4 недели в течение 12 недельного периода лечения.
Параметры безопасности
Оценки безопасности включали измерение показателей жизненно важных функций (таких как пульс и кровяное давление в состоянии покоя) и оценку параметров крови, в том числе: клиническую биохимию (электролиты, содержание жирорастворимых витаминов, функция печени и почек и пуриновый метаболизм), гематологию и липидный профиль (общий холестерин, триглицериды, липопротеины низкой плотности и липопротеины высокой плотности). Пульс и кровяное давление в состоянии покоя оценивались во время каждого визита с помощью стандартных средств измерения; тогда как параметры крови оценивались два раза - во время скринингового обследования и по завершении 12-недельного исследования. Кроме того, участники субъективно оценивали эффективность исследуемого препарата по завершении исследования. Регистрировались все нежелательные явления вне зависимости от их причинно-следственной связи с лечением.
Статистический анализ
Оценка эффективности комплекса IQ производилась на основании нулевой гипотезы, согласно которой различия между IQ и плацебо в отношении среднего уменьшения массы тела отсутствуют.
Объем выборки рассчитывался на основании первичного ожидаемого результата - изменения массы тела в сравнении с исходной массой. Минимальный объем выборки, который составляет 125 участников (с учетом поправки на 30% выбывание) обеспечивает 80% мощность исследования, позволяющую выявлять различия между группами по снижению массы тела в 1,78 кг при уровне значимости 0,045. Поскольку пилотное исследование с применением комплекса IQ не проводилось, оценка объема выборки производилась на основании ограниченных данных, опубликованных в литературе (22,23). В связи с этим была признана необходимость проведения промежуточного анализа без раскрытия рандомизационного кода. С помощью метода Виттеса-Бриттана уровень значимости был скорректирован до 4,5% (двусторонний критерий), что удовлетворяло критерию номинального уровня значимости О'Брайена-Флеминга. Промежуточный анализ (проведенный после того, как половина пациентов завершила участие в 12-недельном исследовании) показал, что коррекции объема выборки не требуется. Демографические и исходные характеристики показателей эффективности и безопасности сначала оценивались методами описательной статистики. Все первичные и вторичные параметры, а также показатели безопасности оценивались как относительные изменения в каждой возрастной группе. Для определения различий между группами использовался параметрический анализ, например, независимый критерий Стьюдента. Дисперсионный анализ повторных измерений ANOVA использовался для оценки всех показателей эффективности в рамках модели повторных измерений. Различие между группами категориальных переменных производилось методом %. Кроме того, среди участников были выделены группа с избыточным весом (ИМТ <30 кг/м2) и группа с ожирением (ИМТ >30 кг/м2), затем был произведен анализ подгрупп с целью определения эффективности комплекса IQP G-002AS только у пациентов с ожирением и только у пациентов с избыточным весом.
Для статистического анализа статистическая значимость (двусторонний критерий) была установлена на уровне Р < 0,05. Все значения, если не указано иное, представлены в виде: среднее ± стандартное отклонение (далее СО). Показатели эффективности и безопасности анализировались для группы всех пациентов, начавших получать лечение (ITT), которые определялись как участники в отношении которых была произведена, по меньшей мере, одна оценка эффективности. Все данные анализировались с использованием программного обеспечения SPSS, версия 19.0 (SPSS, Чикаго, штат Иллинойс).
РЕЗУЛЬТАТЫ
Сто тридцать девять пациентов были приглашены на скрининговое обследование, из них 125 пациентов были зарегистрированы. Все зарегистрированные пациенты продемонстрировали соблюдение инструкций по приему препарата в течение вводной фазы и были случайным образом распределены по группам лечения. Группа пациентов, начавших получать лечение, состояла из 123 человек: 62 участника входили в группу IQ и 61 участник входил в группу плацебо. Один участник был исключен после приема антихолинергетического средства, и еще один участник был исключен, потому что его ИМТ составлял 35,4 кг/м2. Демографические характеристики группыпациентов, начавших получать лечение, приводятся в Таблице 1. Исходные характеристики пациентов в группах IQ и плацебо были одинаковыми; значимые различия между группами в отношении пола, возраста, роста, веса и ИМТ пациентов отсутствовали. В процессе анализа, проведенного в соответствии с протоколом, были исключены еще 5 участников, таким образом, по причинам, указанным на Рисунке 1, в группах IQ и плацебо осталось по 59.
Эффективность
Вес тела. За 2 недели вводной фазы участники в среднем потеряли 1,6% от их исходной массы тела. В конце исследования (неделя 12) потери веса в группе IQ были значимо более высокими в сравнении с группой плацебо (4,5% (3,8 кг) в сравнении с 1,8% (1,4 кг); различие 2,4 кг (Р < 0,001)) (Таблица 2). Значимое различие в изменении массы тела в группах IQ и плацебо наблюдались уже на 4-ой неделе (Р < 0,001) (Рисунок 2).
Всего 75,8% пациентов в группе IQ потеряли, по меньшей мере, 3% от своей исходной массы тела в сравнении с 27,9% пациентов в группе плацебо. Указанное различие между двумя группами было статистически значимым (Р < 0,001). Кроме того, статистически значимо различались доли пациентов, достигших, по меньшей мере, 5% потери веса (IQ: 35,4%; плацебо 16,4%; Р = 0,027) (Рисунок 3).
Проведенный в соответствии с протоколом анализ показал, что средняя потеря веса составила 3,9 ± 1,8 кг в группе участников, получавших комплекс IQ, в сравнении с 1,4 ± 2,6 кг в группе участников, получавших плацебо. Данное различие между исследуемыми группами (2,5 кг) было статистически незначимым (Р < 0,001) (Таблица 2).
Таблица 1 Исходные характеристики всех пациентов, начавших получать лечение
Все пациенты, начавшие получать лечение (п = 123)
Параметр
IQP G-002AS (п= 62
) Плацебо (п = 61)
Пол
Мужчины
16 (25,8%)
14 (23%)
Женщины
46 (74,2%)
47 (77%)
Возраст (годы)
46,0 ± 11,1
44,8 ± 11,6
Вес (кг)
86,6 ± 12,0
83,3 ± 11,2
Рост (см)
170,2 ± 7,8
168,1 ±8,1
ИМТ (кг/м2)
29,8 ±2,9
29,4 ± 2,6
Все данные представлены в виде: среднее ± СО. Значимые различия для всех переменных между группами отсутствуют.
Таблица 2 Среднее (± СО) уменьшения массы тела на 12 неделе по сравнению с исходным значением _
Уменьшение массы тела (кг)
Среднее ± СО (доверительный интервал)
Группа IQP G-002AS
Группа плацебо
Анализ в соответствии с назначенным вмешательством (п = 123)
3,8 ± 1,8 (3,4-4,3)
1,4 ±2,6 (0,8-2,1)
Р < 0,001
Анализ в соответствии с протоколом (п= 118)
3,9 ± 1,8 (3,4-4,4)
1,4 ±2,6 (0,8-2,1)
Р < 0,001
Значения Р получены с помощью параметрического независимого критерия Стьюдента (/-критерия). Положительные значения означают понижение, а отрицательные значения означают повышение.
Был произведен подгрупповой анализ данных о снижении веса у 81 участника с избыточным весом и у 42 участников с ожирением. У пациентов с избыточным весом прием комплекса IQ привел к снижению веса, в более чем в три раза превышающему снижение веса у пациентов, принимавших плацебо (3,6 ± 1,8 кг в сравнении с 0,9 ± 2,3 кг; разница 2,7 кг (Р < 0,001)). У пациентов с ожирением среднее уменьшение массы тела в группе IQ примерно в 1,8 раз превышало соответствующее уменьшение в группе плацебо (4,3 ± 1,9 кг в сравнении с 2,4 ± 2,9 кг; разница 1,9 кг (Р = 0,007)).
Все пациенты, начавшие получать лечение. ИМТ. В конце исследования в группе IQ наблюдалось также уменьшение среднего ИМТ, значимо превышающее уменьшение среднего ИМТ в группе плацебо (1,3 кг/м2 в сравнении с 0,5 кг/м2 (Р < 0,001)) (Таблица 3).Окружность талии. В конце исследования в группе IQ окружность талии уменьшилась значимо более выражено, чем в группе плацебо (разница 1,7 см; Р < 0,001) (Таблица 3).
Содержание жира в организме. Среднее уменьшение содержания жира в организме оказалось более выраженным в группе IQ в сравнении с группой плацебо. По окончании 12 недель исследования различие в массе жира в группах IQ и плацебо составило 1,4 кг (Р < 0,001) или 0,8% (Р = 0,005) (Таблица 3).
Рисунок 1 План исследования и распределение участников.
Безопасность и переносимость
Значимые изменения средних частоты сердечных сокращений и кровяного давления, измеренных исходно и через 12 недель, не зарегистрированы. Кроме того, в обеих группах лечения не наблюдалось клинически значимых изменений параметров крови (Таблица 4).
В конце исследования 98,4% пациентов из группы IQ оценивали переносимость комплекса IQP G-002AS как «хорошую» или «очень хорошую», что совпадало с соответствующими оценками плацебо.
За время исследования были зарегистрированы 26 нежелательных явлений (НЯ) у 24 участников. К числу НЯ относились инфекции верхних дыхательных путей и другие типичные симптомы простуды. Ни одно из зарегистрированных НЯ не было тяжелым и ни одно из зарегистрированных НЯ не было связано с приемом исследуемого продукта.
ОБСУЖДЕНИЕ
Влияние IQP G-002AS на снижение веса (первичная цель)
Первичной целью исследования являлась демонстрация способности IQP G-002AS эффективно понижать вес в течение 12 недель у пациентов с избыточным весом и ожирением. В настоящем исследовании у пациентов, принимавших комплекс IQ, наблюдалось значимо более высокое снижение веса, чем у пациентов, принимавших плацебо; при этом среднее различие между группами составило 2,4 кг; у 35,4% пациентов, принимавших комплекс IQ, уменьшение массы тела составляло, по меньшей мере, 5% от исходного значения. Данный эффект может быть клинически значимым (24, 25), поскольку 5% или более снижение исходного веса уменьшает риск развития метаболического синдрома (в соответствии с критериями Национальной образовательной программы холестерина перечень III для лечения взрослых) на 59% (26).
Рисунок 2 Уменьшение веса с течением времени.
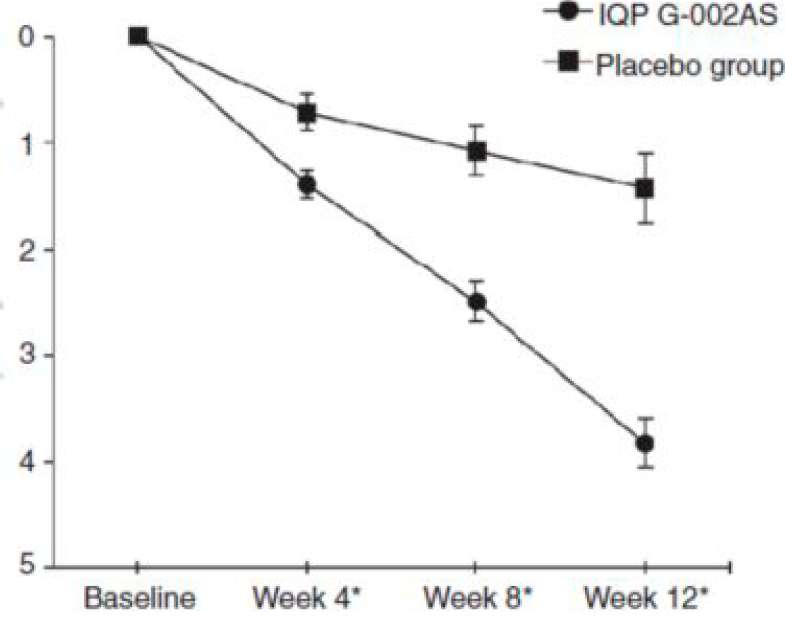
По вертикали: Среднее уменьшение веса, кг
По горизонтали: Исходно, Неделя 4*, Неделя 8*, Неделя 12*
Легенда: группа IQP G-002AS, группа плацебо
Все данные представлены в виде: среднее ± стандартная ошибка среднего. Звездочка означает статистически значимое различие (Р < 0,001) между весом в группах IQP G-002AS и плацебо (данные дисперсионного анализа (ANOVA)).Рисунок 3 Выраженная в процентах доля участников со снижением веса, по меньшей мере, на 3, 5 и 10% пол сравнению с исходным весом.
По вертикали: Доля участников в процентах (%)
По горизонтали: Снижение веса, по меньшей мере, на 3%, Снижение веса, по меньшей мере, на 5%, Снижение веса, по меньшей мере, на 10% Легенда: группа IQP G-002AS, группа плацебо
Звездочка означает статистически значимое различие между группами IQP G-002AS и плацебо (данные получены методом %).Сравнение комплекса IQ и других снижающих вес средств, таких как хитозан (пищевые волокна с похожим механизмом действия) и орлистат (препарат для лечения ожирения) вследствие методологических трудностей, обусловленных недостатком соответствующих прямых сравнительных исследований, затруднено. Джул А.Б. и сотрудники (Jull АВ et al, 27) сообщали о том, что применение хитозана приводит лишь к ограниченному уменьшению веса (0,9 кг). Фармакологическое соединение орлистат в дозировке 60 мг на один прием пищи (три раза в день) и 120 мг на один прием пищи (три раза в день) обеспечивало среднее снижение веса на 1,86 и 2,55 кг, соответственно, после 24 недель приема (28).
ИМТ, содержание жира в организме и окружность талии
Другой результат данного исследования состоит в том, что прием IQP G-002AS в течение 12 недель приводило к значимому уменьшению ИМТ, содержания жира в организме и окружности талии. ИМТ используется ВОЗ в качестве стандарта для определения ожирения, однако его точность ограничена, поскольку подобный стандарт не позволяет учитывать индивидуальные факторы физической конституции, особенно мышечную и костную массу (29). Более того, значимое уменьшение окружности талии у пациентов, принимавших IQ, указывает на более низкое центральное распределение жировой клетчатки, что понижает риск развития диабета, ишемической болезни сердца и гипертензии. Полученный результат очень важен, поскольку окружность талии признается более точным показателем содержания абдоминального жира, чем отношение окружность талии - окружность бедер (25).
Таблица 3 Статистический анализ вторичных параметров эффективности
Вторичные параметры
Группа IQP G-002AS (п=62)
Группа плацебо (п=61)
Среднее ± СО (доверительный интервал)
Среднее ± СО (доверительный интервал)
ИМТ (кг/м2)
1,3 ±0,6 (1,2-1,5) Р<0,001
0,5 ± 0,9 (0,3-0,7)
Окружность талии (см)
3,9 ± 2,7 (3,2-4,6) Р<0,001
2,2 ±2,9 (1,4-3,0)
Содержание жира в организме (кг)
1,9 ±1,8 (1,5-2,4) Р<0,001
0,5 ±2,7 (от-0,2 до 1,2)
Содержание жира в организме (%)
0,7 ±1,7 (0,3-1,1) Р=0,031
-0,1 ±2,5 (от-0,8 до 0,5)
Значения Р получены с помощью параметрического независимого критерия Стьюдента (/-критерия). Положительные значения означают понижение, а отрицательные значения означают повышение.
Ограничения исследования
Последующего наблюдения после завершения настоящего клинического исследования не проводилось. В более продолжительном исследовании может наблюдаться повторная прибавка в весе, как это было зарегистрировано в других ранее проведенных исследованиях (12, 13). Таким образом, целью дальнейших клинических исследований может являться изучение устойчивого продолжительного эффекта снижения веса после приема IQP G-002AS.
Таблица 4 Статистический анализ параметров безопасности
Изменения параметров: значения, полученные до исследования, минус значения, полученные после исследования
Параметры безопасности
Группа IQP G-002AS (Среднее ± СО)
Группа плацебо (Среднее ± СО)
Р-
значение
Систолическое кровяное давление (мм.рт.ст.)
0,5 ± 7,5
0,6 ± 6,3
NS
Диастолическое кровяное давление (мм.рт.ст.)
-0,2 ± 3,4
0,5 ±4,3
NS
Сердечные сокращения/минута
-0,2 ± 3,2
0,1 ±5,0
NS
Уровень гемоглобина (г/дл)
-0,3 ± 0,8
-0,1 ±0,7
NS
Гематокрит (%)
-0,1 ±2,6
0,5 ±2,5
NS
Уровень эритроцитов (Tpt/л)
-0,0 ± 0,2
-0,0 ± 0,2
NS
Уровень тромбоцитов (Gpt/л)
-14,6 ±31,4
-12,7 ±27,3
NS
Уровень лейкоцитов (Gpt/л)
0,0 ± 1,6
-0,3 ± 1,3
NS
Аланинаминотрансфераза (Е/л)
0,7 ± 11,8
2,3 ± 13,7
NS
Аспартатаминотрансфераза (Е/л)
3,1 ± 11,6
3,4 ±6,9
NS
Щелочные фосфаты (Е/л)
2,9 ± 12,9
-0,9 ± 11,9
NS
у-глутамилтрансфераза (Е/л)
2,8 ± 10,1
1,5 ±14,1
NS
Билирубин (мг/дл)
-0,0 ± 0,2
0,0 ± 0,4
NS
Креатинин (мг/дл)
-0,0 ±0,1
0,0 ±0,1
NS
Мочевина (мг/дл)
-0,0 ± 1,1
0,1 ±0,8
NS
Общий холестерин (мг/дл)
-3,0 ±30,1
-1,2 ±30,2
NS
Триглицериды (мг/дл)
5,4 ±63,2
15,9 ±66,2
NS
Липопротеины низкой плотности (мг/дл)
-7,2 ±31,0
-7,5 ± 27,5
NS
Липопротеины высокой плотности (мг/дл)
0,3 ±8,1
0,2 ± 10,2
NS
Витамин А (мг/л)
0,0 ± 0,2
0,1 ±0,3
NS
Витамин D (нг/л)
2,2 ± 8,0
5,1 ±8,4
0,007
Витамин Е (мг/л)
-0,9 ± 4,4
1,4 ±4,3
0,008
Кальций (ммоль/л)
-0,0 ±0,1
0,0 ± 0,0
NS
Натрий (ммоль/л)
0,33 ±2,30
0,40 ± 2,74
NS
Калий (ммоль/л)
-0,44 ± 0,55
-0,32 ±0,56
NS
Магний (ммоль/л)
0,02 ± 0,09
0,04 ±0,10
NS
NS = статистически незначимый. Положительные значения означают понижение, а отрицательные значения означают повышение. Значение Р <0,05 указывает на статистическую значимость значений, выделенных курсивом.
Вторым ограничением настоящего исследования является измерение содержания жира в организме методом анализа биоэлектрического сопротивления. Содержание воды в организме может повлиять на точность анализа биоэлектрического сопротивления.Двухэнергетическая рентгеновская абсорбциометрия является более точным методом; однако, двухэнергетическая
рентгеновская абсорбциометрия связана с повышенным риском облучения участников исследования. Таким образом, метод анализа биоэлектрического сопротивления использовался как разумный компромисс между точностью и безопасностью.
Эффекты литрамина IQP G-002AS, связанные с уменьшением факторов риска развития заболеваний, связанных с ожирением, в настоящем исследовании не оценивались, поскольку протокол исследования и критерии включения в исследование разрабатывались исключительно для определения эффекта IQP G-002AS, связанного со снижением веса. Кроме того, продолжительность исследования в 3 месяца является сравнительно короткой для точного определения возможного улучшения факторов риска развития заболеваний после приема IQP G-002AS. Таким образом, чтобы оценить, как продолжительное употребление IQP G-002AS в сочетании с умеренным снижением веса изменяет связанный с ожирением профиль риска заболевания, можно провести дальнейшее исследование.
Прекращение участия в исследовании/соблюдение инструкций по приему исследуемого препарата и безопасность пациентов
Применение средств против ожирения часто приводит неприятным ощущениям в области живота и связано с нарушением функции печени и психиатрическими побочными эффектами (16-18), что повышает уровень выбывания и понижает степень соблюдения инструкций по приему препарата (примерно 75%) в большинстве клинических исследований препаратов против ожирения. 95,2% пациентов, получавших комплекс IQ, завершили участие в исследовании, что подтверждает безопасность и хорошую переносимость IQP G-002AS. Кроме того, побочные эффекты со стороны ЖКТ, такие как маслянистые выделения, боль в животе, метеоризм и запор, у участников, получавших IQPG-002AS, не отмечались. Это может быть связано с составом IQP G-002AS, комплекса из натуральных волокон, полученных из опунции индийской {Opuntia jicus-indica), обогащенного растворимыми волокнами акации (Acacia spp.), который связывается с жирами, поступающими вместе с пищей. Образование комплексов натуральные волокна IQP О-002А8-жир уменьшают симптомы путем нарушения всасывания жира. Эффективность пищевых волокон в отношении уменьшения числа и понижения степени тяжести побочных реакций со стороны ЖКТ была продемонстрирована в исследовании ингибиторов панкреатической липазы. На основании этого исследования был сделан вывод о том, что слизистое вещество пищевых волокон предупреждает побочные эффекты со стороны ЖКТ, вероятнее всего путем всасывания свободного жира (масла) (30).
Эффективность применения IQP G-002AS в условиях реальной жизни
Благодаря очень низкой частоте выбывания в настоящем исследовании результаты, полученные для пациентов, начавших получать лечение, и пациентов, завершивших исследование в соответствии с протоколом, совпадали. Высокий уровень соблюдения инструкций в соответствии с протоколом позволяет утверждать, что использованная схема (IQP G-002AS плюс гипокалорийная диета плюс умеренная физическая нагрузка) может эффективно применяться в условиях реальной жизни.
Таким образом, представленные результаты подтверждают, что прием внутрь комплекса натуральных волокон литрамин IQP G-002AS является эффективным нефармакологическим средством снижения веса. В настоящее время проводится дополнительное исследование, направленное на изучение поддержания достигнутого снижения веса. Следует отметить, что благоприятное действие достигалось без каких-либо побочных эффектов.
Выражение признательности
Исследование финансировалось «ИнКьюФарм Юроп Лтд.». Мы выражаем благодарность Норману Биттерлиху и Регине Буш за помощь в проведении исследования. Настоящее исследование зарегистрировано под номером: NCT01233349.
Сведения об авторах
Б.Г. являлся главным исследователем в настоящем исследовании. П.-В. Ч. и К.-Ц. Л. являются сотрудниками «ИнКьюФарм Юроп Лтд.», Х.-Д. О. работал в качестве медицинского советника «аналайз энд реалайз аг», клинической исследовательской организации, которая спланировала и провела настоящее исследование.
Формы конфликта интересов Международного комитета редакторов медицинских журналов (ICMJE) для данной статьи см. он-лайн. ©2012 год, Общество по проблемам ожирения
ССЫЛКИ НА ЛИТЕРАТУРУ
1. Stevens G, Mascarenhas М, Mathers С. Global health risks: progress and challenges. Bull World Health Organ 2009;87:646.
2. Finucane MM, Stevens GA, Cowan MJ et al. National, regional, and global trends in body-mass index since 1980: systematic analysis of health examination surveys and epidemiological studies with 960 country-years and 91 million participants. Lancet 2011;377:557-567.
3. Uwaifo AGI, Editor C, Griffing GT. Obesity. Medscape Reference. 2011. Available at: <>. Accessed 20 August 2011.
4. Wellman NS, Friedberg B. Causes and consequences of adult obesity: health, social and economic impacts in the United States. Asia Рас J Clin Nutr 2002; 1 l(Suppl 8):S705-S709.
5. de Wit L, Luppino F, van Straten A et al. Depression and obesity: a metaanalysis of community-based studies. Psychiatry Res 2010;178:230-235.
6. Simon GE, Ludman EJ, Linde JA et al. Association between obesity and depression in middle-aged women. Gen Hosp Psychiatry 2008;30:32-39.
7. Simon GE, Von Korff M, Saunders К et al. Association between obesity and psychiatric disorders in the US adult population. Arch Gen Psychiatry 2006;63:824-830.
8. Wadden ТА, Stunkard AJ. Social and psychological consequences of obesity. Ann Intern Med 1985;103:1062-1067.
9. Hammond RA, Levine R. The economic impact of obesity in the United States. Diabetes Metab Syndr Obes 2010;3:285-295.
10. Fry J, Finley W. The prevalence and costs of obesity in the EU. Proc Nutr Soc 2005;64:359-362.
11. Bray GA, Paeratakul S, Popkin BM. Dietary fat and obesity: a review of animal, clinical and epidemiological studies. Physiol Behav 2004;83: 549-555.
12. Sjustnnn L, Rissanen A, Andersen T et al. Randomised placebo-controlled trial of orlistat for weight loss and prevention of weight regain in obese patients. European Multicentre Orlistat Study Group. Lancet 1998;352: 167-172.
13. Davidson MH, Hauptman J, DiGirolamo M et al. Weight control and risk factor reduction in obese subjects treated for 2 years with orlistat: a randomized controlled trial. JAMA 1999;281:235-242.
14. Russner S, Sjustnnn L, Noack R, Meinders AE, Noseda G. Weight loss, weight maintenance, and improved cardiovascular risk factors after 2 years treatment with orlistat for obesity. European Orlistat Obesity Study Group. Obes Res 2000;8:49-61.
15. Hauptman J, Lucas C, Boldrin MN, Collins H, Segal KR. Orlistat in the long-term treatment of obesity in primary care settings. Arch Fam Med 2000;9:160-167.
16. Collazo-Clavell ML. Safe and effective management of the obese patient. Mayo Clin Proc 1999;74:1255-9; quiz 1259.
17. Johansson K, Neovius K, DeSantis SM, Russner S, Neovius M. Discontinuation due to adverse events in randomized trials of orlistat, sibutramine and rimonabant: a meta-analysis. Obes Rev 2009;10:564-575.
18. US Food and Drug Administration. Safety orlistat (marketed as Alii and Xenical): early communication about an ongoing safety review. 2009:180057-180057.
19. Bachmann C. Ein Fasernkomplex zur Gewichts- reduktion und -kontrolle. Ars Medici thema Phytotherapie 2010:25-27.
20. International Association for the Study of Obesity. Overweight and Obesity in the EU27. International Association for the Study of Obesity: London, 2008.
21. Trumbo P, Schlicker S, Yates AA, Poos M. Dietary reference intakes for energy, carbohydrate, fiber, fat, fatty acids, cholesterol, protein and aminoacids. J Am Diet Assoc 2002;102:1621-1630.
22. Drent ML, van der Veen EA. Lipase inhibition: a novel concept in the treatment of obesity. Int J Obes RelatMetab Disord 1993;17:241-244.
23. Drent M, Larsson I, William-Olsson T et al. Orlistat (Ro 18-0647), a lipase inhibitor, in the treatment of human obesity: a multiple dose study. Int J Obes Relat Metab Disord 1995;19:221-226.
24. US Food and Drug Administration, guidance for industry developing products for weight management guidance for industry developing products for weight management. 2007.
25. National Institutes of Health (NIH), National Heart, Lung, and Blood Institute (NHLBI), North American Association for the Study of Obesity (NAASO). The practical guide: Identification, evaluation and treatment of overweight and obesity in adults. 2000.
26. Phelan S, Wadden ТА, Berkowitz RI et al. Impact of weight loss on the metabolic syndrome. Int J Obes (Lond) 2007;31:1442-1448.
27. Jull AB, Rodgers A, Walker N. Honey as a topical treatment for wounds. Cochrane Database Syst Rev 2008:CD005083.
28. Van Gaal LF, Broom JI, Enzi G, Toplak H. Efficacy and tolerability of orlistat in the treatment of obesity: a 6-month dose-ranging study. Orlistat Dose-Ranging Study Group. Eur J Clin Pharmacol 1998;54:125-132.
29. Romero-Corral A, Virend K, Sierra-Johnson J et al. Accuracy of body mass index to diagnose obesity in the US adult population. Int J Obes (Lond) 2008;32:959-966.
30. Cavaliere H, Floriano I, Medeiros-Neto G. Gastrointestinal side effects of orlistat may be prevented by concomitant prescription of natural fibers (psyllium mucilloid). Int J Obes Relat Metab Disord 2001;25: 1095-1099.
| Июнь 2013 г. |