Опубликовано в журнале:
«Неврология / приложение к журналу Consilium Medicum», 2011, № 15, с. 36-41Прегабалин при лечении вертеброгенной корешковой боли
Ф.А. Хабиров1, Р.Г. Есин1, О.С. Кочергина1, Т.И. Хайбуллин1, Г.И. Ахметова2, М.А. Васильева2, Г.И. Еникеева2, А.А. Исмагилова2, В.М. Каменев2, Ю.Ф. Хабирова3, Э.И. Хузяшева4
1Г0УДП0 Казанская государственная медицинская академия Федерального агентства по здравоохранению и социальному развитию; 2ГМУ Республиканская клиническая больница восстановительного лечения МЗ РТ; 3Клиника "Вертеброневрология"; 40А0 Городская клиническая больница №12, КазаньМеждународная ассоциация по изучению боли определяет боль как "неприятное сенсорное и эмоциональное ощущение, связанное с действительным или возможным повреждением тканей или описываемое в терминах такого повреждения". Боль всегда субъективна. Каждый человек воспринимает боль и употребляет это слово используя свой индивидуальный опыт, связанный с повреждениями, перенесенными ранее. Приведенное определение боли имеет один аспект, не сразу понимаемый всеми врачами: "или описываемое в терминах такого повреждения". Это свидетельствует о том, что боль может возникать и без повреждения тканей, но описываться пациентом как ощущение повреждения кожи, глубоких тканей или несуществующих конечностей. Боль всегда неприятна и поэтому представляет собой эмоциональное восприятие. Именно поэтому П.К.Анохин, И.В.Орлов, Л.Г.Ерохина (1976 г.) рассматривали боль как психофизиологическое состояние человека, отражающее важнейшую интегративную функцию организма, которая мобилизует самые разные функциональные системы его защиты от воздействия повреждающего фактора и включает такие компоненты, как сознание, ощущение, память, мотивации, вегетативные, соматические и поведенческие реакции, эмоции [1].
Распространенность хронической боли в популяции составляет от 2 до 49% [5, 7]. Установлено, что она выше среди женщин, лиц с низкими доходами и пациентов пожилого возраста, связана с депрессией и эмоциональными стрессовыми факторами [6], имеет культурные и этнические особенности. В структуре хронической боли преобладает мышечно-скелетная и головная боль. По данным Всемирной организации здравоохранения, болевые синдромы составляют одну из ведущих причин (от 11 до 40%) обращений к врачу в системе первичной медицинской помощи. Распространенность боли в спине составляет от 12 до 339о- Распространенность нейропатической боли в разных странах составляет в среднем около 7-6% [3].
В структуре неврологического приема пациенты с хронической болью составляют до 52%. Есть также сведения о том, что до 75% пациентов, страдающих хронической болью, предпочитают не обращаться к врачу по разным причинам, в том числе и из-за неадекватной терапии, не принесшей облегчения ранее. По данным отечественных авторов [4] распространенность хронической боли среди населения городов составляет от 13,8 (абдоминальная боль) до 56,7% (мышечно-скелетная боль).
В настоящее время существует несколько вариантов классификации боли. В зависимости от локализации боль подразделяют на соматическую поверхностную (кожные покровы), соматическую глубокую (мышечно-скелетная), висцеральную (внутренние органы), нейропатическую (повреждение периферических нервов) и центральную (структуры центральной нервной системы - ЦНС).
Близка к указанной патогенетическая классификация боли, основанная на вьделении ведущего механизма в формировании боли, что в значительной мере определяет терапевтическую тактику. Различают три основных типа болевых синдромов: ноцицептивные (соматогенные), нейропатические (неврогенные), психогенные.
К ноцицептивным относят синдромы, возникающие при активации ноцицепторов при травме, воспалении, ишемии, растяжении тканей. Ноцицептивную боль разделяют на соматическую и висцеральную. Клинически выделяют посттравматический и послеоперационный болевые синдромы, боль при воспалении суставов, мышц, онкологическую боль, боль при желчнокаменной болезни и др.
Причиной нейропатической боли является органическое поражение разных отделов нервной системы, ответственных за контроль и проведение боли. В 1994 г. международная ассоциация по изучению боли определяла нейропатическую боль как боль, возникающую вследствие первичного повреждения или дисфункции нервной системы. В настоящее время определение уточнено: нейропатическая боль - это боль, возникающая как прямое следствие повреждения или болезни, затрагивающей соматосенсорную систему [Neu PSIG of IASP, 2007 г.].
Наиболее яркими примерами нейропатической боли являются невралгии, фантомный синдром, боль при периферической невропатии, деафферентационная боль и таламический болевой синдром.
В клинической оценке симптомов нейропатической боли выделяют позитивные и негативные симптомы. Термин "позитивный", конечно, не совсем уместен в данном случае. Тем не менее, под позитивными симптомами понимают наличие спонтанных или вызванных алгических явлений. К спонтанным симптомам относятся те признаки, которые возникают без внешних воздействий, и в основе которых лежит спонтанная генерация импульсов ноцицепторами или ноцицептивными волокнами: пароксизмальная боль, дизестезии, парестезии. К вызванным симптомам относят алгические феномены, возникающие как ответ на внешнее воздействие, в основе которых лежит периферическая или центральная сенситизация. Вызванные симптомы: аллодиния (механическая, температурная или химическая), гипералгезия на прикосновение и укол иглой, симпатически поддерживаемая боль. К негативным симптомам относятся объективно выявляемые признаки выпадения сенсорных функций: снижение тактильной (чувствительности к прикосновению), болевой (укол иглой), температурной и вибрационной чувствительности.
Психогенная боль возникает вне зависимости от соматических, висцеральных или нейрональных повреждений и в большей степени определяется психологическими и социальными факторами. Считают, что определяющим в механизме возникновения психогенной боли является психическое состояние человека. Вероятно, под маской психогенной боли скрывается нейропатическая боль, механизм которой мы еще не знаем.
В клинической практике чаще приходится встречаться с микстными формами болевых синдромов (сочетанный болевой синдром), что целесообразно отражать в диагнозе для построения лечебной тактики.
Весьма важным является разделение боли по временным параметрам на острую и хроническую. Острая боль возникает в результате ноцицептивного воздействия, которое может быть обусловлено травмой, заболеванием, а также дисфункцией мышц и внутренних органов. Этот тип боли обычно сопровождается нейроэндокринным стрессом, выраженность которого пропорциональна интенсивности воздействия. Острая боль "предназначена" для обнаружения, локализации и ограничения повреждения тканей, поэтому ее еще называют ноцицептивной болью. Наиболее распространенные виды острой боли посттравматическая, послеоперационая, а также боль, сопряженная с острыми заболеваниями внутренних органов. В большинстве случаев острая боль разрешается самостоятельно или в результате лечения в течение нескольких дней или недель. В тех случаях, когда вследствие нарушенной регенерации или неправильного лечения боль сохраняется, она переходит в категорию хронической. Хроническая боль характеризуется тем, что сохраняется после разрешения острой фазы заболевания или по истечении времени, достаточного для излечения. В большинстве случаев этот период варьирует от 1 до 6 мес. Причиной хронической боли могут быть периферическое ноцицептивное воздействие, а также дисфункция периферической или ЦНС. Нейроэндокринная реакция на стресс ослаблена или отсутствует, отмечаются выраженные нарушения сна и аффективные расстройства.
Боль в спине является, вероятно, одним из самых распространенных страданий человека. Распространенность ее варьирует от 12 до 33% в общей популяции, при этом до половины пациентов с болью в спине имеют неиропатическую боль, связанную с компрессией корешка или спинномозгового нерва.
Лечение нейропатической боли предусматривает использование антидепрессантов, антиконвульсантов, опиоидов и местных анестетиков. В последнее время внимание исследователей привлекает новый антиконвульсант прегабалин. Препарат обладает высокой аффинностью к a2d-протеину пресинаптических окончаний, связывание с которым приводит к уменьшению высвобождения медиаторов, имеющих отношение к передаче болевых импульсов, в том числе глутамата, норадреналина и субстанции Р. Благодаря снижению секреции данных медиаторов прегабалин селективно подавляет возбудимость ноцицептивых нейронов [2]. Препарат хорошо зарекомендовал себя при лечении некоторых форм нейропатической боли, однако отсутствуют данные о его эффективности при вертеброгенных радикулопатиях. Исходя из этого, мы посчитали актуальным и практически важным оценить эффективность прегабалина при лечении вертеброгенных корешковых болей, что и составило цель настоящего исследования.
Пациенты и методы
Исследование проведено на базе неврологических отделений и поликлиники Республиканской клинической больницы восстановительного лечения МЗ РТ в январе-апреле 2008 г. Обследованы 180 пациентов в возрасте от 28 до 69 лет (средний возраст 36,8±6,7 года; 102 (57%) мужчины, 78 (43%) женщин. Критерием включение в исследование служило наличие хронических поясничных болей, ассоциированных с вертеброгенными пояснично-крестцовыми радикулопатиями. Из исследования были исключены пациенты, у которых болевой синдром был обусловлен соматической патологией или специфическими (опухолевыми, воспалительными, травматическими и др.) поражениями позвоночника. Вся выборка случайным методом была разделена на 2 равные группы. Пациенты 1-й (основной) группы, помимо базисной терапии, получали прегабалин (торговое название Лирика) в дозе 300 мг/сут; 2-й (контрольной) - только базисную терапию. Базисная терапия включала соблюдение рационального нейроортопедического режима, назначение нестероидных противовоспалительных средств (диклофенак в стандартных дозах), сосудистых препаратов (эуфиллин внутривенно капельно в стандартных дозах), физиотерапию (СМТ), лечебную физкультуру и массаж. Всем больным для подтверждения диагноза было проведено комплексное неврологическое и неироортопедическое обследование, дополненное рентгенографией и/или компьютерной/магнитно-резонансной томографией. Выраженность болей оценивали с помощью визуальной аналоговой шкалы (ВАШ), а для более подробной характеристики болевого синдрома использовали МакГилловский (сенсорную и аффективную шкалы) и DN4-onpoc-ники. Последний состоит из двух блоков: первый (7 вопросов) заполняется на основании опроса пациента и позволяет оценить позитивные сенсорные симптомы (спонтанные боли, парестезии, дизестезии); второй (3 вопроса) блок основывается на результатах клинического обследования и позволяет выявить аллодинию и негативные сенсорные симптомы.
Статистическую обработку результатов производили на IBM PC-совместимом компьютере с помощью ПО StatSoft Statistica 7.0 с использованием параметрических и непараметрических методов.
Результаты и обсуждение
Клиническая картина заболевания на момент начала исследования у всех больных была однотипной и складывалась из вертебрального (нарушение статики и динамики пояснично-крестцового отдела позвоночника, болезненность при пальпации ПДС и др.), экстр авертебрального (преимущественно мышечно-тонические и нейродистрофические изменения в ягодичных, грушевидной и ишиокруральных мышцах) и радикулярного синдромов. Признаки радикулопатии L5 выявлены у 41% пациентов, S1 - у 45%, L5 и S1 - у 14%. Выраженность болевого синдрома по ВАШ и МакГилловскому опроснику в группах была сопоставимой (р>0,1), что можно сказать и о частоте позитивных и негативных симптомов нейропатической боли по опроснику DN4 (р>0,1; рис. 1, 2).
Рис. 1. Оценки (Me) по ВАШ, сенсорной (СМГО) и аффективной (АМГО) шкалам МакГилловского опросника до начала лечения.
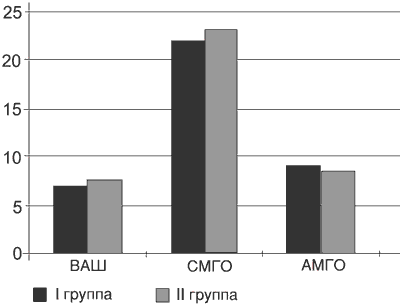
Рис. 2. Частота (в %) позитивных и негативных симптомов невропатической боли (опросник DN4) до начала лечения.
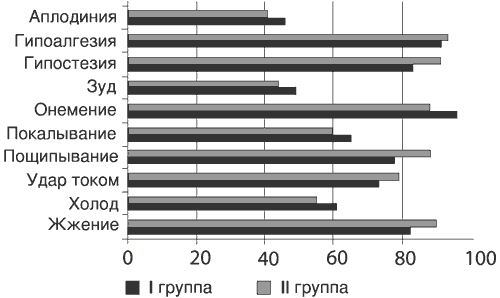
После проведенного курса лечения (через 6 нед после начала исследования) в обеих группах наблюдалась положительная динамика как по субъективным, так и объективным показателям. О субъективном улучшении в 1-й группе сообщили 90% пациентов, о значительном улучшении - 55%, а во 2-й - только 69 (р<0,01) и 12% (р<0,01 соответственно). Оценки по ВАШ и шкалам МакГилловского опросника (рис. 3) также снизились в обеих группах, но в наибольшей степени в 1-й (р<0,05). Частота позитивных и негативных симптомов нейропатической боли в 1-й группе также уменьшилась в большей степени, чем во 2-й (особенно дизестезии и аллодинии, рис. 4).
Рис. 3. Оценки (Me) по ВАШ, сенсорной (СМГО) и аффективной (АМГО) шкалам МакГилловского опросника после курса терапии.
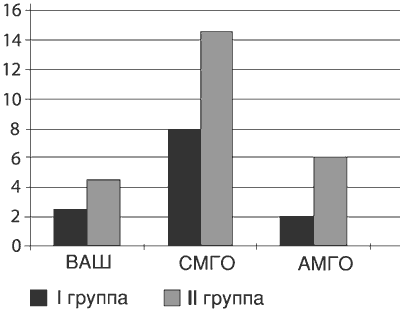
Рис. 4. Частота (в %) позитивных и негативных симптомов невропатической боли (опросник DN4) после курса терапии.
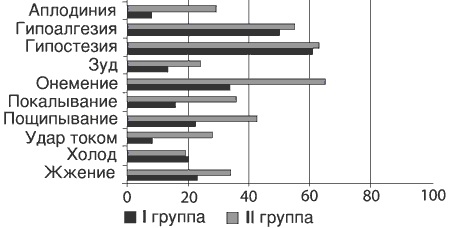
Побочные эффекты при терапии прегабалином были редкими (головокружение у 3 пациентов) и не потребовали отмены препарата. Таким образом, результаты исследования свидетельствуют о высокой эффективности прегабалина при хронических вертеброгенных корешковых синдромах. Тем не менее, при наличии несомненной положительной динамики в 1-й группе в целом, у 9 (10%) больных лечение оказалось неэффективным, а еще у 7 больных его можно было охарактеризовать как недостаточно эффективное. При детальном анализе особенностей болевого синдрома в этой подгруппе выяснилось, что при сопоставимых оценках по ВАШ и сенсорной шкале МакГилловского опросника по сравнению с остальными пациентами 1-й группы количество положительных ответов на вопросы DN-4, а также оценка по аффективной шкале МакГилловского опросника у них были значимо ниже. Так, из 17 человек 4 ответили положительно только на 2 вопроса DN-4, 8 - на 3 вопроса; между тем среди оставшихся пациентов не было ни одного, кто бы не ответил положительно менее чем на 4 вопроса DN-4. Таким образом, недостаточную эффективность прегабалина у этих больных, вероятно, следует объяснить тем, что боли у них были преимущественно не нейропатического характера.
Заключение
Прегабалин является эффективным препаратом для купирования нейропатических болей, связанных с вертеброгенными пояснично-крестцовыми радикулопатиями, однако следует подчеркнуть, что необходимо четко соблюдать показания к его назначению. Вертеброгенный болевой синдром является смешанным и складывается из нейропатического и ноцицептивного компонентов (а при хроническом течении, как правило, присоединяется еще и психогенный компонент) и вклад этих составляющих в каждом конкретном случае может существенно варьировать. В частности, по нашим наблюдениям, у отдельных пациентов даже при наличии очевидных признаков радикулопатии неиропатическии компонент не является доминирующим в структуре болевого синдрома. Этот факт еще раз подчеркивает необходимость тщательного обследования пациента и дифференциальной диагностики ноцицептивных и нейропатических болей, например, с помощью опросника DN-4. В целом, на основании проведенного исследования Лирику следует рекомендовать к широкому применению в практической неврологии как препарат выбора, показавший хорошую переносимость, минимальные побочные действия, высокую терапевтическую эффективность при лечении нейропатической боли.
ЛИТЕРАТУРА
1. Анохин П.К., Орлов И.В., Брохина Л.Г. Боль Большая медицинская энциклопедия. 3-е изд.М, 1976; 3- 869-71.
2. Данилов А.Б. Прегабалин (Лирика) влечении нейропатической боли.Лечение нервных болезней. 2007; 1- 55.
3. Данилов. Нейропатическая боль, Давыдов О.С. Нейропатическая боль. М.: Боргес, 2007.
4. Павленко С.С, Тов Н.Л. Исследование распространенности основных видов хронических болевых синдромов среди населения Новосибирска. Боль. 2003; 1: 13-6.
5. Павленко С.С, Денисов В.Н., Фомин Г.И. Организация медицинской помощи больным с хроническими болевыми синдромами. Новосибирск:ГП "Новосибирский полиграфкомбинат", 2002.
6. Carson J.V., Keefe F.J., Goli Vet al. Forgiveness and chronic low back pain: a preliminary study examining the relationship of forgiveness to pain, anger, and psychological distress.] Pain 2005; 6 (2): 84-91.
7. Gureje O., Simon G.E., Von Korff M. A cross-national study of the course of persistent pain inprimary care.Pain. 2001;92:195-200.
| Апрель 2012 г. |