Опубликовано в журнале:
«Русский медицинский журнал», 2008, том 16, №9 с. 2-11Первые доказательства безопасности для эндометрия экстракта клопогона кистевидного (Actaea или Cimicifuga racemosa) CR BNO 1055
Карел Рауш1, Козима Брюкер2, Кристоф Горков3 , Вольфганг Вуттке4
1Университет Чарльза, Прага, Чехия 2Клиника Северного Нюрнберга, Нюрнберг, Германия 3Бионорика АГ, Ноймаркт, Германия 4Отделение клинической и экспериментальной эндокринологии Университета Георга–Августа, г. Гёттинген, ГерманияВпери– и постменопаузальном периоде более двух третей женщин страдают от климактерических нарушений. Выраженные вазомоторные проявления, включая приливы, отмечаются у 70–75% женщин. Примерно у половины подобных пациенток эти симптомы сохраняются в течение 5 и более лет. Двадцать процентов женщин называют эти проявления нестерпимыми [1]. В этой связи именно данные нарушения являются решающим фактором, заставляющим начинать лечение.
Вазомоторные симптомы (приливы) вызваны повышенной активностью гипоталамического центра, выделяющего гонадотропин-рилизинг гормон, который, в свою очередь, действует на нейроны, регулирующие температуру [2]. Приливы коррелируют с изменениями в секреции лютеинизирующего гормона (ЛГ) [3], а в процессе регуляции температуры участвуют многочисленные медиаторы, включая адреналин и серотонин [4,5].
Постменопаузальная гормональная заместительная терапия (ГЗТ), то есть прием эстрогенов с прогестинами или без, в течение длительного времени являлась стандартом в лечении в связи с тем, что она воздействует на большинство из связанных с менопаузой жалоб и заболеваний, таких как остеопороз. В то же время результаты недавно проведенного исследования Heart and Estrogen/Progestin Replacement Study, Women’s Health Initiative и Million Women Study показали, что ГЗТ сопровождается повышенным риском развития рака груди, тромбоэмболии, инсульта и, возможно, заболеваний сердца [6–8]. В этой связи все больший интерес привлекают альтернативные неэстрогенные виды лечения, и их преимущества и недостатки активно изучаются.
Альтернативные виды лечения включают препараты растительного происхождения, такие как соя, красный клевер и клопогон кистевидный (Actaea или Cimicifuga racemosa (экстракт Цимицифуги рацемозы)). В связи с содержанием в соевых экстрактах изофлавонатов даидзеина и генистейна необходимо учитывать их потенциальные негативные эстрогенные эффекты. При приеме в высоких дозах в течение 5 лет гиперплазия эндометрия развивалась у 3,37% женщин, получавших лечение, и у 0% женщин, получавших плацебо [9].
Экстракт Цимицифуги рацемозы является более перспективным в связи с тем, что его прием приводит к снижению выраженности климактерических жалоб и усилению синтеза костной ткани [10–14]. Несмотря на предполагаемую эстроген-селективность, в экстрактах Цимицифуги рацемозы до настоящего времени не выявлено веществ с эстрогенными свойствами [15–19].
Наличие на рынке различных экстрактов Цимицифуги рацемозы, полученных с применением разных технологий, может являться объяснением того, что в одних исследованиях было показано, что данный экстракт действует независимо от эстрогеновых рецепторов, а в других, что он обладает эстрогенной или даже антиэстрогенной активностью.
С другой стороны, в экспериментальных условиях даже при применении высоких доз экстрактов Цимицифуги рацемозы не было установлено никаких эстрогенных эффектов на матку крыс с удаленными яичниками [15,20].
В недавно проведенных исследованиях было показано, что экстракт Цимицифуги рацемозы содержит вещества, связывающиеся с серотониновыми рецепторами, действие которых может объяснять эффекты данного препарата на приливы [21]. Также показано существование дофаминергического действия [22], при этом известно, что эстрогенные вещества повышают концентрацию дофамина в мозге женщин, находящихся в постменопаузальном периоде [23]. Тем не менее точный механизм действия экстракта Цимицифуги рацемозы на симптомы, вызванные недостатком эстрогенов, продолжает оставаться неясным.
Одним из основных недостатков ГЗТ является то, что прием эстрогенов у женщин, имеющих матку, всегда должен сопровождаться также приемом прогестинов с учетом того, что при приеме только эстрогенов возрастает риск развития рака эндометрия. В связи с тем, что экстракт Цимицифуги рацемозы рассматривается в качестве альтернативного метода лечения, возникает вопрос о том, действительно ли данное растительное средство не приводит к гиперплазии эндометрия. Целью настоящего исследования являлось получение достаточного количества данных о развитии гиперплазии и/или других изменений эндометрия и изучение безопасности и переносимости, а также эффективности приема экстракта Цимицифуги рацемозы BNO 1055 в течение 12 месяцев. Как и при проведении исследований ГЗТ, мы следовали рекомендациям European Agency for the Evaluation of Medicinal Products [24].
Методы
Дизайн исследования
Данное открытое, несравнительное, проспективное, многоцентровое международное исследование было проведено в 44 гинекологических клиниках Чехии и Польши в период с 2002 по 2004 г. (одобрено Чешским институтом контроля над лекарственными препаратами за номером 1779/02 и Польским центром по регистрации клинических исследований за номером 196/02). Проведение исследования, обработка данных и их статистический анализ были выполнены в соответствии с рекомендациями International Conference on Harmonization–Good Clinical Practice (ICH-GCP) и Хельсинкской декларацией. Протокол исследования был одобрен девятью этическими комитетами обеих стран до начала работы (рис. 1).
Рис. 1. Схема проведения исследования

После получения письменной и устной информации о сущности, целях, рисках, преимуществах и длительности работы, а также об альтернативных методах лечения женщины подписывали информированное согласие на участие в исследовании [25,26].
Необходимое число больных в исследовании было рассчитано в соответствии с рекомендациями European Agency for the Evaluation of Medicinal Products [24]. Для получения необходимого уровня статистической достоверности требовалось не менее 300 пациенток, которые должны были получать лечение в течение 12 месяцев (верхняя граница 95%–го доверительного интервала не должна превышать точечный оценочный показатель более чем на 2%). Для того чтобы подтвердить, что безопасность данного препарата не уступает таковой для ГЗТ, частота гиперплазии и других изменений эндометрия не должна была превышать 2% в соответствии с рекомендациями European Agency for the Evaluation of Medicinal Products [24]. Таким образом, число женщин с подобными изменениями должно было быть не более шести. В связи с тем, что ожидаемая частота выбывания из исследования составляла 20%, мы включили в исследование 400 женщин.
Состояние пациенток оценивали при первом (за 1-4 недели до начала исследования), втором (начало исследования), третьем (через 4 недели после начала исследования), четвертом (через 13 недель после начала исследования), пятом (через 26 недель после начала исследования), шестом (через 39 недель после начала исследования) и седьмом (через 52 недели после начала исследования)визитах.
Критерии включения/исключения
В исследование включали пациенток, соответствующих следующим критериям включения: амбулаторные пациентки; получено информированное согласие; возраст от 50 до 75 лет; после менопаузы с симптомами, вызванными недостатком эстрогенов; не менее 7 приливов в течение нескольких недель до первого и второго осмотров; наличие матки; индекс массы тела менее или равный 28 кг/м2; последний менструальный период не менее двух лет назад; уровень фолликулостимулирующего гормона 35 мЕд/мл и более; уровень 17β–эстрадиола менее 40 пг/мл; толщина эндометрия 5 мм или менее; отсутствие патологических изменений в эндометрии, то есть при гистологическом исследовании было достаточно материала для установления диагноза в соответствии с классификацией Committee for Proprietary Medical Products (CPMP) [24], модифицированной Kurman и Mazur [27], и эндометрий был отнесен к категории 2–0 (атрофический и/или неактивный эндометрий), 3–1 (секреторный эндометрий, циклический тип), 3–2 (секреторный эндометрий, прогестационный тип) или 4–0 (пролиферативный эндометрий) или материала было недостаточно (категория 1–0, недостаточно ткани для диагноза), а толщина эндометрий составляла 5 мм или менее.
Пациентки, имевшие какие-либо из критериев исключения (табл. 1), в исследование не включались.
Таблица 1. Критерии исключения
- Отказ от дачи информированного согласия
- Стадии 0-0 и с 5 по 8 по данным биопсии эндометрия согласно классификации Kurman и Mazur [27]
- Подозрительные данные по результатам трансвагинального ультразвукового исследования
- Мазок из шейки матки с отклонениями в цитологической картине, неэпителиальные злокачественные опухоли
- Прием эстрогенов, тиболона, селективных модуляторов эстрогеновых рецепторов, антиэстрогенных препаратов в течение 6 месяцев до первого визита
- Прием комбинации эстрогена и прогестерона в течение месяца до первого визита
- Применение мази эстриола в течение двух недель до первого визита
- Применение парентеральных форм половых гормонов в течение 12-36 месяцев до первого визита
- Пищевые добавки, содержащие фитоэстрогены в течение шести недель до первого визита
- Острый флебит, панкреатит
- Хронические заболевания, оказывающие действие на абсорбцию лекарственных препаратов, их метаболизм и выведение
- Острые и хронические заболевания печени на момент осмотра или в анамнезе
- Неконтролируемый сахарный диабет
- Нестабильная нелеченная гипертония
- Комбинация артериальной гипертензии, сахарного диабета и ожирения
- Заболевания системы гемостаза
- Наличие в анамнезе тромбоэмболии
- Серповидно-клеточная анемия
- Не поддающаяся лечению гипертриглицеридемия
- Влагалищное кровотечение невыясненной этиологии в течение последних 2 лет
- Любые злокачественные заболевания, особенно эстроген-зависимые
- Гестационный герпес в течение предыдущей беременности
- Мигрень
- Аллергия к любым компонентам исследуемого препарата
Препарат
Изучавшийся препарат сухого водно-этанолового экстракта Цимицифуги рацемозы BNO 1055 из корневища Actaea (она же экстракт Цимицифуги рацемозы – клопогон кистевидный) (Климадинон®, Бионорика, Германия), произведенный в соответствии с Good Manufacturing Practice, был предоставлен в форме таблеток в оболочке. Ежедневная доза состояла из двух таблеток внутрь. Каждая таблетка (серия номер 2471502) содержала от 1,66 до 2,86 мг экстракта, что со ответствует 20 мг растительного препарата.
Соответствующим образом упакованные и подписанные упаковки, содержавшие 200 таблеток, выдавали на втором, четвертом, пятом и шестом визитах.
Оценивавшиеся показатели безопасности и эффективности
Биопсию эндометрия выполняли по стандартной методике [9] с применением вакуумного забора эндометрия при первом посещении, в конце исследования, если пациентки прекращали участие преждевременно, при развитии метроррагии и через 52 недели после начала исследования (визит 7) [28]. Повторную биопсию проводили в случае отсутствия ткани эндометрия (стадия 0–0) на первом визите или стадии 0–0 или 1–0 (количество эндометриальной ткани недостаточно для постановки диагноза) на 7–м визите или при преждевременном прекращении участия в исследовании. Образцы ткани оценивали два независимых эксперта согласно ранее описанной классификации CPMP [24], модифицированной Kurman и Mazur [27]. При наличии расхождений во мнении двух патологов спорные образцы исследовал третий специалист. Если они не могли придти к единому мнению, для дальнейшего анализа использовали наиболее неблагоприятный диагноз [24]. Патологи не знали ни дизайна исследования, ни типа применявшегося препарата.
Толщину эндометрия оценивали с применением УЗИ (частота ≥5 Мгц), учитывая все слои в области дна матки, где толщина была максимальной на первом, пятом и седьмом визитах, а также в конце исследования в случае его преждевременного завершения. Толщина эндометрия более 5 мм на фоне лечения рассматривалась, как неблагоприятный эффект препарата. Этим пациенткам выполняли выскабливание или гистероскопию после забора биопсии.
Наличие и интенсивность кровотечений (оценивавшихся по следующей классификации: кровотечения нет, «мажущие» выделения, слабое, умеренное, выраженное) регистрировали по данным дневников пациенток. Эпизоды кровотечения и сопутствующие жалобы фиксировали, как побочные эффекты лечения.
Осмотр груди, измерение артериального давления, частоты сердечных сокращений и веса тела проводили на первом, пятом и седьмом визитах, а также в случае преждевременного прекращения участия в исследовании.
Если при исследовании груди обнаруживали какие–либо отклонения, пациенткам выполняли маммографию до включения в исследование (если подобное исследование проводили в течение 12 месяцев до включения в работу, его не повторяли), в конце исследования, а также в случае преждевременного прекращения участия в исследовании, если маммография не выполнялась в течение последних 12 месяцев. Ультразвуковое исследование груди выполняли в случае преждевременного прекращения участия в исследовании, если последняя маммограмма была сделана не ранее чем за 12 месяцев, и осмотр груди не выявил изменений.
Все маммограммы были оценены централизованно и ретроспективно с целью выявления любых изменений по сравнению с исходными исследованиями, проведенными до начала лечения. Плотность молочных желез оценивали в соответствии с Wolfe [29] и BIRADS [30].
На первом, четвертом, пятом и седьмом визитах проводили забор крови для исследования уровней 17β–эстрадиола, Л Г, ФСГ и маркеров активности остеобластов (остеокальцин) и остеокластов (β–CrossLaps – продукты распада коллагена 1 α 1), которое выполняли с помощью системы ELECSYS 2010 (Roche–Diagnostics, Мангейм, Германия). Для изучения метаболизма костной ткани женщин разделили на три подгруппы в зависимости от исходных уровней β–CrossLaps (высокий исходный уровень: ≥0,5 нг/мл; средний – от 0,217 до 0,5 нг/мл, низкий – менее 0,217 нг/мл).
Уровни общего холестерина, липопротеинов выской плотности (ЛПВП), липопротеинов низкой плотности (ЛПНП) и триглицеридов оценивали с применением ферментных цветовых тестов.
Исследование уровней креатинина, общего белка, натрия, калия, общего билирубина, глутамат-оксалоацетат-трансаминазы, глутамат-пируват-трансаминазы, гамма-глутамил-трансферазы, щелочной фосфатазы, глюкозы, общего анализа крови, уровня гемоглобина и состояния системы гемостаза (международное нормализованное отношение) проводили на первом, пятом и седьмом визитах в центральной лаборатории.
Развитие (серьезных) побочных эффектов оценивали (тип, тяжесть, длительность, связь с приемом препарата) и регистрировали.
Для оценки тяжести климактерических нарушений пациентки заполняли анкету Menopause Rating Scale II (MRSII) (табл. 2) [31]. Частота (раз в день) и тяжесть приливов (легкая – приливы без потливости и нарушений повседневной деятельности, средняя – приливы с или без потливости, нарушающие, но не препятствующие повседневной активности, тяжелая – приливы с потливостью, препятствующие повседневной активности) отмечались пациентками в дневниках.
Таблица 2. Симптомы, оцениваемые в опроснике Menopause Rating Scale II
- Приливы жара, потливость (эпизоды потливости)
- Дискомфорт в области сердца (необычное ощущение сердцебиения, беспокойство)
- Проблемы со сном (сложности с засыпанием, сном, ранние пробуждения)
- Депрессивное настроение (ощущение печали, плаксивость, резкие колебания настроения, отсутствие желания что–либо делать)
- Раздражительность (нервозность, внутреннее напряжение, агрессивность)
- Тревожность (внутреннее беспокойство, паника)
- Физическое и умственное истощение (снижение работоспособности, нарушения памяти, сниженная концентрация внимания, забывчивость)
- Сексуальные нарушения (изменения сексуального желания, сексуальной активности и удовлетворения от нее)
- Нарушения мочеиспускания (затруднения при мочеиспускании, поллакиурия, недержание мочи)
- Сухость влагалища (ощущение сухости или жжения во влагалище, затруднения при половом акте)
- Проблемы с костями и мышцами (боли в суставах, ревматические симптомы)
Степень тяжести: нет – 0, легкая – 1, средняя – 2, тяжелая – 3, очень тяжелая – 4. Статистический анализ
Основным оценивавшимся в исследовании показателем являлась частота встречаемости гиперплазии эндометрия или более тяжелых побочных эффектов (рак эндометрия) после приема препарата в течение 52 недель. До проведения дальнейшего анализа полученные данные разделяли на положительные (при наличии гиперплазии и/или рака эндометрия) или отрицательные, если подобные изменения отсутствовали. В дальнейшем рассчитывали вероятность развития этих осложнений и ее 95%–й доверительный интервал [32].
Статистический анализ других показателей был основан на данных, полученных у 375 женщин, которые прошли лечение в течение 52 недель в соответствии с протоколом исследования. Были оценены исходные характеристики этих пациенток, толщина эндометрия, плотность груди, эпизоды кровотечений из влагалища, основные показатели общего осмотра, а также побочные эффекты. В случае если показатели концентрации гормонов в крови выходили за пределы крайних для данного метода измерения значений, их заменяли на крайние значения.
Изменения лабораторных показателей рассчитывали как разницу между исходными значениями и таковыми после 52 недель лечения. Для выявления различий использовали знаковый ранговый критерий.
Особый интерес уделяли анализу средних изменений остеокальцина и β–CrossLaps. Для оценки изменений этих показателей на фоне лечения также применяли знаковый ранговый критерий.
Сумма баллов ответов на вопросы с 1 по 11 из MRS II до и после лечения была сопоставлена с применением теста Вилкоксона.
Приливы оценивали с применением количественного показателя, который составляли, суммируя ежедневное число легких приливов, умноженное на 1, число приливов средней степени тяжести, умноженное на 2, и число тяжелых приливов, умноженное на 3. Рассчитывали средние значения данного показателя за период 4 недели. Изменения данного среднего показателя сравнивали, используя значения, полученные после 26 и 52–й недель лечения с применением теста Вилкоксона.
Значения р≤0,05 рассматривали как статистически достоверные. Все расчеты были выполнены с применением программы SAS версия 8.2.
Результаты
Общие сведения об участницах исследования представлены в таблице 3. В целом на предмет возможности участия в исследовании были оценены 686 больных. Одна пациентка не пришла на второй визит, а 285 не могли быть включены в исследование. Основными причинами этого были нарушения критериев включения или исключения (в большинстве случаев – данные гистологического исследования). У пяти женщин гиперплазия и/или более тяжелые изменения эндометрия были выявлены до начала исследования (в двух случаях стадия 6–1 – простая гиперплазия эндометрия (железы с нарушениями структуры, включая измененный характер пролиферации и кистозную железистую гиперплазию) и по одному случаю стадии 5–3 – эндометрий с по липами (полипы с признаками пролиферации/гиперплазии), 7–1 – рак эндометрия, и 8–1 – другое (виды гиперплазии или опухоли, не указанные в категориях 5–3, 6 или 7). В общей сложности 400 женщин соответствовали всем критериям включения и ни одному из критериев исключения и стали участницами исследования. Прежде временно прекратили участие в исследовании 25 пациенток (16 – отказ от ин формированного согласия, 7 – недостаточная эффективность, 2 – нарушение режима приема препарата). В общей сложности 375 женщин прошли лечение в течение 52 недель в соответствии с протоколом исследования. Из них одна отказалась от биопсии на седьмом визите, а результаты биопсии еще 39 женщин не поддавались оценке в связи с тем, что относились к стадии 0–0 (эндометриальной ткани не получено) или 1–0 (количество эндометриальной ткани недостаточно для постановки диагноза) (n=24) или вследствие того, что биопсию брали более чем через 42 дня после прекращения приема препарата (n=15). Таким образом, основной оценивавшийся показатель мог быть проанализирован по данным, полученным у 335 пациенток.
В таблице 3 представлены основные демографические показатели 400 женщин, включенных в исследование, и 375 женщин, закончивших его.
Таблица 3. Демографические характеристики пациенток
Показатель Среднее±СО Минимум Медиана Максимум Возраст, лет ЗИ 56,45±4,77 48,92 55,59 74,94 ВИ 56,38±4,73 48,92 55,43 74,94 Рост, см ЗИ 166,14±6,38 145,00 165,00 184,00 ВИ 166,09±6,34 145,00 166,00 184,00 Вес, кг ЗИ 68,16±8,47 44,00 68,00 88,00 ВИ 68,14±8,55 44,00 68,00 88,00 Индекс массы тела, кг/м2 ЗИ 24,65±2,40 18,56 24,68 29,00 ВИ 24,66±2,41 18,36 24,67 29,00 Длительность менопаузы, мес. ЗИ 71,27±53,38 18,00 50,83 334,43 ВИ 71,14±52,86 18,00 50,58 334,43 1 7β–эстрадиол, пг/мла ЗИ 19,86±9,38 5,00 21,50 39,40 ВИ 20,19±9,03 5,00 21,50 39,40 MRS II (общая сумма) ЗИ 13,82±7,49 3,00 12,00 36,00 ВИ 13,92±7,45 3,00 13,00 36,00 Приливы (среднее за 4 недели) ЗИ 11,9±8,9 1,9 9,1 55,9 ВИ 11,9±8,8 1,9 9,1 55,9 ЗИ – закончившие исследование (n=375); ВИ – включенные в исследование (n=400); MRS – Menopaus Rating Scale; СО - стандартное отклонение; a – значения ниже пределов измерения заменены минимальными определяемыми значениями Биопсии эндометрия
Из 375 женщин, закончивших исследование, трехкратная оценка биопсийного материала была необходима в 6 случаях на первом визите, в одном случае на пятом визите и в 4 случаях на седьмом визите.
Распределение стадий результатов биопсии эндометрия представлено на рисунке 2. Несмотря на то, что шесть случаев гиперплазии и/или более тяжелых изменений эндометрия рассматривались в качестве удовлетворительного результата в соответствии с рекомендациями CPMP, ни одна из следующих категорий:
- Эндометрий с полипами (полипы с признаками пролиферации/гиперплазии)
- Простой гиперпластический эндометрий (железы только со структурными отклонениями, включая измененную пролиферацию и кистозную гиперплазию желез)
- Комплексная гиперплазия эндометрия (скопления желез со структурными отклонениями без цитологической атипии)
- Атипичная гиперплазия эндометрия (железы с цитологическими и структурными отклонениями)
- Рак (эндометриоидный)
- Рак (неэндометриоидный)
- Рак (другой)
- Другое (типы гиперплазии и опухолей, не указанные в категориях 5–3, 6 или 7) не было выявлено в ходе исследования.
Рис. 2. Частота разных стадий по результатам гистологического исследования ткани эндометрия согласно классификации Kurman и Mazur [27] среди пациенток, биопсии которых могли быть оценены (n=335) до начала исследования (первый визит) и после 52 недель лечения (седьмой визит)
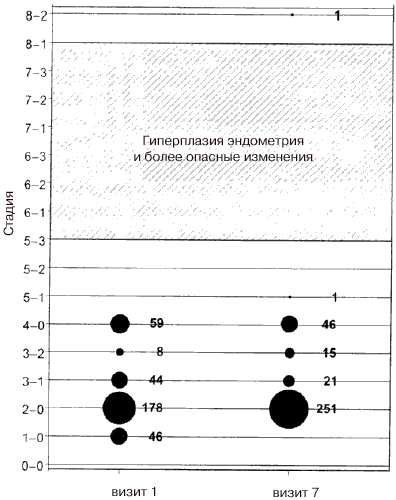
Таким образом, вероятность развития гиперплазии эндометрия или более тяжелых изменений составила 0,0 с верхней границей 95%–го доверительного интервала 0,011.
Наиболее часто при исследовании биопсийного материала, полученного как в начале, так и в конце исследования, обнаруживали атрофию, что согласуется с возрастом и гормональным статусом обследованных. Количество случаев атрофии по мере проведения исследования увеличивалось (178 до начала исследования, 251 по окончании исследования), что в сочетании с отсутствием осложнений со стороны эндометрия описанным выше (рис. 2), поддерживает гипотезу о безопасности экстракта Цимицифуги рацемозы. Из 178 женщин, у которых исходно имела место атрофия, пролиферация эндометрия была выявлена в конце исследования у 16. Более выраженные изменения у этих женщин выявлены не были. Из 55 женщин с пролиферативным эндометрием в начале исследования к его окончанию у 38 имела место картина атрофии. Более того, на фоне лечения было отмечено всего два случая формирования эндометрия стадий выше 4–0 (пролиферативный эндометрий). Одна пациентка была отнесена к стадии 5–1 (эндометрий с атрофическими полипами) и еще одна к 8–2 (менее серьезные изменения, не указанные в рубриках с 0–0 по 5–2), а именно – полипоидный эндометрий с некротическими и пролиферативными характеристиками. В обоих случаях эти данные не были патологическими.
Среди прекративших исследование случаев гиперплазии или более опасных изменений выявлено не было. Таким образом, в одном случае имела место стадия 0–0 (ткани эндометрия не получено), в пяти – 2–0 (атрофичный и/или неактивный эндометрий) и в двух – 4–0 (пролиферативный эндометрий). Среди 27 выбывших из исследования 17 женщин отказались от проведения повторной биопсии. Среди пациенток, данные биопсии которых не были включены в окончательный анализ в связи с тем, что последняя была выполнена более чем через 42 дня после окончания приема препарата (n=15), не было выявлено случаев гиперплазии или более опасных изменений. В этой группе были выявлены стадия 1–0 (ткани эндометрия не получено) в пяти случаях, стадия 2–0 (атрофичный и/или неактивный эндометрий) в четырех, 3–1 (секреторный эндометрий, циклический тип) в трех и 4–0 (пролиферативный эндометрий) в трех.
Толщина эндометрия
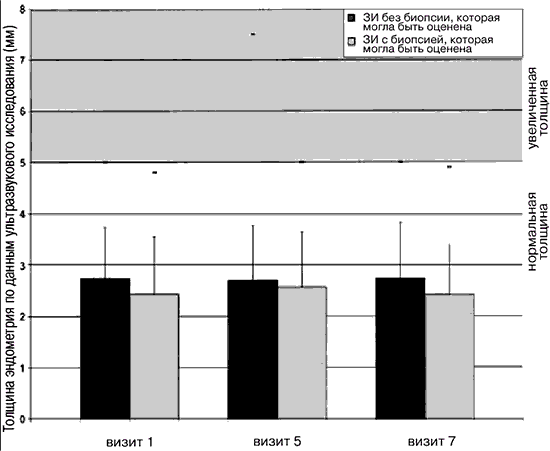
В соответствии с результатами биопсии эндометрия толщина последнего не на фоне лечения не увеличивалась. Это относится как к тем случаям, которые были включены в окончательный анализ (n=335), так и к тем, которые не были в него включены (n=39) (рис. 3). Среди 39 результатов биопсии, не включенных в анализ, большинство было получено более чем через 42 дня после последнего приема препарата (n=15) или выявления стадий 0–0 (22, отсутствие ткани эндометрия) и 1–0 (2, недостаточно материала для установки диагноза). Только в двух случаях толщина эндометрия превышала 5 мм, что считается верхней границей нормы. В одном случае толщина эндометрия составила 7,5 мм на пятом визите (26 недель) и гистологическое исследование выявило стадию 4–0. У другой больной толщина эндометрия составила 9,0 мм на шестом визите (39 недель). По данным гистологического исследования была выявлена стадия 2–0 (атрофия).
Рис. 3. Толщину эндометрия оценивали по данным ультразвукового исследования на первом визите и после 26 и 52–й недель исследования среди женщин, прошедших его до конца (ЗИ – закончившие исследование), у которых удалось получить биопсию, которая могла быть оценена (n=335), а также у тех, кто прошел исследование, однако их биопсии не могли быть оценены в связи с тем, что они относились к стадиям 0–0, 1–0 или были выполнены более чем через 42 дня после последнего приема препарата (n=39). Показаны средние значения±стандартное отклонение, а также максимальные значения.
Влагалищные кровотечения
В общей сложности 59 женщин отметили эпизоды кровотечения в период приема препарата (36 – мажущие выделения, 8 – слабое кровотечение, 9 – кровотечение средней тяжести, 6 – тяжелое кровотечение). Уровни эстрадиола и ФСГ сыворотки крови оставались в пределах нормальных постменопаузальных значений (ФСГ≥35 мЕд/мл, 17β–эстрадиол <40 пг/мл). Из 59 женщин, отмечавших кровотечения, у 17 они продолжались более 10 дней. Независимо от интенсивности кровотечений признаков гиперплазии выявлено не было, ни в одном из этих случаев толщина эндометрия не превышала 5 мм. У большинства женщин, сообщавших о влагалищных кровотечениях (75%), имел место атрофический или неактивный эндометрий. Среди оставшихся 25% выявляли секреторный (циклический тип) или пролиферативный эндометрий.
Исследования груди, артериального давления, частоты сердечных сокращений, веса тела
Результаты исследования груди, артериального давления, частоты сердечных сокращений и веса тела на фоне лечения не изменялись.
Маммограммы (плотность груди)
Отклонения при маммографии были выявлены только у одной женщины, у которой во время исследования был выявлен инвазивный рак груди. Этот случай был расценен как не связанный с приемом препарата (подробности данного случая представлены в разделе «Побочные эффекты»). Маммограмма, выполненная у этой женщины до начала исследования, не показывала каких–либо подозрительных изменений.
Маммограммы 138 женщин, полученные до и после лечения, были централизованно проанализированы.
То, что централизованно проанализированы были маммограммы, полученные лишь у 138 женщин, было вызвано тремя причинами:
- В связи с юридическими проблемами маммограммы, полученные в Польше, были исключены из это го анализа. Таким образом, централизованно могли быть оценены только маммограммы, полученные в Чехии (n=327).
- Идея централизованного анализа возникла только после окончания исследования. В связи с этим данный анализ не был частью информированного согласия. Во избежание нарушения закона о защите личной информации некоторые исследователи отказались предоставить необходимые материалы. В связи с этим 139 женщин из 9 центров не могли быть оценены.
- Некоторые радиологи не предоставили достаточной информации. В некоторых случаях маммограммы, полученные до или после лечения были потеряны. Некоторые были сделаны более чем за 12 месяцев до начала исследования. В связи с этим еще 50 женщин не могли быть включены в этот анализ.
По данным 138 маммограмм, оцененных с применением классификаций Wolfe [29] и BI–RADS [30], не было отмечено увеличения плотности груди, за исключением одной женщины (0,72%) с повышенной плотностью.
Метаболизм костной ткани
В соответствии с концентрацией β–CrossLaps 80 женщин были отнесены к группе с высоким уровнем (среднее значение 0,72±0,21 нг/мл, минимум 0,51 нг/мл, медиана 0,66 нг/мл, максимум 1,57 нг/мл). В группах со средним (среднее значение 0,33±0,08 нг/мл, минимум 0,22 нг/мл, медиана 0,33 нг/мл, максимум 0,50 нг/мл) и низким (среднее значение 0,16±0,05 нг/мл, минимум 0,01 нг/мл, медиана 0,18 нг/мл, максимум 0,22 нг/мл) уровнями была 201 и 79 женщин соответственно. На фоне лечения у женщин из группы с низкими концентрациями отмечено достоверное увеличение уровня β–CrossLaps на 137,78, 166,63 и 96,31% после 12, 26 и 52–й недель лечения соответственно. В те же временные периоды было отмечено повышение уровня остеокальцина на 34,47, 52,52 и 36,64% соответственно.
В группе со средним уровнем метаболизм костной ткани изменялся меньше. В то же время в группе с высокими концентрациями имело место существенное снижение β–CrossLaps (примерно на 26%), то есть было отмечено антирезорбтивное действие по сравнению с исходными показателями (изменение через 13, 26 и 52 недели лечения: 9,62, 23,36 и 25,67% соответственно), при этом остеокальцин повышался лишь незначительно (изменение по сравнению с исходными показателями после 13, 26 и 52 недель лечения: 7,12, 8,25 и 5,66% соответственно). Антирезорбтивное действие, заключавшееся в снижении уровня маркера костной резорбции (β–CrossLaps), а также отсутствии существенных изменений концентрации остеокальцина (формирование костей) у пациенток с исходными значениями β–Cross Laps выше 0,5 нг/мл, представлено на рисунке 4.
Рис. 4. Представлены относительные изменения по сравнению с исходными показателями значений β–CrossLaps и остеокальцина из подгруппы с высокими исходными показателями (≥ 0,5 нг/мл) (n=80) β–CrossLaps и достоверными (*) значениями р по сравнению с исходными показателям (критерий знаков)

Гормоны
Было отмечено небольшое статистически достоверное повышение уровней 17β-эстрадиола и снижение ЛГ и ФСГ (табл. 4). Повышение уровня эстрадиола было связано с двумя женщинами, у которых, по–видимому, имела место овуляция и концентрация 17β–эстрадиола составила 800 и 821,5 пг/мл, что сочеталось с существенным снижением уровней ЛГ и ФСГ. В связи с этим более информативным является среднее значение концентрации 17β–эстрадиола, которое снизилось на 4,6 мг/мл. Следует отметить, впрочем, что степень этих изменений была далека от клинической значимости.
Таблица 4. Средние изменения лабораторных показателей (на 52–й неделе по сравнению с исходными)
Неделя 0 (среднее±СО) Неделя 52 (среднее±СО) Различие (среднее±СО) p Гормоны 17β–эстрадиол (пг/мл)а 19,86±9,38 22,66±50,35 2,81±50,38 ДР ФСГ (мЕд/мл)б 75,05±27,36 68,86±33,44 -6,19±29,45 ДР ЛГ (мЕд/мл)а 31,79±11,48 29,64±13,26 -2,15±11,85 ДР Липиды Общий холестерин (мг/дл) 202,91±26,41 216,06±36,07 13,15±37,28 ДР ЛПВП (мг/дл) 64,28±12,60 71,38±15,52 7,11±12,65 ДР ЛПНП (мг/дл) 124,14±22,59 132,10±30,25 7,96±31,47 ДР Триглицериды (мг/дл) 110,47±38,75 138,93±85,03 28,46±84,55 ДР Биохимические показатели Глутамат-оксалоацетат-трансаминаза (ед/л) 21,78±10,37 31,47±11,67 9,69±13,77 ДР Глутамат-пируват-трансаминаза (ед/л) 25,21±11,53 28,48±35,22 3,27±35,53 ДР Гамма-глутамил-трансфераза (ед/л) 26,61±17,47 27,44±31,54 0,83±32,84 НР Общий билирубин (мг/дл) 0,51±0,25 0,56±0,29 0,05±0,25 ДР Мочевая кислота (мг/дл) 4,42±1,10 4,42±1,10 0,00±1,12 НР Глюкоза (мг/дл) 98,46±13,42 100,62±27,78 2,16±28,84 НР Гемостаз МНО 1,01±0,11 0,96±0,26 -0,05±0,27 ДР ФСГ – фолликуло–стимулирующий гормон; ЛГ – лютеинизирующий гормон; ЛПВП – липопротеиды высокой плотности; ЛПНП – липопротеиды низкой плотности; МНО – международное нормализованное отношение; ДР – достоверное различие, НР – недостоверное различие
а – значения ниже нижних пределов измерения заменены минимальными определяемыми значениями; б – значения выше высших пределов измерения заменены максимальными определяемыми значениямиМетаболизм липидов
Известно, что недостаток 17β–эстрадиола приводит к изменениям в метаболизме липидов и в особенности к увеличению уровня общего холестерина. Изменения уровней липидов у женщин, получавших лечение, представлены в таблице 4. Статистически достоверное увеличение имело место в случае общего холестерина, ЛПВП, ЛПНП и триглицеридов, хотя эти изменения не были клинически значимыми и согласовались со снижением уровней 17β–эстрадиола. Не было отмечено никаких субъективных жалоб, связанных с данными изменениями. Соотношение ЛПНП/ЛПВП снизилось у 64,8% пациенток к концу исследования (52–я неделя) и увеличилось у 35,2%. Только 4 женщины (1%) имели значения более 3,5, то есть выше порогового показателя, указывающего на повышение риска развития ишемической болезни сердца.
Биохимические показатели
Результаты обследования, имеющие патофизиологическое значение, представлены в таблице 4. Несмотря на наличие в некоторых случаях статистически достоверных различий, их клиническое значение представляется сомнительным. Верхние значения нормы для глутамат-оксалоацетат-трансаминазы, глутамат-пируват-трансаминазы и гамма-глутамил-трансферазы согласно протоколу должны были превышать нормальные значения в три раза. У 3 женщин были отмечены более высокие показатели глутамат-пируват-трансаминазы. У двух женщин отмечен эпизод повышения уровня данного фермента на пятом визите, при этом к седьмому визиту показатель пришел в норму. У одной женщины повышение имело место на седьмом визите. В связи с тем, что дальнейшее обследование не проводилось, данное отклонение расценено как окончательное. В общей сложности у 7 женщин было выявлено повышение уровня гамма-глутамил трансферазы. У одной пациентки данный показатель был повышен и на пятом, и на седьмом визитах, у пяти – только на пятом и у одной только на седьмом. Все эти отклонения регистрировали, как неопасные побочные эффекты, не связанные с приемом препарата. Эти повышения оказали влияние на средние значения. В отношении показателей, не представленных в таблице 4 (натрий, калий, креатинин, щелочная фосфатаза, общий белок и данные общего анализа крови), изменений выявлено не было.
Гемостаз
Клинически значимых изменений международного нормализованного отношения отмечено не было (табл. 4).
MRS II/среднее число приливов за 4 недели
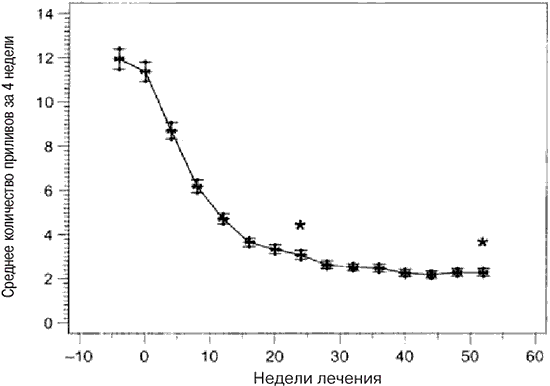
Выраженность климактерических нарушений, отражавшаяся в сумме баллов MRS II (вопросы с 1 по 11, табл. 2) снизилась примерно на 50% (рис. 5). На фоне приема экстракта Цимицифуги рацемозы BNO 1055 среднее количество приливов за 4 недели снизилось на 80,7% по сравнению с исходными значениями (рис. 6).
Рис. 5. Общая сумма баллов Menopause Rating Scale II (MRS II) (вопросы с 1 по 11) и изменения по сравнению с исходными показателями после 4, 13, 26, 39 и 52–й недель лечения экстрактом Цимицифуги рацемозы BNO 1055 (ежедневная доза соот ветствует 40 мг растительного препарата). Представлены среднее±стандартная ошибка среднего и значения р (* – достоверные) по сравнению с исходными показателями (тест Вилкоксона)

Рис. 6. Среднее количество приливов за 4 недели (количество приливов в день, умноженное на коэффициент, зависящий от выраженности: тяжелый – 3, умеренный – 2, легкий – 1; сумма всех дней за предшествующие 4 недели, разделенная на количество дней). Представлены среднее±стандартная ошибка среднего и значения р (* – достоверные) по сравнению с исходными показателями (тест Вилкоксона, коррекция по Bonferroni)
Побочные эффекты
В общей сложности было зарегистрировано 752 побочных эффекта (ПЭ). Из них 414 (55%) были расценены, как не связанные с приемом препарата и 12 (1,6%) были исключены из дальнейшего анализа. Связь с приемом препарата была расценена как возможная в 318 (42%) и вероятная в 8 (1%) случаях ПЭ. Большинство из связанных с приемом препарата побочных эффектов (295 случаев) выражалось в повышении уровня липидов сыворотки крови (97 – повышение уровня три глицеридов, 95 – повышение общего холестерина, 101 – повышение ЛПНП, 2 – снижение ЛПВП). Также имели место 4 случая желудочно–кишечных расстройств. Семь случаев ПЭ, связанных с приемом препарата, были отнесены к категории заболеваний половой системы и молочных желез. В одном из этих случаев гиперплазия эндометрия (9 мм) была установлена по данным УЗИ, в то время как гистологическое исследование подобных изменений не подтвердило. Еще 20 случаев ПЭ, вызванных приемом препарата, были связаны с другими органами и системами (один случай гипотиреоидизма, четыре – повышение уровня глюкозы, два – повышение гамма-глутамил-трансферазы, один – повышение калия, два случая рака шейки матки второй стадии, четыре случая артериальной гипертензии, один – тромбофлебита, один – аллергического дерматита, два случая головных болей, один случай депрессии и один случай гриппа).
Тяжесть ПЭ была легкой в 88% случаев, умеренной в 10,5% и тяжелой в 1,9%.
Примерно в 65% случаев ПЭ проходили без остаточных явлений, в 30% они сохранялись до конца исследования. Ни в одном из 25 случаев преждевременное прекращение участия в исследовании не было связано с ПЭ.
Из 752 случаев ПЭ 8 были расценены как серьезные. Они имели место у 3 женщин: одна плановая госпитализация по поводу холецистэктомии вследствие желчекаменной болезни; у одной из 3 женщин имели место 5 побочных эффектов, 4 явились результатом несчастного случая (афакия, кровоизлияние в глаз, разрыв глазного яблока, патологический перелом, перелом плечевой кости) и один – длительной госпитализации по поводу острого бронхита. Еще одна женщина с диагнозом рака молочной железы в период лечения была госпитализирована, и ей было выполнено оперативное вмешательство, зарегистрированное в качестве отдельного побочного эффекта. Операция была выполнена по поводу так называемой интервальной опухоли, при этом на маммограмме, выполненной до начала исследования, никаких изменений не было. В связи с тем, что злокачественной опухоли молочной железы требуется от 7 до 10 лет для того, чтобы достигнуть стадии, на которой она может быть выявлена, данный случай никак не может быть связан с приемом препарата. Все серьезные побочные эффекты, по нашему мнению, не были связаны с приемом препарата.
Обсуждение
Настоящее исследование является первым, в котором подтверждена безопасность экстракта Цимицифуги рацемозы для эндометрия. Биопсия эндометрия является золотым стандартом в оценке состояния по след него. В соответствии с рекомендациями Committee for Proprietary Medicinal Products (CPMP) [24] для такого по объему исследования допустимо было развитие 6 случаев гиперплазии и более тяжелых изменений эндометрия, при этом мы не выявили ни одного подобного случая. Наиболее важным является отсутствие при знаков стимулирующего действия экстракта на толщину эндометрия, что свидетельствует о высочайшей безопасности исследовавшегося препарата Цимицифуги рацемозы BNO 1055 для эндометрия.
Постменопаузальная атрофия эндометрия является физиологическим процессом. Влагалищные кровотечения у женщин с атрофическим эндометрием – хорошо известное явление, которое может быть связано со склеротическими и дегенеративными изменениями сосудов эндометрия [33]. В связи с тем, что количество женщин с атрофией эндометрия за период лечения увеличилось, вероятность кровотечений также возросла.
У женщин с секреторным или пролиферативным эндометрием может иметь место нерегулярный цикл. Активность эстрадиола может повышаться в результате нерегулярного созревания фолликулов с последующим кровотечением. Подобные изменения с временными повышениями уровня эстрадиола были отмечены у 15 женщин, и это привело к повышению средних показателей уровня эстрадиола в период исследования. В этой связи мы считаем более показательными значения медианы уровня эстрадиола в крови, которые снижались.
Хорошо известно, что прием экзогенных половых стероидов, а именно прогестерона и эстрадиола, может приводить к повышению плотности ткани молочных желез [34], что рассматривается в качестве одного из факторов риска развития рака молочных желез [7]. В некоторых исследованиях было показано увеличение плотности ткани молочных желез на 50% на фоне комбинированной гормональной терапии [35]. Увеличение плотности молочных желез вызвано разрастанием как соединительной, так и эпителиальной тканей. Плотная ткань молочных желез рассматривается в качестве фактора риска развития рака [29,36–38]. Маммографическое исследование не выявило изменений плотности молочных желез среди тех женщин, данные которых могли быть оценены централизованно. Единственный случай рака молочных желез, выявленный во время исследования, был расценен как не связанный с исследовавшимся препаратом.
В исследовании не было отмечено никаких клинически значимых изменений уровней гормонов. Также не было выявлено значимых колебаний показателей биохимического анализа крови и гемостаза. В то же время имели место существенные повышения общего холестерина, ЛПНП, глутамат-оксалоацетат-трансаминазы и глутамат-пируват-трансаминазы. С другой стороны, благоприятное снижение соотношения ЛПНП к ЛПВП имело место у 65% женщин к концу исследования, а повышение – у 35%. Кроме того, было отмечено повышение ЛПВП. Следует отметить, что клиническое значение этих данных, как благоприятных, так и неблагоприятных, продолжает оставаться сомнительным. Кроме того, следует принять во внимание методологические особенности измерения уровней липидов крови. Международные стандарты данных показателей могут существенно варьировать, так, например, международным стандартом для холестерина является значение 6,5 ммоль/л, при этом оно может колебаться от 5,24 до 7,86 ммоль/л. То же самое имеет место и в случае триглицеридов, верхняя граница которых может колебаться от 1,3 до 1,6 ммоль/л, в то время как международное значение составляет 1,46 ммоль/л. Некоторые из неблагоприятных изменений, представленных в таблице 4, могут быть статистически значимыми и при этом их клиническое значение представляется несущественным. Если применять самые строгие стандарты, то значительная часть пациенток на момент начала исследования нуждалась в проведении лечения статинами [39], особенно это касается женщин с факторами риска, такими как наличие семейного анамнеза, артериальной гипертензии, сахарного диабета и ишемической болезни сердца.
Среди ПЭ, расцененных исследователями как возможно или вероятно вызванных приемом препарата, большинство было связано с повышением уровней холестерина, ЛПНП и триглицеридов. К сожалению, повышение общего холестерина и ЛПНП регистрировали как отдельные побочные эффекты, в то время как они взаимосвязаны (и составили около 60% всех ПЭ). Практически все женщины не имели симптомов, и они не получали лечения и не были направлены к специалистам. В настоящем исследовании не было отмечено неожиданных серьезных реакций на исследованный препарат. Кроме того, ни один из серьезных ПЭ не был связан с приемом препарата.
Что касается значения снижения значений MRS II и количества и выраженности приливов, то кто–то может заметить, что в некоторых исследованиях было отмечено статистически достоверное снижение данных показателей на 40% среди получавших плацебо. Несмотря на отсутствие контрольной группы в настоящем исследовании, снижение показателя MRS II на 50% и количества приливов на 80% являются весьма многообещающими. Следует отметить, что эти изменения носили долгосрочный характер, и нами не было отмечено их колебаний.
Результаты, касающиеся костных маркеров, весьма интересны. Учитывая данные, указывающие на возможность благоприятного влияния препарата на метаболизм костной ткани у женщин с повышением последнего, а также данные экспериментальных исследований, изучение действия данного вещества на костную ткань может стать целью последующих исследований. В этих исследованиях могут быть применены такие методы, как изучение микроструктуры костей, денситометрия и, возможно определение даже более специфичных и чувствительных костных маркеров. В проведенном ранее клиническом исследовании, а также в экспериментальной работе, выполненной на крысах, было отмечено положительное действие на костную ткань [12,40].
Учитывая постоянное увеличение количества женщин, находящихся в постменопаузальном периоде и имеющих различные связанные с этим нарушения, а также возможные побочные эффекты от долговременной гормональной терапии и недавно выявленное действие фитоэстрогенов на эндометрий, применение безопасного для эндометрия экстракта Цимицифуги рацемозы является важным дополнением для лечения симптомов эстрогенного дефицита. Возможное профилактическое действие на костную ткань является дополнительным преимуществом данного препарата и должно быть исследовано более подробно.
Заключение
Результаты настоящего исследования показали, что двенадцатимесячное лечение экстрактом Цимицифуги рацемозы BNO 1055 является безопасным для эндометрия по данным биопсий последнего. Отсутствие действия на плотность молочных желез может свидетельствовать об отсутствии повышения риска развития рака. Кроме того, отсутствие действия на печеночные ферменты и гемостатические факторы может свидетельствовать о том, что данный экстракт не имеет подобных побочных эффектов. На основании показателей, отражающих обмен костной ткани, можно определенно утверждать, что экстракт Цимицифуги рацемозы BNO 1055 обладает антирезорбтивной активностью. Хотя нами было выявлено повышение уровней общего холестерина и ЛПНП, данный эффект может быть компенсирован ростом ЛПВП. Негативное действие триглицеридов нуждается в дальнейшем изучении.
Снижение количества приливов на 80% отражает существенное субъективное улучшение.
Реферат подготовлен В.В. Иремашвили по материалам статьи Raus K., Brucker C., Gorkow C., Wuttke W. First–time proof of endometrial safety of the special black cohosh extract (Actaea or Cimicifuga racemosa extracts) CR BNO 1055, The Journal of The North American Menopause Society 2006; 13 (4): 678–691
| Февраль 2009 г. |