Займы на карту . |
Опубликовано в журнале:
«Клинические перспективы гастроэнтерологии, гепатологии», 2009, №1, с. 35-41Лечение и профилактика поражений слизистой оболочки желудочно-кишечного тракта в терапевтической практике
А.Л. Верткин, Е.И. Вовк, А.В. Наумов, В.С. Иванов, А.В. Отпущенко, П.А. Семенова
Московский государственный медико-стоматологический университет, Городская клиническая больница № 50 г. МосквыЦель обзора. Охарактеризовать этиологические факторы, особенности патогенеза, клинической картины, подходов к лечению и профилактике желудочно-кишечных кровотечений(ЖКК) у пациентов с ишемической болезнью сердца(ИБС).
Последние данные литературы. Острые эрозии или язвы желудка и двенадцатиперстной кишки, приведшие к ЖКК у больных, умерших от инфаркта миокарда или расслоения аневризмы аорты, выявляются в 21% случаев. В структуре причин летального исхода у больных стационара терапевтического профиля скорой медицинской помощи частота ЖКК при острых заболеваниях сердца и аорты составила 8%. Ключевые факторы, ведущие к развитию ЖКК у пациентов с ИБС, в первую очередь в острый период инфаркта миокарда, представлены инфекцией Helicobacter pylori и гастропатией, обусловленной лечением нестероидными противовоспалительными препаратами(НПВП).
Риск развития НПВП-гастропатии наиболее высок у пациентов с язвенной болезнью в анамнезе, в возрасте старше 65 лет, принимающих кортикостероиды. Не связанными между собой факторами наиболее высокого риска возникновения ЖКК у больных в критическом состоянии вне зависимости от основного заболевания являются дыхательная недостаточность, коагулопатия, искусственная вентиляции легких более 48 ч. Адекватная антисекреторная терапия позволяет решить как минимум три задачи: прекратить активное кровотечение, предотвратить его рецидив и ЖКК в принципе. На базе результатов доказательных исследований оптимальными по антисекреторной активности, быстроте развития эффекта, отсутствию толерантности, безопасности и простоте применения у больных с ЖКК признаны ингибиторы протонной помпы (уровень доказательности А).
Заключение. ЖКК вносят существенный «вклад» в структуру летальных исходов у пациентов с сердечно-сосудистой патологией. Единственная эффективная стратегия их профилактики у больных категории высокого риска – назначение ингибиторов протонной помпы.
Ключевые слова: инфаркт миокарда, желудочно-кишечные кровотечения, профилактика, лечение.
Treatment and prophylaxis of gastro-intestinal mucosa lesions in therapeutic practice
A.L. Vertkin, Ye.I. Vovk, A.V. Naumov, M.M. Shamuilova, V.S. Ivanov, V.S. Filimonov, A.V. Otpuschenko
The aim of review. To characterize etiological factors, features of pathogenesis, clinical pattern, approaches to treatment and prophylaxis of gastro-intestinal bleedings(GIB) in patients with ischemic heart disease(IHD).
Basic statements. Acute erosions or ulcers of the stomach and duodenum, that led to GIB in patients died of myocardial infarction or aortic aneurysm dissection, are revealed in 21% of the cases. Among mortality causes at ambulance therapeutic hospital patients GIB frequency at acute diseases of the heart and aorta is 8 %. The key factors, leading to GIB at patients with IHD, first of all - at the acute stage of myocar-dial infarction, include Helicobacter pylori infection and nonsteroid anti-inflammatory drugs-related gastropathy (NSAID-related gastropathy).
The risk of NSAID-related gastropathy is the highest among patients with peptic ulcer in the past history, over 65 years of age and taking corticosteroid drugs. Respiratory failure, coagulopathy, assisted pulmonary ventilation for more than 48 hs are independent factors of the highest risk of GIB at patients in critical state with no relation to the basic disease. Adequate antisecretory therapy allows to cope with at least three challenges: to stop active bleeding, to prevent its relapse and GIB in general. On the basis of results of evidence-based studies, proton pump inhibitors are recognized to be optimal by antisecretory activity, time of effect onset, absence of resistance, safety and simplicity of application at patients with GIB (grade of evidence А).
Conclusion. GIB bring essential impact to the pattern of mortality at patients with cardio-vascular pathology. Unique efficient strategy of their prophylaxis at high risk patients is prescription of proton pump inhibitors.
Key words: myocardial infarction, gastro-intestinal bleedings, prophylaxis, treatment.
Кровотечение является одним из частых осложнений причин летального исхода больных в современной клинике. По данным Московского городского центра патологоанато-мических исследований, кровотечения встречаются не менее чем в 8% аутопсий умерших в стационаре и не менее чем в 5% аутопсий при внебольничной летальности. Характерно, что при внебольничной летальности кровотечение более чем в половине случаев не диагностируется при жизни.
Более 80% летальных кровотечений образуют кровотечения из желудочно-кишечного тракта (ЖКТ) и почти половина из них – кровотечения, не ассоциированные со злокачественными новообразованиями и осложнившие острые или хронические эрозивно-язвенные поражения слизистой оболочки верхних отделов ЖКТ: пищевода, желудка и двенадцатиперстной кишки(ДПК).
Известно, что в России пептической язвенной болезнью (ЯБ) страдает 8–10% населения, а желудочно-кишечное кровотечение (ЖКК), с некоторой поправкой на возможную его непептическую этиологию, развивается у 10–15% больных.
Причиной около 25% кровотечений из верхнего отдела ЖКТ являются острое эрозивно-язвенное поражение гастродуоденальной слизистой оболочки при критических состояниях, терапия нестероидными противовоспалительными препаратами (НПВП) или поражения гастродуоденальной слизистой оболочки коррозионными веществами.
При жизни редко диагностируются «стрессовые» острые повреждения слизистой оболочки желудка или ДПК у критически больных с обострением ишемической болезни сердца(ИБС).
В то же время установлено, что ЖКК у критически больных с обострением ИБС встречаются в 8–25% случаев и сопровождаются 50–80% летальностью.
В исследовании А.Л. Верткина и соавт. (2005) острые эрозии или язвы желудка и ДПК, приведшие к ЖКК у больных, умерших от острого инфаркта миокарда (ОИМ) или расслоения аневризмы аорты, были выявлены в 21% случаев (рис. 1).
Рис. 1. Смертельные гастродуоденальные осложнения острых ишемических заболеваний сердца и аорты в стационаре скорой медицинской помощи, % (2005)
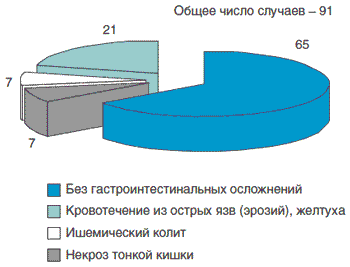
ЖКК возникли у 7% умерших больных с декомпенсацией сердечной недостаточности на фоне постинфарктного кардиосклероза и у 5% больных с ОИМ, у которых при аутопсии был выявлен рак.
Возраст больных с ЖКК на фоне обострения ИБС составил 76,0±7,7 года. Мужчин в выборке было 54%, женщин – 46%.
В структуре причин летального исхода у больных терапевтического профиля стационара скорой медицинской помощи (СМП) частота ЖКК при острых заболеваниях сердца и аорты составила 8% (рис. 2).
Рис. 2. Заболевания и смертельные осложнения - причины летального исхода в терапевтическом стационаре скорой медицинской помощи, % (2005)
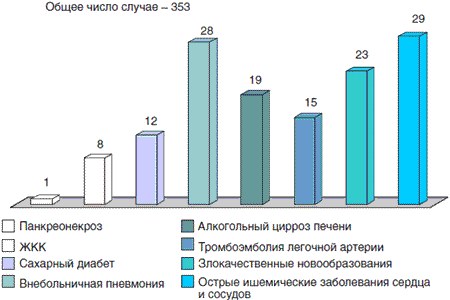
Характерно, что ЖКК у больных с острыми ишемическими заболеваниями сердца и аорты составили более 2/3 всех случаев кровотечений из верхнего отдела ЖКТ, приведших к летальному исходу больных терапевтического профиля в стационаре СМП (рис. 3).
Рис. 3. Этиология желудочно-кишечных кровотечений у больных терапевтического профиля в стационаре скорой медицинской помощи, % (2005)
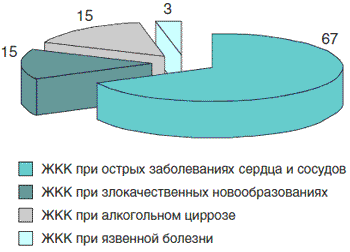
Обострение ИБС, в частности при ОИМ, особенно повторном, приводит к декомпенсации кровообращения в слизистой оболочке желудка и развитию острых язв или эрозий, приводящих к значительному ЖКК. Эта вторая причина высокой частоты кровотечений у пожилых пациентов (особенно с анамнезом пептической ЯБ и сахарным диабетом) на практике часто недооценивается.
Между тем в России в 2003–2004 гг. С.В. Колобовым и О.В. Зайратьянцем проведено фундаментальное исследование частоты и распространенности острых эрозивно-язвенных повреждений гастродуоденальной слизистой оболочки (ОПГС) у больных с ОИМ. По данным 3008 патологоанатомических вскрытий, оказалось, что острые эрозии и язвы желудка и ДПК встречаются у 10% больных, умерших от ОИМ. Частота эрозий составляет 48,7%, язв – 24%, петехиальных кровоизлияний – 20,4%. Более чем у 20% больных эти повреждения привели к ЖКК с развитием острой постгеморрагической анемии(ОПГА).
Реальную распространенность ОПГС у больных ОИМ определить практически невозможно, поскольку для этого требуется проведение эндоскопии всем пациентам отделений кардиореанимации. Поразительно, но и в отчетах аутопсии факту выявления ОПГС и ЖКК у больных, умерших от ОИМ, часто не придается значения возможной роли развившейся ОПГА в механизме смерти.
В известной степени частоту гастродуоденальных поражений при острых формах ИБС отражают результаты отечественного клинико-морфологического исследования, в котором ОПГС выявлены у 10% умерших от ОИМ. Среди умерших больных с ОПГС кровотечение развилось у каждого пятого больного с первичным ОИМ и у каждого второго – с повторным ОИМ и сахарным диабетом (Byron Cryer M.D., 2002).
Эпидемиологические и патогенетические особенности острых гастродуоденальных поражений при обострении ишемической болезни сердца
Механизм развития ОПГС при обострении ИБС в целом отражает известный патогенез «стрессового» поражения гастродуоденальной слизистой оболочки у критически больных, который практически не зависит от особенностей основного заболевания. Установлено, что ОПГС развивается в результате пептического (кислотного) повреждения слизистой оболочки на фоне глубокой ишемии с угнетением всех механизмов гастропротекции: секреции бикарбоната, муцина, пролиферации эпителия.
У части больных, особенно при длительной иммобилизации, развитию ОПГС может способствовать действие других факторов агрессии, таких как дуоденогастральный желчный рефлюкс и гастропарез. У больных, перенесших оперативное вмешательство, в развитии ОПГС также нельзя исключить влияние гипопротеинемии, анемии, резорбции эндотоксинов, а также последствий анестезии.
Тем не менее многие исследователи настаивают на необходимости рассматривать ОПГС как острое, ассоциированное с гиперацидностью, повреждение гастро-дуоденальной слизистой оболочки, при котором первичным этиологическим фактором является не гели-кобактерный гастрит, как при пептической язве, и не длительный прием НПВП, как при НПВП-гастропатии, а тяжелое заболевание.
Тяжелое заболевание приводит к гипотонии, ишемии гастродуоденальной слизистой оболочки, которая, в свою очередь, вызывает обратную диффузию Н+, ацидоз, истощение буферных систем, гибель клеток эпителия. В результате повреждается целостность слизистой оболочки (рис. 4, 5).
Рис. 4. Острая язва желудка у больного острым инфарктом миокарда
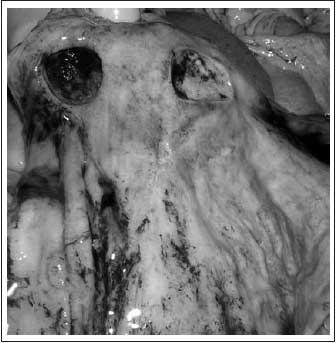
Рис. 5. Микропрепарат: повторный инфаркт миокарда, острое желудочное кровотечение. Край острой язвы слизистой оболочки желудка: некроз на глубину всей слизистой оболочки до мышечного слоя, очаговые отложения солянокислого гематина. Окраска гематоксилином и эозином, ×200
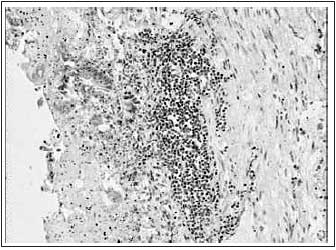
Тот факт, что механизм развития ОПГС при обострении ИБС является своеобразным, подтверждают несоответствия демографических данных пациентов с пептической ЯБ, среди которых преобладают мужчины относительно молодого возраста с анамнезом хронического рецидивирующего заболевания и симптомокомплексом «голодной боли», а также умерших от осложнений ЯБ, возраст которых превышает 60 лет.
Кроме того, неоднородность с клинической точки зрения статистической выборки пациентов с ЯБ, включающей всех когда-либо перенесших эрозивно-язвенное поражение желудка или ДПК, иллюстрируют выраженные половые различия больных при стратификации по возрасту. Как известно, именно женщины старше 60 лет, что совершенно нетипично для пептической ЯБ, являются основным контингентом больных, длительно принимающих НПВП и страдающих НПВП-гастропатией.
Интересной проблемой является взаимосвязь ОПГС и контаминации гастродуоденальной слизистой оболочки Helicobacter pylori. Известно, что инфицированность H. pylori пожилых больных вследствие «эффекта когорты» сегодня выше, чем у молодых. Существует предположение, что между геликобактериозом (как вялотекущей хронической инфекцией) и поражением коронарных сосудов существует фундаментальная этиопатогенетическая связь в аспекте «инфекционной» теории атеросклероза. В пользу этой гипотезы свидетельствуют результаты ряда исследований, в которых:
- у умерших от ОИМ в возрасте 40–59 лет, болевших ЯБ, обструкция левой коронарной артерии встречалось в 5 раз чаще, чем у не болевших ЯБ (Sternby N., 1976);
- окклюзии магистральных артерий нижних конечностей при ЯБ встречаются чаще, чем при других заболеваниях: 18% против 3,3% соответственно (Raso A.M. et al., 1985);
- при ИБС антитела к H. pylori встречаются достоверно чаще, чем в контрольной по полу и возрасту группе (Mendall M.A. et al., 1994);
- больные ИБС и низким коэффициентом риска ее развития (2,8) оказались достоверно чаще инфицированы цитотоксичными штаммами H. pylori (62% против 40%, р<0,004); эта разница получена с учетом влияния значимых для геликобактериоза социально-демографических факторов (Pasceri V. et al., 1998);
- геликобактерный гастрит у больных с высокой экспрессией аллели гена В2, кодирующего синтез фибриногена, приводит к увеличению его концентрации в плазме в случае развития ОИМ (Zito F. et al., 1999);
- у больных ИБС, инфицированных H. pylori и С. pneumonia, через 6 мес после деконтаминации возбудителей достоверно и стойко уменьшается концентрация фибриногена (Torgano G. et al., 1999).
Существует также множество гипотез о механизмах влияния H. pylori на атерогенез и развитие ИБС:
- агрессивные штаммы H. pylori, поддерживающие активный гастрит, вероятно, стимулируют атерогенез через длительно циркулирующие медиаторы воспаления: цитокины, ФНО-α, С-реактивный белок;
- активный геликобактерный гастрит является источником сенсибилизации циркулирующих лимфоцитов к эндотелию и атеросклеротическим бляшкам сосудов;
- геликобактерный гастрит приводит к уменьшению всасывания кобаламина и сопутствующей гипергомоцистеинемии, потенцирующей развитие ИБС.
По данным литературы, инфицированность критически больных H. pylori в странах Европы превышает среднюю для соответствующего возраста, составляет 38–67% и не зависит от возраста, основного заболевания, тяжести болезни и влияния факторов риска возникновения ЖКК.
Между тем в масштабном исследовании M.S. Robertson, J.F. Cade, R.L. Clancy уровень антител у критически больных коррелировал исключительно с длительностью пребывания в отделении интенсивной терапии. В связи с этим авторы не считают, что больным целесообразно проводить эрадикационное лечение в условиях реанимации, как этого требуют стандарты лечения больных, перенесших ЖКК другой этиологии.
Таким образом, с эволюционной точки зрения геликобактериоз, возможно, является дополнительным фактором риска развития атеросклероза и ИБС. Однако с клинической точки зрения существенно, что геликобактериоз играет основную роль в развитии пептической ЯБ. Как важнейший этиологический фактор атрофии слизистой оболочки желудка он резко увеличивает риск развития острых язв или эрозий с ЖКК у больных ОИМ. Так, наиболее часто встречающаяся атрофия слизистой оболочки антрального отдела желудка увеличивает риск образования дуоденальной язвы более чем в 10 раз.
Важнейшая роль НПВП-гастропатии, в частности на фоне длительного приема препаратов ацетилсалициловой кислоты (АСК), в генезе ОПГС у больных с обострением ИБС также не может игнорироваться. Согласно последним исследованиям длительный прием низких (до 100 мг/сут) доз АСК в 2–3 раза увеличивает риск развития ЖКК.
Установлено, что даже доза, равная 10 мг АСК в день, при длительном назначении способна привести к изъязвлению слизистой оболочки желудка. По выражению B. Cryer (2002), вероятно, нет такой дозы аспирина, которая бы обладала антитромботическим эффектом и не была гастротоксичной.
Таким образом, уменьшение резистентности гастродуоденальной слизистой оболочки на фоне терапии АСК потенциально угрожает любому пациенту с ИБС. Однако наиболее высоким является риск возникновения ЖКК у больных с установленными в известном исследовании ARAMIS (Fries J.T., 1997) факторами риска развития НПВП-гастропатии.
Отдельного внимания требует более высокий риск ЖКК у больных с обострением ИБС, получавших на амбулаторном этапе варфарин.
Основные факторы риска развития НПВП-гастропатии (ARAMIS, по J.T.Fries, 1997):
- ЯБ в анамнезе;
- возраст старше 65 лет;
- сопутствующий прием кортикостероидов.
Как уже говорилось, результаты ряда исследований, в которых показана более высокая частота развития тяжелых ОПГС у пациентов с ОИМ на фоне постинфарктного кардиосклероза, сахарного диабета, плохо контролируемой артериальной гипертонии, требует создания алгоритма рассмотрения значимости фоновых болезней и влияния других факторов коморбидности в аспекте анализа предикторов ЖКК при обострении ИБС.
Так, при ретроспективном изучении результатов аутопсий 3008 умерших от ОИМ установлено, что ОПГС с ЖКК чаще развивается у пожилых больных с повторным ОИМ, артериальной гипертензией и сахарным диабетом. Согласно данным литературы, риск кровотечения существенно увеличивается у пожилых женщин и в случаях, когда больной уже переносил ЖКК, а также имеет сердечную недостаточность, анемию или уремию.
В заключение описания эпидемиологических особенностей ОПГС при обострении ИБС не будет преувеличением утверждать, что в России осложненная кровотечением и приводящая к летальному исходу ЯБ, по сути, является заболеванием пожилых людей:
- пожилые больные имеют высокую степень инфицированности H. pylori;
- у значительной части пожилых пациентов имеется атрофия слизистой оболочки желудка;
- высокая частота полипатии и полиорганной недостаточности;
- у пожилых больных ИБС часто имеются плохо контролируемые артериальная гипертензия и сахарный диабет;
- у большинства пожилых суммируется влияние факторов ульцерогенности: возрастной инволюции, НПВП-гастропатии, химического рефлюкс-гастрита, атрофии слизистой оболочки вследствие геликобактериоза, ишемических расстройств.
Таким образом, на практике выявление симптомов ЯБ, кислой диспепсии или эрозивно-язвенного поражения желудка и ДПК в пожилом возрасте должно приводить к определенному клинико-диагностическому поиску и рассматриваться как предиктор высокого риска ЖКК.
Особенности клинической картины
ЖКК при ОГПС носит характер паренхиматозного. Часто развивается на 2–5-е сутки после госпитализации больного в отделение интенсивной терапии и начинается бессимптомно. По данным А.Ф. Логинова и соавт. (1998), у 52% больных с обострением ИБС кровотечение становится первым проявлением поражения ЖКТ, которое у 68% развивается в течение 10 дней от начала ОИМ или после аортокоронарного шунтирования.
Большинство исследователей согласно с тем, что ЖКК у критически больных происходят гораздо чаще, чем выявляются. Однако поскольку в большинстве случаев они протекают субклинически, не приводят к существенным гемодинамическим нарушениям, то и не являются актуальной клинической проблемой.
В связи с этим значительная часть исследователей считает, что клиническое значение ОПГС не стоит преувеличивать. Этому мнению оппонируют данные С.В. Колобова и соавт. (2002), согласно которым у больных ОИМ состоявшееся ЖКК в 30% случаев приводит к острой постгеморрагической анемии, что, как известно, в 1,5 раза увеличивает риск наступления госпитальной смерти и в 4 раза – повторного массивного ЖКК.
В свою очередь, ЖКК вдвое увеличивает риск летального исхода (RR= 1–4) и удлиняет сроки лечения в отделении интенсивной терапии в среднем на 4–8 дней.
Не связанными между собой факторами наиболее высокого риска ЖКК у критически больных вне зависимости от основного заболевания являются дыхательная недостаточность, коагулопатия, искусственная вентиляция легких более 48 ч.
Лечение и профилактика желудочно-кишечного кровотечения при остром поражении гастродуоденальной слизистой оболочки на фоне обострения ишемической болезни сердца
Установлено, что антисекреторная терапия, позволяющая увеличить рН содержимого желудка до 5–7, в период активного влияния факторов риска снижает вероятность возникновения ЖКК у критически больных как минимум на 50% и позволяет инициировать активную эпителизацию ОПГС. Благодаря адекватной антисекреторной терапии решаются как минимум три задачи:
- прекращение активного кровотечения;
- предотвращение рецидива кровотечения;
- предотвращение ЖКК в принципе.
Возможность антисекреторной терапии влиять на объем активного кровотечения и предотвращать его рецидивы основана на способности устойчиво сдвигать рН содержимого желудка в щелочную сторону. В результате блокируется лизис свежих тромбов и таким образом обеспечивается полноценный сосудисто-тромбоцитарный гемостаз.
Другой механизм действия представляется особенно важным для пациентов с обострением ИБС, страдающих от нарастающего снижения сократительной способности миокарда, гипотонии и длительной ишемии гастродуоденальной слизистой оболочки. Данный механизм заключается в прекращении при условии раннего назначения антисекреторной терапии влияния длительной пептической агрессии на слизистую оболочку желудка и ДПК.
Доказательства необходимости как можно более раннего назначения адекватной антисекреторной терапии получены в упомянутом уникальном клинико-морфологическом исследовании С.В. Колобова и соавт. При иммуноморфологическом исследовании авторы обнаружили, что у пациентов с ОИМ имеются тяжелые нарушения микроциркуляции и угнетение пролиферации эпителия слизистой оболочки желудка и ДПК, при этом продукция соляной кислоты не снижается.
Внутривенное капельное введение 40 мг омепразола уже в первые сутки значительно повышает пролиферативную активность эпителиоцитов и активную репаративную регенерацию слизистой оболочки, темпы которой практически не зависят от тяжести текущего ОИМ.
Теоретически нейтрализации содержимого желудка можно добиться введением любых антацидов или антисекреторных препаратов: гидроокисей магния и алюминия, сукральфата, антагонистов Н2-рецепторов к гистамину (АН2-Р), ингибиторов протонной помпы (ИПП).
Однако на базе результатов доказательных исследований оптимальными по антисекреторной активности, быстроте развития эффекта, отсутствию толерантности, безопасности и простоте применения у больных с ЖКК признаны ИПП (уровень доказательности А).
ИПП также являются более эффективными, чем АН2-Р, при назначении для профилактики рецидива кровотечения в стационаре. Так, для достижения рН > 6 в течение 24 ч необходимо внутривенно болюсно ввести 80 мг омепразола, далее – внутривенно капельно каждый час по 8 мг. Оказалось также, что pH > 5,5 у критически больных, даже находящихся на искусственной вентиляции легких, можно достичь введением внутрь суспензии омепразола из расчета 40 мг/сут.
В отделениях интенсивной терапии и кардиореанимации только 10% больных с обострением ИБС получают антисекреторную терапию ранитидином. ИПП чаще не назначают.
Необходимость широкого профилактического назначения антисекреторных препаратов критически больным пациентам нередко оспаривается на том основании, что потенциально летальные кровотечения развиваются не более чем у 5–8% больных. Ощелачивание желудка у всех пациентов, во-первых, стимулирует рост грамотрицательной микрофлоры в ЖКТ и увеличивает частоту нозокомиальной пневмонии, во-вторых, обусловливает существенную экономическую нагрузку. В связи с этим некоторые авторы предлагают априори назначать стандартную антисекреторнную терапию только больным, находящимся на искусственном дыхании и имеющим коагулопатию.
Однако в новейших исследованиях показано, что увеличение риска возникновения нозокомиальной пневмонии на фоне антисекреторной терапии происходит именно у больных на аппаратном дыхании. В то же время у пациентов нехирургического профиля этот риск не превышает общего для стационаров и не может служить аргументом для отказа от широкой фармакологической профилактики ЖКК с летальностью, превышающей 50%.
Решению проблемы лечения и профилактики острых эрозивно-язвенных поражений при обострении ИБС прежде всего препятствует отсутствие в практике неотложной кардиологии методики выявления и формирования групп риска развития ЖКК.
Согласно опыту систем первичной медицинской помощи в США и странах Европы этот процесс сопряжен с большими трудностями субъективного характера. По данным N.P. Lam и соавт. (1999), врачи общей практики, хирурги и анестезиологи только в общих чертах представляют проблему ОПГС и в 50% случаев не владеют навыками выполнения современных рекомендаций по проведению антисекреторной терапии.
У больных с острым коронарным синдромом, особенно у пожилых пациентов, риск возникновения ЖКК часто переоценивают и отказываются от проведения тромболизиса и гепаринотерапии даже при относительных противопоказаниях. Около 10% больным после ОИМ не назначают АСК, мотивируя это такими относительными противопоказаниями, как перенесенное ЖКК во время ОИМ или пептическая язва в анамнезе. Однако известно, что у не получавших АСК летальность в течение года после инфаркта миокарда была в 2 раза больше, чем у получавших.
Проблема предотвращения ЖКК у больных, которым необходима терапия антиагрегантами показалась решенной с появлением клопидогреля, эффективность которого в профилактике коронарного тромбоза оказалась сравнима с длительной терапией АСК. Рекомендации по назначению 75 мг/сут клопидогреля тем пациентам, которые не могут принимать низкие дозы АСК, были включены в национальные стандарты США.
Эти рекомендации и сегодня все еще существуют, несмотря на новейшие исследования F.K.L. Chan и соавт. (2005), убедительно показавших, что при высоком риске возникновения ЖКК длительная терапия низкими дозами АСК и 20 мг/сут эзомепразола значительно реже сопровождается кровотечением, чем длительная терапия клопидогрелем.
С объективной точки зрения внедрение в практику протокола эффективной антисекреторной терапии больных ОИМ не требует вложения дополнительных сил и средств, поскольку доказательная база применения ИПП и препараты этого ряда являются общедоступными.
Единственная эффективная стратегия реальной профилактики поражения гастродуоденальной слизистой оболочки – назначение антисекреторных препаратов (ИПП – омеза) тем больным и в тех клинических ситуациях, когда высок риск развития НПВП-гастропатии и (или) ЖКК.
| Январь 2011 г. |