Особенности и преимущества препарата Ксеплион
Палиперидона пальмитат
Обзор препарата1
- Действующее вещество: палиперидон
- Химико-физическая структура: пальмитат (сложный эфир пальмитиновой кислоты) палиперидона. Практически нерастворим в воде, растворимость достигается за счет патентованной технологии нанокристаллов (Nanocrystal®)
- Форма: водная суспензия для внутримышечного ведения пролонгированного действия.
- Хранение: при комнатной температуре в виде готовой суспензии.
- Механизм действия: антагонист D2 и серотониновых 5-HT2A рецепторов, антагонист α1- и α2- адренергических и H1-гистаминергических рецепторов. Отсутствие блокады холинергических, мускариновых, β1- и β2-адренергических рецепторов (способствует хорошей переносимости).
- Метаболизм: выводится преимущественно почками (80% выводится с мочой), слабо метаболизируется печенью (отсутствие клинически значимых взаимодействий с препаратами, метаболизиуемыми CYP450), не требует коррекции дозы у пациентов с низкой или средней степенью печеночной недостаточности.1,2
Терапия
- Показания: лечение шизофрении и профилактика рецидивов шизофрении
- Назначение: назначается без перорального перекрытия при начале терапии (за счет особой схемы старта). Возможно введение в дельтовидную и ягодичную мышцы (поставляется с двумя иглами)
- Дозы: 25-150 мг-экв (или 39-234 мг).
Абсолютные дозы Эквивалетные дозы 39 мг 25 мг-экв 78 мг 50 мг-экв 117 мг 75 мг-экв 156 мг 100 мг-экв 234 мг 150 мг-экв
- Перед первой инъекцией пациентам, ранее не принимавшим рисперидон/палиперидон, нужно назначить 2 дозы перорального палиперидона или рисперидона для проверки переносимости
Дозирование
Инициация терапии
(нагрузочные дозы)3,4Поддерживающая терапия3,4 День 1 День 8 ± 2 Через месяц
± 7 днейЧерез месяц *Выбор иглы:
- Не требуется коррекции дозы для пожилых пациентов или людей с легкой или средней степенью печеночной недостаточности3,4
- Может потребоваться коррекция дозы у пациентов с почечной недостаточностью
- Не наблюдалось синдрома постинъекционного делирия/седации (PDSS) по данным 15 завершенных исследований на 3.164 пациентах (ок.115.000 инъекций)5
Вторая инъекция (в день 8) может быть сделана ранее или позже на два дня, а ежемесячная с допущением ±7 дней (удобно в повседневной практике) без клинически значимого изменения концентрации палиперидона в крови.
- Длинная: ягодичные инъекции или дельтоидные инъекции у пациентов весом ≥90 кг
- Короткая: дельтоидные инъекции у пациентов весом <90 кг
Особые группы пациентов
- Почечная недостаточность:
- Умеренная (клиренс креатинина ≥50 мл/мин-<80 мл/мин):
- Начало терапии: день 1=100 мг-экв, день 8=75 мг-экв (дельтовидное)
- Поддерживающая терапия: 50 мг-экв (дельтовидное или ягодичное)
- Варьирование в диапазоне 25 - 100 мг-экв в зависимости от переносимости
- Более низкий клиренс креатинина: не рекомендовано
- Печеночная недостаточность:
- Легкая или умеренная: не требуется коррекции дозы
- Тяжелая: нет исследований
- Пожилые пациенты:
- Не требуется коррекции дозы (кроме случаев почечной недостаточности)
Техника проведения инъекций3,4,6
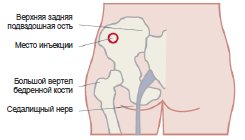
- Палиперидона пальмитат назначается в виде однократной в/м инъекции в дельтовидную или в верхний наружный квадрат ягодичной мышцы
- Упаковка содержит одноразовый, заполненный в заводских условиях шприц и две безопасные иглы (длинная и короткая)
- Набор хранят при комнатной температуре (25°C); разрешен диапазон температур от 15 до 30°C
- Шприц нужно энергично встряхивать 10 секунд для обеспечения гомогенности суспензии, до прикрепления иглы
- Следует использовать иглу с поправкой на вес тела, чтобы избежать введения палиперидона пальмитата в жировой слой дельтовидной мышцы
Эффективность
- Эффективен как для первого эпизода (редукция острой симптоматики 8,9), так и для пациентов со стажем заболевания и терапии (доказанное снижение числа/предотвращение рецидивов (PSY-3001)7)
- Нет необходимости в пероральном перекрытии при начале терапии10
- Эффективность и безопасность по сравнению с плацебо: доказаны в 4 краткосрочных7-10 и долгосрочном11,12 КИ 3 фазы (статистически достоверно более высокие баллы PANSS и более длительное время до прогрессирования заболевания)
- Эффективность и безопасность относительно Рисполепта Консты: сопоставимы (отсутствие преимущества) 13,14
- Улучшение личностного и социального функционирования по шкале PSP по сравнению с плацебо 8,9
Безопасность и переносимость
- Доказанная в клинических исследованиях долгосрочная безопасность и переносимость
- Сходная переносимость с Инвегой, Рисполептом Конста и плацебо во всем диапазоне рекомендуемых доз независимо от длительности терапии и вне связи с возрастом, полом, ИМТ пациента
- Самые частые НЯ: головокружение (2,5% vs 1% в группе плацебо), седация (2% vs 1%), головная боль, рвота, боль в месте инъекции (8% vs 4%), миалгия (1% vs 0%)
- Симптомы гиперпролактинемии выявлены у 1-3% пациентов, преимущественно у женщин
- Дозозависимое увеличение веса (средняя прибавка веса не более 2 кг в продленной открытой фазе лечения палиперидона пальмитатом)
- Риск ЭПС сходен при лечении палиперидона пальмитатом и назначении плацебо
- Не отмечалось увеличения интервала QT
- Низкая степень влияния на печень
Различия пролонгированных инъекционных рисперидона и палиперидона пальмитата
Рисполепт Конста Ксеплион Действующее вещество – рисперидон Действующее вещество – палиперидон Технология микросфер Технология нанокристаллов 1 раз в 2 недели 1 раз в 4 недели Для поддерживающей терапии Как для поддерживающей терапии, так и для купирования острых психозов Стартовая доза соответствует планируемой терапевтической Особый режим начала терапии Требуется сопутствующий прием пероральных препаратов в начале терапии Не требуется «перекрытие» Требует низкотемпературного режима хранения и разведения перед инъекцией Готовая суспензия с режимом хранения при комнатной температуре Соблюдение режима терапии Соблюдение режима терапии и социальное функционирование Сравнительные характеристики пролонгированных антипсихотиков и нейролептиков
Палиперидона пальмитат3 Рисперидон инъекционный пролонгированный15 Оланзапина памоат16 Галоперидола деканоат17 Форма Водная суспензия Водная суспензия с микросферами Водная суспензия Масляный растворитель Начало лечения Инъекции на 1-й и 8-й дни лечения; дополнительное «прикрытие» пероральными препаратами не требуется 21-дневный «перекрест» антипсихотиков при начале лечения и при каждом повышении дозы Различные стратегии насыщающих доз Различные стратегии насыщающих доз; не требуется прикрытия пероральными формами антипсихотиками Поддерживающая доза Поддерживающая терапия Каждые 2 недели Каждые 2 или 4 недели Обычно каждые 2-4 недели Путь введения Дельтовидная, ягодичная мышцы Ягодичная мышца Внутримышечно Ранжир доз (мг) 25, 50, 75, 100 и 150 мг экв 25, 37,5 и 50 мг 150, 210, 300 и 405 мг Широкий ряд (обычно 25-100 мг) Как поставляется Не требуется разведения – поставляется в предварительно заполненном шприце Требуется разведение, все дозы в 2 мл Требуется разведение Не требуется разведения Условия хранения Не требуется охлаждения. При температуре не выше 30°С. Охлаждение необходимо Не требуется охлаждения Постинъекционный контроль Не требуется5 Не требуется Да (1-3 часа) Нет Фармакокинетические параметры ряда антипсихотиков
Биодоступность (%) Связывание с белком (%) Период полужизни (час.) Время достижения стабильной концентрации (дни) Основные CYP энзимы, ответственные за биотрансформацию Клозапин 12–81 97 6–33 4–8 CYP1A2, CYP2C19 (CYP3A4, CYP2D6) Рисперидон 68 90 3–24 4–6 CYP2D6, CYP3A4 Палиперидон 28 74 23 4–5 N/A Оланзапин 60–80 93 20–70 5–7 CYP1A2, CYP2D6 Кветиапин 9 ± 4 83 5–8 2–3 CYP3A4 Зипразидон 60 >99 4–10 2–3 CYP3A4 Арипипразол 87 >99 48–68 14 CYP3A4, CYP2D6 Литература:
1. Инструкция по краткому применению препарата Инвега®
2. Vermeir et al. Drug Metab Dispos 2008;36:769–779
3. Инструкция по медицинскому применению препарата Ксеплион
4. Gopal et al. Curr Med Res Opin 2010;26:377–387
5. Alphs L. et al. Curr Drug Saf. 2011 Feb 1;6(1):43-5
6. Kozier et al. Fundamentals of nursing concepts, process and practice (5th ed); Menlo Park, CA: Addison Wesley Longman, Inc; 1998 p784–785;
7. Kramer et al. Int J Neuropsychopharmacol 2010;13:635–647;
8. Gopal et al. Int Clin Psychopharmacol 2010;25:247–56;
9. Nasrallah et al. Neuropsychopharmacology 2010;35:2072–2082;
10. Pandina et al. J Clin Psychopharmacol 2010;30:235–244;
11. Hough et al. Schizophr Res 2010;116:107–117;
12. Gopal et al. J Psychopharmacol. 2011 May;25(5):685-97;
13. Pandina et al. Prog Neuropsychopharmacol Biol Psychiatry 2011;35:218–226;
14. Li et al. Poster presented at CINP, June 6–10 2010, Hong Kong
15. Инструкция по медицинскому применению препарата Рисполепт Конста®
16. Di Lorenzo R., Brogli A.Neuropsychiatric Disease and Treatment 2010:6 573–58
17. Инструкция по медицинскому применению галоперидола деканоата
18. Adapted from Spina and Leon. Basic Clin Pharmacol Toxicol 2007;100:4–22 and individual products prescribing informationИнформация актуальна на 04.06.2012
| Август 2014 г. |