Опубликовано в журнале:
«Кардиология» №1, 2012г.Лечение ивабрадином пациентов со стабильной стенокардией и коморбидной хронической обструктивной болезнью легких
А.А.Хамаева, Ф.И.Белялов, Л.В.Керзина, О.В.Березовская, Е.Д.Паршукова, Г.Ю.Захарова
МСЧ ИАПО, Иркутский государственный институт усовершенствования врачей, Городская клиническая больница №3, Иркутск
Изучено влияние ивабрадина на толерантность к физическим нагрузкам и качество жизни у пациентов со стабильной стенокардией в сочетании с хронической обструктивной болезнью легких на фоне лечения β-адреноблокаторами. Показано, что применение ивабрадина в комбинации с β-адреноблокаторами у больных стабильной стенокардией и коморбидной хронической обструктивной болезнью легких эффективнее снижает частоту сердечных сокращений, увеличивает толерантность к физическим нагрузкам и ослабляет стенокардию, чем монотерапия β-адреноблокаторами, а у больных хронической обструктивной болезнью легких I и II стадии улучшаются показатели качества жизни, связанные со стенокардией. Добавление ивабрадина к лечению β-адреноблокаторами в течение 2 мес не усиливает обструкцию бронхов.
Ключевые слова: стенокардия, хроническая обструктивная болезнь легких, ивабрадин, качество жизни.
Efficacy of Ivabradine in Patients with Stable Angina and Comorbid Chronic Obstructive Pulmonary Disease
A.A. Khamaeva, F.I. Belyalov, L.V.Kerzina, O.V. Berezovskaya, E.D. Parshukova, G.Y.Zaharova
Irkutsk state Institute for medical Advanced studies, municipal hospital №3, RussiaWe investigated impact of ivabradine on exercise capacity and quality of life in patients with stable angina and comorbid chronic obstructive pulmonary disease during treatment with β-blockers. Ivabradine with β-blockers reduced heart rate, increased exercise capacity and improved angina more effective than β-blockers only. Quality of life associated with angina increased in patients with stage I and II chronic obstructive pulmonary disease. Addition of ivabradine to β-blockers for 2 month did not produce adverse respiratory effects.
Key words: stable angina, chronic obstructive pulmonary disease, ivabradine, quality of life.
Хроническая обструктивная болезнь легких (ХОБЛ) часто сочетается с ишемической болезнью сердца (ИБС). У госпитализированных пациентов с ИБС распространенность обструкции бронхов составила 34%, что почти в 2 раза выше, чем у лиц без коронарной болезни [1]. Среди пациентов с ХОБЛ у 34—36% имеется ИБС и в 2 раза повышены риск госпитализации и смертность от сердечно-сосудистых заболеваний [2—4].
Данные эпидемиологических исследований указывают на то, что одним из факторов риска развития сердечно-сосудистых заболеваний и предиктором сердечно-сосудистой и общей смертности является высокая частота сердечных сокращений (ЧСС), которая ассоциируется с увеличением потребности миокарда в кислороде [5—8].
Основной группой лекарственных средств, урежающих ЧСС при ИБС, являются β-адреноблокаторы. В то же время коморбидная ХОБЛ затрудняет применение этих препаратов. Кроме того, несмотря на приемлемую переносимость β-адреноблокаторов, добиться адекватного снижения ЧСС у больных стабильной стенокардией (СтСт) и коморбидной ХОБЛ не удается [9].
Целью настоящего исследования явилось изучение влияния ивабрадина на толерантность к физическим нагрузкам (ТФН) и качество жизни (КЖ) у пациентов со СтСт в сочетании с ХОБЛ на фоне лечения β-адреноблокаторов.
Материал и методы
Обследованы 146 человек, лечившихся в городской клинической больнице №3 Иркутска с диагнозом СтСт I—III функционального класса (ФК) — включая 120 (81%) мужчин и 26 (19%) женщин, средний возраст которых составил 60 лет (при 95% доверительном интервале — ДИ от 58,5 до 61,5 года). Диагноз устанавливали в соответствии с рекомендациями Всероссийского научного общества кардиологов (2008). У 79 (54%) пациентов была выявлена сопутствующая ХОБЛ, диагностированная в соответствии с критериями Global initiative for chronic Obstructive Lung Disease (2010), том числе I стадии — у 17%, II стадии — у 27,4% и III стадии — у 9,6%.
Дизайн исследования был одобрен Этическим комитетом Иркутского государственного медицинского университета.
Всем пациентам проводили общеклиническое обследование, регистрацию электрокардиограммы (ЭКГ) в 12 отведениях, эхокардиографию, холтеровское монито-рирование (ХМ) ЭКГ, велоэргометрию, спирометрию с бронходилатационным тестом. Был рассчитан индекс коморбидности Чарльсона. КЖ оценивали с помощью опросника качества жизни SF-36, Сиэтловского опросника стенокардии (SAQ) и респираторного опросника госпиталя Святого Георгия (SGRQ). Для оценки психического статуса применяли Госпитальный опросник тревоги и депрессии HADS.
У всех пациентов, включенных в исследование, имелись артериальная гипертония II—III степени и хроническая сердечная недостаточность (ХСН) I—II ФК. Одновременно с анамнестическими и клиническими данными учитывали медикаментозную терапию заболевания сердца (антиагреганты, статины, антагонисты кальция, нитраты, диуретики, ингибиторы ангиотензинпревращающего фермента) и ХОБЛ (ингаляционные β-агонисты, холинолитики, глюкокортикостероиды).
Статистическую обработку данных проводили с помощью программы Statistica 7.0. Для представления данных использовали методы описательной статистики, а нормальность распределения оценивали по критерию Шапиро—Уилка. Для сравнительного анализа групп применяли непараметрические критерии (Манна—Уитни, Краскела—Уоллиса, Вилкоксона), различия частот оценивали с помощью таблицы 2×2, для оценки взаимосвязей использовали коэффициент корреляции Спирмена.
Из группы больных СтСт в сочетании с ХОБЛ были выделены пациенты с ЧСС более 60 уд/мин. Эти больные методом случайных чисел были рандомизированы на 2 группы лечения по 30 человек (табл. 1). Сформированные группы были сопоставимы по полу, возрасту, длительности СтСт и ХОБЛ, уровню артериального давления, исходной ЧСС, показателям функции внешнего дыхания. Критериями исключения были нарушения ритма сердца (фибрилляция предсердий, брадиаритмии), исходная ЧСС меньше 60 уд/мин, острый инфаркт миокарда, ХСН IV ФК, дыхательная недостаточность III степени, обострение и (или) декомпенсация других сопутствующих заболеваний. Таким образом, были сформированы 2 группы, сопоставимые по клиническим и лабораторным показателям и медикаментозному лечению (см. табл. 1; табл. 2).
Таблица 1.
Клиническая характеристика сравниваемых групп
Показатель 1-я группа (n=30) 2-я группа (n=30) p Мужчины 28(93,3%) 29 (96,7%) 0,82 Женщины 2 (6,7%) 1 (3,3%) 0,62 Возраст, годы* 63,0 (от 55,6 до 70,4) 61,8 (от 53,8 до 69,8) 0,52 ЧСС, уд/мин* 75,5 (от 71,4 до 79,6) 74,7 (от 70,4 до 79,0) 0,72 ИБС, годы* 7,0 (от 3,7 до 10,3) 9,6 (от 6,3 до 12,9) 0,29 ХОБЛ, годы* 7,4 (от 4,0 до 10,8) 6,1 (от 2,7 до 8,5) 0,71 СтСт I ФК 11 (36,7%) 10 (33,3%) 0,77 СтСт II ФК 9 (30%) 9 (30%) 1,0 СтСт III ФК 10 (33,3%) 11 (36,7%) 0,77 ХОБЛ, I стадия 9 (30%) 10 (33,3%) 0,85 ХОБЛ, II стадия 16 (53,3%) 15 (50%) 0,85 ХОБЛ, III стадия 5 (16,7%) 5 (16,7%) 1,0 ХСН, ФК I 2 (6,7%) 3 (10%) 0,68 ХСН, ФК II 20 (67%) 20 (67%) 1,0 ХСН, ФК III 8 (26,7%) 7 (23,3%) 0,81 Индекс коморбидности Чарльсона, баллы* 4,3 (от 3,7 до 4,9) 4,2 (от 3,2 до 5,2) 0,36
Примечание. * — данные представлены в виде среднего и 95% доверительного интервала. ЧСС — частота сердечных сокращений; ИБС — ишемическая болезнь сердца; ХОБЛ — хроническая обструктивная болезнь легких; СтСт - стабильная стенокардия; ХСН — хроническая сердечная недостаточность; ФК — функциональный класс.Таблица 2.
Медикаментозная терапия в сравниваемых группах
Лекарственные препараты 1-я группа (n=30) 2-я группа (n=30) p Ацетилсалициловая кислота Статины
Антагонисты кальция
Нитраты
Диуретики
Ингибиторы ангиотензинпревращающего фермента
Ингаляционные β-агонисты
Ингаляционные холинолитики
Ингаляционные кортикостероиды
28 (93%) 11 (36,7%)
8 (26,7%)
14 (46,7%)
9 (30%)
17 (56,7%)
15 (50%)
15 (50%)
6 (20%)
29 (97%) 10 (33,3%)
9 (30%)
15 (50%)
9 (30%)
18 (60%)
17 (56,7%)
15 (50%)
5 (16,7%)
0,92 0,85
0,83
0,87
1,0
0,8
0,77
1,0
0,78
В дизайне исследования 1-я (основная) группа в целях более эффективного контроля ЧСС получала β-адреноблокатор бисопролол (конкор, Nycomed) в комбинации с ивабрадином (кораксан, Servier). Во 2-й (контрольной) группе продолжали лечение только β-адреноблокаторами. Дозу ивабрадина титровали от 10 до 15 мг/сут в течение 2—4 нед, причем начальная доза ивабрадина составляла 10 мг/сут. Одновременно во 2-й группе титровали дозу бисопролола от 2,5 до 10 мг/сут для достижения ЧСС 60 уд/мин.
На 2-м визите, который был предусмотрен через 2 нед, анализировали показатели гемодинамики, проводили спирографию, ХМ ЭКГ с целью определения среднесуточной, среднедневной и средненочной ЧСС, выявления различных нарушений ритма сердца, определения ТФН. Кроме того, оценивали КЖ пациентов с помощью опросников. В последующем были предусмотрены еще 2 визита — через 4 и 8 нед. На каждом визите определяли ЧСС, артериальное давление, безопасность и эффективность терапии при анализе дневника самоконтроля, изучали число приступов стенокардии и переносимость физических нагрузок. На 4-м визите вновь проводили ХМ, спирографию и оценку КЖ в динамике.
Результаты
Исходные ЧСС, ТФН и КЖ в сравниваемых группах больных не различались. Через 2 нед лечения выявлено снижение ЧСС на 3,9 и 3,4 уд/мин в 1-й и 2-й группах соответственно, но эти изменения были недостоверными (табл. 3). Такое снижение ЧСС не привело к изменениям частоты приступов стенокардии в обеих группах. Через 8 нед в 1-й группе выявлено достоверное снижение среднесуточной ЧСС на 4,6 уд/мин (p=0,009), дневной ЧСС на 4,0 уд/мин (p=0,009) и недостоверное снижение ночной ЧСС на 3,2 уд/мин (p=0,06). Во 2-й группе наблюдалось недостоверное снижение среднесуточной ЧСС на 1,7 уд/мин, дневной и ночной ЧСС на 0,8 и 0,4 уд/мин соответственно (см. табл. 3).
Таблица 3.
Динамика ЧСС при лечении ивабрадином
Показатель 1-я группа (n=30) 2-я группа (n=30) ЧСС, уд/мин (исходно)* 75,5 (от 71,4 до 79,6) 74,7 (от 70,5 до 79,0) ЧСС, уд/мин (через 2 нед)** 71,6 (от 66,9 до 76,3; p=0,18) 71,3 (от 67,6 до 75,0; p=0,45) ЧСС, уд/мин (через 8 нед)** 67,3 (от 63,8 до 70,2; p=0,009) 69,6 (от 65,7 до 73,5; p=0,12)
Примечание. * — ЧСС по ЭКГ покоя; ** — среднесуточная ЧСС по данным ХМ. Здесь и в табл. 4 данные представлены в виде среднего и 95 доверительного интервала. ЧСС — частота сердечных сокращений; ЭКГ — электрокардиограмма; ХМ — холтеровское мониторирование.По данным оценки частоты приступов стенокардии через 8 нед выявлено достоверное снижение числа приступов стенокардии в неделю в 1-й группе (p=0,005) и недостоверное во 2-й группе (p=0,3) (см. рисунок).
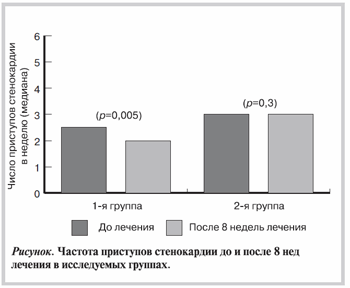
При изучении уровня переносимости физических нагрузок было обнаружено повышение ТФН в зависимости от стадии ХОБЛ. Так, в 1-й группе повышение ТФН выявлено у больных ХОБЛ I и II стадии (табл. 4).
Таблица 4.
Динамика ТФН по стадиям ХОБЛ
Группа Стадия ХОБЛ ТФН, Вт p исходно через 8 нед 1-я I—III 60,9 (от 54,8 до 67,0) 67,4 (от 61,5 до 73,3) 0,004 I 63,5 (от 48,8 до 78,2) 78,3 (от 66,5 до 90,1) 0,01 II 62,8 (от 55,6 до 70,0) 66,4 (от 59,9 до 72,9) 0,05 III 50,0 (от 35,5 до 64,5) 50,8 (от 45,6 до 56,0) 0,9 2-я I—III 63,0 (от 57,9 до 68,1) 65,1 (от 60,0 до 69,7) 0,02 I 62,9 (от 52,5 до 73,3) 64,1 (54,7 до 75,3) 0,59 II 64,2 (от 56,4 до 72,0) 67,7 (от 60,4 до 75,0) 0,06 III 58,8 (от 52,9 до 64,7) 59,0 (от 51,0 до 68,0) 0,9
Примечание. ТФН — толерантность к физической нагрузке; ХОБЛ — хроническая обструктивная болезнь сердца.Во 2-й группе достоверного повышения ТФН не выявлено, однако у больных ХОБЛ II стадии также отмечено увеличение ТФН. У больных ХОБЛ III стадии в обеих группах изменений уровня ТФН выявлено не было. Учитывая более высокую физическую активность больных ХОБЛ I и II стадии, можно предположить высокую значимость полученных результатов именно для этих пациентов.
При подсчете результатов по 5 шкалам Сиэтловского опросника стенокардии в 1-й группе выявлены достоверные изменения (улучшение) по шкале ограничения физических нагрузок (p=0,01), шкале стабильности приступов стенокардии (p=0,01) и шкале частоты приступов стенокардии (p=0,001). При разделении групп пациентов в зависимости от степени тяжести ХОБЛ в 1-й группе обнаружены изменения по шкале ограничения физических нагрузок у больных ХОБЛ I стадии (p=0,07) и II стадии (p=0,04). Однако у больных ХОБЛ III стадии изменения не выявлены. По шкалам стабильности приступов и частоты приступов также были выявлены достоверные изменения у больных ХОБЛ I и II стадии (p=0,04). Во 2-й группе у больных ХОБЛ I и II стадии также отмечалась положительная динамика по шкалам Сиэтловского опросника (ограничение физических нагрузок, стабильность приступов, частота приступов), но результат был статистически недостоверным. По шкалам удовлетворенности лечением и отношению к болезни в обеих группах за время наблюдения достоверных изменений не было (табл. 5).
Таблица 5.
Динамика качества жизни по Сиэтловскому опроснику
Группы Шкалы Сиэтловского опросника Оценка, баллы исходно через 8 нед p 1-я Шкала ограничений физических нагрузок (PL)
Шкала стабильности приступов (AS)
Шкала частоты приступов (AF)
Шкала удовлетворенности лечением (TS)
Шкала отношения к болезни (DP)50,0 (35—60)
50,0 (35—50)
60,0 (40—70)
60,0 (50—70)
45,0 (30—60)55, 0 (40—65)
50,0 (50—75)
70,0 (60—80)
60,0 (50—75)
43,0 (30—65)0,01
0,01
0,001
0,3
0,42-я Шкала ограничений физических нагрузок (PL)
Шкала стабильности приступов (AS)
Шкала частоты приступов (AF)
Шкала удовлетворенности лечением (TS)
Шкала отношения к болезни (DP)50,0 (40—60)
50,0 (45—50)
50,0 (50—70)
50,0 (50—70)
50,0 (45—50)50,0 (45—65)
50,0 (50—60)
55,0 (50—75)
50, 0 (50—75)
50,0 (45—55)0, 08
0,07
0,06
0,4
0,5
Примечание. Данные представлены в виде медианы и 25—75-го процентилей.Таким образом, можно предположить позитивное влияние ивабрадина на КЖ пациентов с сочетанием СтСт и ХОБЛ начальных стадий за счет снижения частоты приступов стенокардии и лучшей переносимости физических нагрузок. При анализе уровня тревоги и депрессии в динамике по шкале HADS достоверных изменений не было выявлено в обеих группах.
Добавление ивабрадина к лечению β-адрено-блокаторами в течение 2 мес не повлияло на показатели функции внешнего дыхания. При сравнении показатели объема форсированного выдоха за первую секунду (ОФВ1) до назначения и после лечения ивабрадином в течение 2 мес достоверно не различались. В 1-й группе ОФВ1 составил 68,3% (при 95% ДИ от 65,8 до 70,8) до лечения и 68,1% (при 95% ДИ от 65,7 до 70,5) после лечения ивабрадином, во 2-й группе — 66,3% (при 95% ДИ от 64,8 до 67,8) до лечения и 65,8 % (при 95% ДИ от 63,8 до 67,8) после него.
Полученные нами результаты не противоречат современным данным литературы. Ранее в исследованиях были показаны эффективность и безопасность применения ивабрадина в комбинации с β-адреноблокаторами у пациентов со СтСт и коморбидной ХОБЛ, продемонстрированы достоверное снижение ЧСС, уменьшение частоты приступов стенокардии, продолжительности безболевой ишемии миокарда и потребности в нитратах по сравнению с монотерапией β-адреноблокаторами [10—14]. В других исследованиях установлено, что применение ивабрадина в комбинации с β-адреноблокаторами повышало ТФН и улучшало КЖ у пациентов со СтСт в сочетании с ХОБЛ [15—17].
Несмотря на то что применение β-адреноблокаторов с ивабрадином сопровождалось достоверным снижением ЧСС и повышением ТФН, в обеих группах не было получено достоверных результатов по шкалам КЖ удовлетворенности лечением и отношению к болезни. Исходя из этого, можно предположить, что существуют другие факторы, влияющие на КЖ, у пациентов со СтСт и ХОБЛ. В нашем исследовании, несмотря на улучшение соматических показателей, не выявлено положительной динамики в психическом статусе больных; возможно, это и явилось причиной отсутствия изменений в КЖ пациентов.
Полученные результаты наводят на мысль о необходимости дальнейших исследований, изучения КЖ и особенностей больных стенокардией с коморбидной ХОБЛ с учетом как психических, так и соматических факторов и лечением соответствующих нарушений.
Выводы
1. Применение ивабрадина в комбинации с β-адрено-блокаторами у больных стабильной стенокардией с коморбидной хронической обструктивной болезнью легких эффективнее снижает частоту сердечных сокращений, увеличивает толерантность к физическим нагрузкам и ослабляют стенокардию, чем монотерапия β-адрeноблокаторами.
2. На фоне лечения ивабрадином в комбинации с β-адреноблокаторами у больных хронической обструктивной болезнью легких I и II стадии улучшаются показатели качества жизни, связанные со стенокардией.
3. Добавление ивабрадина к лечению β-адреноблокаторами в течение 2 мес не усилило бронхиальную обструкцию по данным оценки функции внешнего дыхания.Сведения об авторах:
Иркутская государственная медицинская академия последипломного образования
Кафедра гериатрии и геронтологии
Белялов Ф.И. - д.м.н., проф. кафедры.МСЧ ИАПО Иркутска
Отделение неотложной кардиологии
Хамаева А.А. - врач-кардиолог.ГКБ №3 г. Иркутска
Отделение функциональной диагностики
Керзина Л.В. - врач функциональной диагностики.
Березовская О.В. - врач функциональной диагностики.
Паршукова Е.Д. - врач функциональной диагностики.
Захарова Г.Ю. - врач функциональной диагностики.Литература
1. Soriano J.B., Rigo F., Guerrero D. et al. High prevalence of undiagnosed airflow limitation in patients with cardiovascular disease. Chest 2010;137:333—340.
2. Curkendall S.M., DeLuise C., Jones J.K. et al. Cardiovascular disease in patients with chronic obstructive pulmonary disease. Ann Epidemiol 2006;16:63—70.
3. Mapel D.W., Dedrick D., Davis K. et al. Trends and cardiovascular co—morbidities of COPD patients in the Veterans Administration Medical System, 1991—1999. J Chron Obstruct Pulmon Disease 2005;2:35—41.
4. Sidney S., Sorel M., Quesenberry C.P. et al. COPD and incident cardiovascular disease hospitalizations and mortality: Kaiser Permanente Medical Care Program. Chest 2005;128:2068—2075.
5. Liang M., Puri A., Devlin G. Heart Rate and Cardiovascular Disease: An Alternative to Beta Blockers. Cardiol Res Pract 2009;179:350.
6. Rosano G.M., Vitale C., Volterrani M. Heart rate in ischemic heart disease. The innovation of ivabradine: more than pure heart rate reduction. Adv Ther 2010;27:202—210.
7. Singh B.N. Morbidity and mortality in cardiovascular disorders: impact of reduce heart rate. J Cardivasc Pharmacol Ther 2001;6:313—331.
8. Шальнова С.А., Деев А.Д., Оганов Р.Г. и др. Частота пульса и смертность от сердечно-сосудистых заболеваний у российских мужчин и женщин. Результаты эпидемиологического исследования. Кардиология 2005;10:45—50.
9. Salpeter S., Ormiston T., Salpeter E. Cardioselective beta-blockers for chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2005;19:CD003566.
10. Aalbers J. Comparison of ivabradine plus beta-blockers versus beta -blocker therapy only. Cardiovasc J Afr 2010;21:116.
11. Koester R., Kaehler J., Ebelt H. et al. Ivabradine in combination with beta-blocker therapy for the treatment of stable angina pectoris in every day clinical practice. Clin Res Cardiol 2010;99:665—672.
12. Агеев Ф.Т., Макарова Г.В. и др. Эффективность и безопасность комбинации β-адреноблокатора бисопролола и ингибитора If-каналов ивабрадина у больных со стабильной стенокардией и хронической обструктивной болезнью легких. Кардиология 2010;10:22—26.
13. Комлев А.Д., Кузяев А.И., Ласкин Г.М. и др. Влияние блокатора If-каналов ивабрадина на показатели функции внешнего дыхания у больных хронической обструктивной болезнью легких в период стабильного течения заболевания. Тер арх 2010;3:23—25.
14. Татарченко И.П., Позднякова Н.В., Бирюченко М.В. и др. Оценка клинической эффективности включения ивабрадина и небиволола в комплексную терапию больных ишемической болезнью сердца с дисфункцией левого желудочка. Тер арх 2008;9:40—45.
15. Sarullo F.M., Fazio G., Puccio D. et al. Impact of «Off-Label» Use of Ivabradine on Exercise Capacity, Gas Exchange, Functional Class, Quality of Life, and Neurohormonal Modulation in Patients With Ischemic Chronic Heart Failure. J Cardiovasc Pharmacol Ther 2010;15:349—355.
16. Steg P.G. New insights into coronary artery disease: role of ivabradine. Eur Heart J 2010;12:11—15.
17. Коломоец Н.М., Бакшеев В.И., Заpубина Е.Г. и др. Клиническая эффективность ивабpадина у пациентов с каpдиоpеспиpатоpной патологией. Клин мед 2008;5:44—54.
| Февраль 2014 г. |