Опубликовано в журнале:
«ИНФОРМАЦИОННЫЙ ЖУРНАЛ ПО АКУШЕРСТВУ И ГИНЕКОЛОГИИ»; № 4; 2006; стр. 12-16.Особенности контрацепции при гормонотерапии доброкачественных гиперплазии в женской репродуктивной системе
Новикова В. А.
Кафедра акушерства и гинекологии ФПК и ППС КГМУ, г. Краснодар.Доброкачественные гиперплазии женских половых органов (гиперпластические процессы эндометрия, миома матки, эндометриоз) - являются нефизиогенной пролиферацией тканей репродуктивных органов, как правило, обусловлены избыточной и длительной эстрогенной стимуляцией в условиях недостаточного влияния прогестерона, представляют сложный нейроэндокринный синдром, вызванный нарушением в системе гипоталамус -гипофиз - яичники - матка (1). Частота выявляемости генитального эндометриоза составляет 10% среди женщин репродуктивного и пременопаузального возраста. У женщин пременопаузального возраста частота диагностики миомы матки при аутопсии матки составляет 50%. Около 50% женщин в возрасте 40-50 лет страдают дисфункциональным маточными кровотечениями, при которых в 10-50% выявляется гиперплазия эндометрия (2). По мнению Л. М. Шабада, любая доброкачественная опухоль способна к озлокачествлению с различной степенью вероятности, и при наличии факторов риска по развитию рака эндометрия, тела матки вероятность возникновения данной патологии возрастает на 50%. В канцерогенезе (схема 1) прослеживается морфологическая многостадийность и необратимость прогрессии, в реализации которого лежат не только генетический, наследственный фактор, но и сила, длительность воздействия канцерогена. Точно определить момент начала действия канцерогена, мутации протоонкогена (инициацию канцерогенеза) или переход к собственно прогрессии процесса практически невозможно. Выявление патологии, потенциально предшествующей злокачественным процессам, в частности, гиперплазии эндометрия, миомы матки, эндометриоза представляется надежным гарантом снижения смертности от гинекологического рака. Например, существует два патогенетических варианта рака эндометрия (таблица 2). Развитию I варианта предшествуют гиперпластические изменения эндометрия, матки, сопутствуют метаболические расстройства (ожирение, сахарный диабет, гипертоническая болезнь). Онкологическая настороженность при диагностике доброкачественных гиперплазий женских репродуктивных органов, особенно у женщин позднего репродуктивного и перименопаузального периодов действительно позволяет снизить показатели смертности женщин от гинекологического рака, обоснованна и необходима (3).
Схема 1.
Многостадийность процесса канцерогенеза.Таблица 1.
Патогенетические варианты рака эндометрия
Признаки I вариант II вариант Менструальная функция Ановуляторные маточные кровотечения Не нарушена Детородная функция Снижена, нередко бесплодие Не нарушена Время наступления менопаузы После 50 лет До 50 лет Тип кольпоцитологической реакции в постменопаузе Эстрогенный Атрофический Состояние яичников Гиперплазия тека-ткани Фиброз II СПКЯ II Феминизирующие опухоли Фон эндометрия Гиперпластические процессы Атрофия Состояние миометрия Фибромиома, внутренний эндометриоз Без особенностей Ожирение Есть Нет Гиперлипидемия Есть Нет Сахарный диабет Есть Нет Гипертоническая болезнь Сочетается с ожирением и/ или с СД Нет, или не сочетается с ожирением и/ или с СД Т- система иммунитета Без изменений Иммунодепрессия Продолжительность симптомов Обычно длительная Обычно короткая Степень дифференцировки опухоли Высокая (чаще I—II степень) Снижена (чаще III IV степень) Глубина инвазии в миометрий Чаще поверхностная Чаще глубокая Потенциал к лимфогенному метастазированию Невысокий Высокий Чувствительность к прогестагенам Высокая Невысокая Первичномножественные опухоли Яичники, молочная железа, толстая кишка Не характерны Прогноз Благоприятный Сомнительный Схема 1.
Многостадийность процесса канцерогенеза.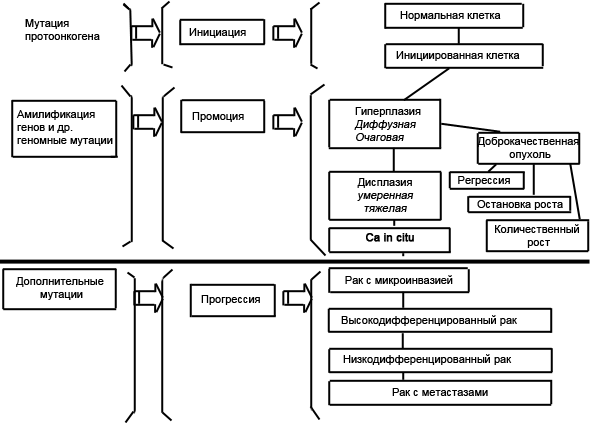
Факторами риска развития гинекологического рака являются:
Удлинение времени репродуктивного периода (раннее менархе и/или поздняя менопауза) Гиперпластические процессы эндометрия Ановуляторные кровотечения Нарушение менструальной и половой функции в анамнезе Сочетание гиперпластических процессов с ожирением и/или сахарным диабетом Бесплодие эндокринного генеза Олиго-овулятороные или аноовуляторные менструальные циклы (СПКЯ) Феминизирующие опухоли, стромальная гиперплазия, текоматоз, фолликулярные кисты с гиперплазией тека- и/или гранулезных клеток яичников Миома матки Операции по поводу заболеваний яичников Эстрогенный тип кольпоцитограммы в мено- и постменопаузе Заболевания печени, при которых нарушен метаболизм стероидных гормонов Хронические заболевания печени (> 10 лет) Длительный прием эстрогенов Отягощенная наследственность по онкозаболеваниям Семейная предрасположенность к онкозаболеваниям Нарушен метаболизм стероидных гормонов Хронические стрессовые ситуации Гипотиреоз Выраженная андрогенизация в менопаузе Нарушение липидного обмена Метаболический синдром Наличие воспалительно-дегенеративных изменений в эндометрии Основные принципы лечения доброкачественных гиперплазий органов женской репродуктивной системы следующие:
Коррекция эндокринопатии (нарушение функции щитовидной железы, гиперпролактинемии, гиперандрогении различного генеза и т. д.) и метаболических нарушений Ликвидация абсолютной гиперэстрогении. Восполнение дефицита гестагенов. Нормализация овуляции Формирование «искусственного » менструального цикла Создание временной медикаментозной аменореи Гормонотерапия не показана при: ГПЭ после удаления спирали; выявленной впервые ГПЭ у женщин репродуктивного возраста без нейро-обменно-эндокринных нарушений.
Гормонотерапия противопоказана при наличии такой патологии, как: злокачественные новообразования; узловые образования молочных желез; увеличение придатков матки неясного генеза; заболевания печени; тромбофлебит в стадии обострения; язвенная болезнь в стадии обострения; миома матки более 12 недель беременности.
Препараты для гормонотерапии доброкачественных гиперплазий органов женской репродуктивной системы.
Гестагены вызывают подавление овуляции, децидуальную трансформацию эндометрия, очагов эндометриоза, регресс вплоть до инволюции пролиферативных процессов в матке, молочных железах. Терапевтическая эффективность высокая (82%), что так же обусловлено значительно большей дозировкой препарата, чем в КОК. Длительность приема зависит от выраженности процесса: стартовое лечение может быть в непрерывном режиме в течение 3 месяцев, с последующим переходом на контрацептивный режим в течение 3 месяцев, затем рекомендовать во вторую фазу менструального цикла от 3 до 6 месяцев. Возможными побочными эффектами приема гестагенов являются диспепсические расстройства, мастодиния, «кровотечения прорыва», формирование инсулинорезистентности, влияние на атерогенный спектр крови, свертывающую систему.
Даназол является антагонистом гонадотропных гормонов, приводящим к блокированию овуляторного пика ЛГ и ФСГ, подавлению овуляции. Механизм воздействия даназола на репродуктивную регуляцию разнороден: 1) наличие андрогенных и прогестагенных свойств; 2) способность взаимодействовать с рецепторами половых гормонов; 3) нарушение гипоталамо-гипофизарно-яичниковых связей; 4) приводит к атрофии пролифератов и т. д. Считается, что прием даназола уже в первые 8 часов приводит к подавлению синтеза гонадотропных гормонов, выключению функции яичников, а значительная клиническая эффективность определяется уже через 2 недели. Рекомендуемый прием препарата: по 100 или 200 мг 2-3 раза в день от 3 до 6 месяцев, иногда до 12 мес.
Гестринон применяется в качестве эндокринотерапии пролиферативных процессов в женской репродуктивной системе благодаря своим андрогенным, прогестагенным, антипрогестагенным и антиэстрогенным свойствам. Считается, что он приводит не только к блокаде овуляторного выброса ЛГ, но и снижению базального уровня, следовательно - к снижению уровня эстрогенов, увеличению концентрации тестостерона в крови, аменорее в 50-100% случаев. Рекомендуемый прием препарата: по 1,25 - 5 мг 2 раза в неделю от 6 до 9 месяцев.
Агонисты Гн-РГ являются синтетическими аналогами гонадотропин-рилизинг-гормонов (Гн-РГ), вырабатываемого в области переднего медиобазального гипоталамуса, секретируемого в импульсном режиме каждые 90 мин. Механизм действия агонистов ГнРГ основан на обратимом длительном взаимодействии с рецепторами гипофиза, преходящим увеличением уровня ЛГ, ФСГ, эстрадиола в крови с максимумом через 4 ч после введения аналогов и постепенным снижением к 7-17 дням после введения. В дальнейшем происходит полное исчезновение рецепторов с поверхности гипофиза (down-регуляция), полная блокада секреции гонадотропинов, торможение секреции половых гормонов яичниками, обратимой аменорее ("медикаментозной псевдоменопаузе»). Препараты: золадекс (гозерелина ацетат), декапептил (Трипторелин), нафарелин, бусерелин. Способ введения: подкожный (ежедневно, депо-формы — 1 раз в 1 или 3 месяца), эндоназальные инсуффляции. Рекомендуемый прием препарата: золадекс, депо-форма, 3,6 мг, подкожное введение 1 раз в 28 дней; нафарелин, эндоназальный спрей, 00-800 мг/сут, 200 мг в каждой инсуффляции. Введение препарата следует начинать на 2-4-й дни менструального цикла, повторяя каждые 4 недели в течение 6 -12 месяцев, а 4-й неделе лечения у 60% женщин наступает аменорея, на -й неделе - у 100%.
Метод и продолжительность гормонотерапии зависит г только от морфологической верификации патологического процесса, но и от возраста пациентки, длительности и выраженности процесса, наличия экстрагенитальной патологии.
Сочетание доброкачественных гиперплазий органов женкой репродуктивной системы с инсулинорезистентностью требует особенного терапевтического подхода. Инсулинорезистентность генетически детерминирована, ген P450SCC обеспечивает аутосомно-доминантный тип наследования патологии. Синдром инсулинорезистентности в 1988 г. G. eaven был назван «синдромом X», именуемый в настоящее ремя и как метаболический синдром, который имеет свои признаки: абдоминально-висцеральное ожирение; инсулинорезистентность и гиперинсулинемия; дислипидемия (липидная триада); артериальная гипертония; нарушение толерантности к глюкозе/ сахарный диабет II; ранний атеросклероз/ :БС; нарушение гемостаза; гиперурикемия и подагра; микроальбуминурия; гиперандрогения.
При инсулинорезистентности гиперинсулинемия опосредованно через IGF I приводит к росту нескольких фолликулов, их персистенции, трансформации в кисты (поликистоз), гиперандрогении, гиперэстрогении; в избыточной жировой ткани происходит ароматизация андрогенов в эстрогены, гиперплазии эндометрия, миоматозным и аденомиозным изменениям миометрия; при гиперинсулинемии в печени подавляется продукция СССГ, что так же приводит к гиперэстрогении. Применение метформина по 500 мг 3 раза в сутки в течение 3-6 месяцев также благотворно влияет на нормализацию менструально-овариальной функции.
Однако ликвидация эндокринопатии, формирование двухфазного менструального цикла, полноценной лютеиновой фазы с/ без стимуляцией овуляции приводит к возрастанию возможности наступления беременности. Известно, что агонисты Гн-РГ, приводят к стимуляции аденогипофиза в первые 7-10 дней от начала лечения, что может проявляться кровомазанием, кровотечением «прорыва».
Риск возникновения нежелательной беременности при сексуальной активности даже для женщин старше 40 лет составляет 50% Согласно литературным данным незапланированная беременность наступает в 10% у женщин 40-44 лет, 2-3% у женщин 45-49 лет. У женщин с наступившей менопаузой в течение последующих 2-3 лет не исключена вероятность спонтанной овуляции и возникновения беременности.
Целью исследования явилась оценка частоты наступления беременности при гормонотерапии доброкачественных гиперплазий органов женской репродуктивной системы.
Ретроспективно обследовано 50 женщин в возрасте от 35 до 48 лет (41,5 0,16 лет), которым проводилось прерывание беременности, наступившей на фоне гормонального лечения доброкачественных гиперплазий органов репродуктивной системы женщины (миомы матки, эндометриоза, гиперпластических процессов эндометрия). Используемые препараты: золадекс (3,6 мг/ 4 нед), даназол (400-600 мг/сут в непрерывном режиме), гозерелин 2,5 мг 2 раза в неделю; медроксипрогестерона ацетат (МПА) 10-50 мг/сут с 16го по 25й дни цикла; дидрогестерон 20мг/сут с 16го по 25й дни цикла, 17-ОПК 12,5% 250 - 500 мг в/м на 14й и 21й дни цикла или на 14й, 17й и 21й дни цикла; терапия проводилась в течение 3-6 месяцев.
Диагностика беременности производилась на основании жалоб, данных ультразвукового исследования. Частота наступления беременности на фоне гормонотерапии, сроки выявления представлены в таблице 2.
Таблица 2.
Частота возникновения и сроки выявления беременности на фоне гормонального лечения доброкачественных гиперплазий органов репродуктивной системы
Золадекс 3 6 2 4 1 2 Даназол 2 4 0 0 2 4 Гестринон 2 4 0 0 2 4 МПА 6 12 2 4 4 8 Дидрогестерон 32 64 6 12 26 52 17-0П 5 10 0 0 5 10 Таблица 3.
Формы и режим применения Фарматекса
Форма выпуска Начало контрацептивного действия Длительность контрацептивного действия Характер увлажняющего действия Вагинальные суппозитории Через 5 минут после введения 4 часа, на 1 половой акт Умеренное увлажнение Вагинальная таблетка Через 10 минут после введения 3 часа, на 1 половой акт Не увлажняет Вагинальный крем Сразу после введения 10 часа, на 1 половой акт Обильное увлажнение Вагинальная капсула Через 10 минут после введения 4 часа, на 1 половой акт Умеренное увлажнение Вагинальный тампон Сразу после введения Несколько половых актов в течение 24 часов Нормализует увлажнение Жалобы: нагрубание молочных желез, тошнота, раздражительность, плаксивость, кровянистые выделения из половых путей, рвота, не связанная с приемом пищи, изменение аппетита, утомляемость, снижение памяти, сонливость, нарушение сна - расценивались и женщиной, и акушером-гинекологом как побочные эффекты гормонотерапии. Оценка эффективности гормонотерапии на состояние эндо-, миометрия при использовании ультразвукового метода исследования через 1 месяц гормонотерапии проводилась только у 10 (20%) женщин, где была заподозрена беременность малого срока, произведена вакуум-аспирация полости матки. У 40 (80%) беременность была диагностирована в сроке 7 0,05 недель, был произведен артифициальный аборт.
Осложнением артифициального аборта у обследованных женщин было: кровотечение в 16% случаев; reabrasio полости матки (остатки плодного яйца) - в 10%.
Наступившая нежелательная беременность, прерывание её нарушили лечебный алгоритм имеющейся патологии. Всем женщинам в последующий менструальный цикл повторно проводился весь комплекс диагностических мероприятий, уточняющих течение основной патологии (доброкачественной гиперплазии органов женской репродуктивной системы), что требовало дополнительных временных и материальных затрат.
Прерывание беременности у женщин на фоне гормонотерапии доброкачественных гиперплазий органов женской репродуктивной системы является грубым вмешательством в регуляцию гипоталамо-гипофизарно-яичниковой системы. Даже при отсутствии патологии гинекологического плана аборт может явиться серьезным экзаменом для адаптационно-регуляторных механизмов регуляции женской половой функции. Доброкачественные гиперплазии органов женской репродуктивной системы являются отражением органических нарушении в осуществлении этой регуляции. Поэтому прерывание беременности у данной когорты лиц, тем более на фоне гормонотерапии катастрофически усугубляет имеющиеся нарушения в реализации контроля за состоянием органов репродуктивной системы. Предупреждение нежелательной беременности на фоне гормонотерапии доброкачественных гиперплазий органов женской репродуктивной системы является залогом эффективности проводимого лечения, достижения поставленной цели.
Для профилактики наступления нежелательной беременности рекомендуется контрацепция: барьерная (презервативы Innotex); местная (Фарматекс). Фармакологические свойства Фарматекса обеспечиваются активным веществом препарата - Бензалкония хлоридом. Бензалкония хлорид является катионным веществом, изменяющим натяжение клеточной мембраны. При введении в во влагалище (в форме капсулы, таблетки, крема, свечи или тампона) покрывает слизистую влагалища, образуя на ней сплошную пленку. Достаточно нескольких секунд, чтобы сперматозоиды были иммобилизованы и разрушены путем отделения жгутиков от головок. Обладая спермицидным действием, бензалкония хлорид in vitro оказывает бактерицидное и вирусоцидное действие на возбудителей ЗППП и герпес, цитомегаловирус, ВИЧ. Не нарушает сапрофитную флору влагалища. Бензалкония хлорид не проникает в кровь, материнское молоко, оказывает исключительно местное воздействие, в том числе антисептическое. Индекс Перля для Фарматекса составляет 1,2.
На фоне гормонотерапии агонистами Гн-РГ и антагонистами гонадотропных гормонов у 100% женщин уже на 2-м месяце возникает сухость во влагалище, диспаренурия различной степени выраженности. Применение Фарматекса в виде вагинального крема, суппозиториев или капсул имеет особое значение для сексуально активных женщин, так как способствуют увлажнению стенок влагалища, нивелируют неприятные ощущения при половом акте, связанные с эстрогенодефицитом.
Таким образом, гормонотерапия доброкачественных гиперплазий органов женской репродуктивной системы не исключает возникновение спонтанной овуляции. Имеющийся риск возникновения беременности у женщин репродуктивного и пременопаузального периода увеличивается при коррекции эндокринопатии (нарушений функции щитовидной железы, гиперпролактинемии, гиперандрогении различного генеза и т. д.) и метаболических нарушений, ликвидации абсолютной гиперэстрогении, восполнении дефицита гестагенов, нормализации овуляции. Аборт, выполненный у женщин с нарушениями регуляции репродуктивной функции, имеет более пагубные последствия, так как усугубляет имеющиеся нарушения. Информирование женщины о риске наступления нежелательной беременности, динамический ультразвуковой контроль состояния эндометрия, применение барьерной (презервативы Innotex) и местной спермицидной контрацепции (Фарматекс) на фоне гормонотерапии доброкачественных гиперплазий органов женской репродуктивной системы является залогом успешного лечения, реализации поставленных терапевтических задач, улучшения качества жизни женщины.
Литература
1. Рациональная фармакотерапия в акушерстве и гинекологии. Том IX. Под ред. В. И. Кулакова, В. Н. Серова.- М.: Литтерра, 2005 - С. 581-586; 609-614
2. Роузвиа Сильвия К. Гинекология (под ред. Э. К. Айламазяна). М.: МЕДпресс-информ, 2004
3. Серов В. Н., Прилепская В. Н., Овсянникова Т. В. -Гинекологическая эндокринология. — М.: МЕДпресс-информ, 2004. - С. 7-96; 182-207; 321-334; 381-508.
| Сентябрь 2010 г. |