Выбор. . Только теперь. |
Последующая информация предназначена только для медицинских работников!
Выбрав ссылку "Продолжить", Вы подтверждаете, что являетесь специалистом в области здравоохранения.
Опубликовано в журнале:
«ВЕСТНИК Санкт-Петербургской государственной академии им. И. И. Мечникова», 2006, №1, С. 7-14Результаты лечения больных хроническим вирусным гепатитом В в течение 12 месяцев (многоцентровое исследование)
Т. В. Сологуб, И. П. Баранова, А. А. Шульдяков, М. X. Турьянов
Санкт-Петербургская медицинская академия имени И. И. Мечникова,
Пензенский институт усовершенствования врачей,
Саратовский медицинский институт,
Медицинская академия последипломного образования, г. МоскваВведение
Вирусный гепатит В (ВГВ) — одна из важнейших медико-социальных проблем современности, так как в мире ежегодно погибает около 2 млн человек с разными формами ВГВ инфекции, из них около 100 тысяч от фульминантных форм ВГВ, еще полмиллиона — от острой инфекции, около 700 тысяч — от цирроза печени и 300 тыс. — от гепатоцеллюлярной карциномы. За 15-20 лет от ВГВ в мире гибнет больше людей, чем за всю Вторую мировую войну [1-2]. В последние 3 года заболеваемость ВГВ в России составляет 18,1-21,9 случая на 100 тыс. населения. В настоящее время среди заболевших преобладают молодые люди и подростки, в отличие от 70-80-х годов, когда 80% заболевших составляли лица старше 40-50 лет.
Наибольшие успехи в лечении хронического вирусного гепатита В (ХВГВ) получены при проведении интерферонотерапии. Применяются различные препараты рекомбинантного интерферона-альфа (ИФН-а) [4]. К сожалению, стабильных положительных результатов удается достичь не более чем у 30-35% больных ХВГВ. [5, 6]. В то же время, при парентеральном применении интерферонов нередко возникают побочные эффекты [7, 8].
Новые возможности в лечении больных ХВГВ появились при использовании интерфероногенов. Это вещества природного или синтетического происхождения, способные индуцировать в организме человека продукцию эндогенного ИФН, обладающего преимуществами перед экзогенным ИФН. Наиболее изученным индуктором ИФН является акридонуксусная кислота (циклоферон). При введении циклоферона вырабатывается ИФН, не обладающий антигенностью, а регуляторные механизмы синтеза защищают организм от перенасыщения интерферонами. Однократное введение циклоферона обеспечивает относительно длительную циркуляцию эндогенного ИФН [9-11].
К препаратам выбора при лечении ВГВ-инфекции относится и ламивудин (зеффикс, эпивир). Он оказывает мощное подавляющее действие на репликацию ВГВ, ингибируя альфа-, бета- и гамма-ДНК-полимеразы, нарушает сборку частиц вириона [12]. Однако, по данным ряда авторов, нередко отмечается рецидив репликации вируса после прекращения терапии ламивудином, что может сочетаться с резким подъемом уровня АЛТ [13, 14]. Длительное лечение ламивудином провоцирует развитие устойчивости вируса из-за появления YMDD мутантных форм, что, как правило, сопровождается возобновлением репликации вируса и повышением АЛТ, несмотря на продолжающееся лечение [15, 16]. Одним из вариантов оптимизации терапии ХВГВ является комбинация препарата ИФН-а, в том числе пегилированной формы, с ламивудином [17]. Данная комбинация повышает эффективность терапии ХВГВ и снижает образование мутантных штаммов [18,19]. Хотя существует мнение о неэффективности комбинации интерферона с ламивудином, интерферон используется для терапии пациентов с ламивудин-резистентными штаммами вируса ХВГВ [20, 21]. Среди новых подходов к терапии ХВГВ — назначение комбинации индуктора интерферона и ламивудина.
Цель исследования
Целью исследования, результаты которого приведены в данной статье, была оценка эффективности различных схем противовирусной терапии больных ХВГВ (монотерапия циклофероном или ламивудином и комбинированная — циклоферон+ламивудин).
Материалы и методы исследования
В исследование, проведенное в Государственной медицинской академии им. И. И. Мечникова, Институте усовершенствования врачей (Пенза), Саратовском медицинском институте, было включено 300 пациентов кавказской расы, разделенных на три группы. Первая (n=100) получала монотерапию циклофероном. Вторая группа (n=100) — монотерапию ламивудином. Третья группа (n=100) комбинированную терапию циклофероном и ламивудином.
В программу исследования включались пациенты, соответствующие следующим критериям: больные (мужчины/женщины) в возрасте 20-40 лет (табл. 1) с впервые установленным диагнозом хронического гепатита В в фазе репликации (ДНК ВГВ+), длительностью заболевания ХВГВ менее 5 лет и уровнем АЛТ, превышающим норму в 1,5-8 раз.
Таблица 1. Распределение больных ХВГВ по возрасту
Возраст Число больных % соотношение 20-30 лет 187 62,3% 30-40 лет 113 37,6% Таблетки циклоферона применяли 1 раз в сутки, 3 раза в неделю (понедельник, среда, пятница) из расчета 10-15 мг/кг массы тела (4-6 таблеток на прием). Длительность курса 12 мес. Ламивудин применяли 1 раз в сутки, ежедневно, из расчета 3 мг/кг массы тела, но не более 100 мг в сутки. Длительность курса 12 мес. При необходимости больные получали гепатопротекторы (карсил, лив-52, хофитол, гепабене, лохеин), спазмолитики (нош-па, никошпан), ферменты (мезим-форте, фестал, панкреатин, креон, панцитрат), при запорах — лактулозу.
Оценку эффективности применения циклоферона и ламивудина осуществляли в 5 точках: через 1, 3, 6, 12 месяцев от начала терапии и через 6 месяцев после окончания лечения. Основным критерием было отсутствие в сыворотке крови ДНК ВГВ через 6 месяцев после завершения лечения.
Для интегральной оценки лечебной эффективности препарата была использована шкала качества жизни SF-36.
Результаты исследования были статистически обработаны с помощью пакета статистических программ Statgrancs. Различия считались достоверными при р<0,05 и 0,01.
Под наблюдением находилось 300 больных ХВГВ в возрасте от 20 до 40 лет (табл. 1)
Среди наблюдаемых пациентов преобладали молодые люди мужского пола (табл. 2), что соответствует эпидемиологической ситуации заболеваемости ХВГВ.
Таблица 2. Распределение больных ХВГВ по полу
Пол Число больных % соотношение Мужской 216 72% Женский 84 28% Таблица 3. Характеристика групп больных хроническим гепатитом В
Показатели 1-я группа 2-я группа 3-я группа Число больных 100 100 100 Мужской пол, в % 64,0 73,0 80,0 Возраст, лет 29,0 ±2,8 30,3 ±3,3 31,8±7,5 Диагноз ставился на основании клинико-эпидемиологических данных, результатов биохимических тестов с использованием рутинных методов определения в сыворотке АЛТ, ACT, билирубина с фракциями, протеинограммы, а также углубленных серологических обследований с выявлением HBsAg, HBeAg, HBcorAB, HBsAB, HBeAB методом ИФА, детекцией ДНК ВГВ методом ПЦР.
К началу терапии у всех больных был диагностирован ХВГВ с умеренной активностью трансаминаз (в 4,5-8 раз выше нормы) в фазе репликации (обнаружение HBeAg и ДНК ВГВ). Срок инфицирования не превышал 5 лет. У 132 чел. (44%) — до 1 года, у 60 чел. (20%) — от 1 года до 3 лет и у 108 (36%) —от 3 до 5 лет.
Ведущими синдромами у наблюдаемых больных были: диспептический в 40,0-43,0% случаев, астеновегетативный в 62,0-66,0% случаев, однако самым частым клиническим проявлением ХВГВ было увеличение печени (табл. 4). Лишь у части больных регистрировались «малые» печеночные знаки (телеангиэктазии, пальмарная эритема и др.), желтуха и увеличение селезенки отмечалось не всегда.
Таблица 4. Частота регистрации клинических симптомов у наблюдаемых больных
Симптомы 1-я группа 2-я группа 3-я группа Диспептический 43,0 40,0 42,0 Астеновегетативный 66,0 64,0 62,0 Гепатомегалия 87,0 88,0 86,0 Спленомегалия 28,0 24,0 20,0 Иктеричность кожи и склер 22,0 20,0 20,0 Среди лабораторных показателей (табл. 5) у всех больных регистрировалась гиперферментемия (уровень АЛТ и ACT превышал норму в 4,5-8 раз). У 36-42,0% больных отмечалась билирубинемия, его уровень не превышал норму более чем в 2 раза. У 11-13,0% больных наблюдалось повышение уровня билирубина за счет неконъюгированной фракции.
Таблица 5. Биохимические показатели крови у больных ХВГВ до начала терапии
Биохимические показатели 1-я группа 2-я группа 3-я группа АЛТ (норма до 55 ЕД/л) 182,8 ±3,0 191,0 ±4,9 188,4 ±5,0 ACT (норма до 59 ЕД/л) 124,0 ±2,9 122,7 ±6,3 120,9 ±2,8 Щелочная фосфатаза (норма до 430 ЕД/л) 741,2 ±4,9 842,6 ±5,1 813,4±4,2 Амилаза (норма до 220 ЕД/л) 204,0 ±2,5 212,0±11,7 211,6±4,9 Билирубин (норма до 21 мкмоль/л 36,4 ±7,9 34,0 ±12,2 39,6 ±3,8 Общий белок (норма до 60 г/л) 58,2 ±2,3 57,6 ±2,0 61,7 ±1,65 Альбумины (норма 50%) 52 ±1,5 51,3± 1,1 51,6 ±0,75 Гамма-глобулины (норма 15-20%) 26,06 ±0,9 25,04±0,7 26,7 ±0,45 Диспротеинемия с гипергаммаглобулинемией была невыраженной, до 25-26,7%, и отмечалась у 15-18% больных.
Результаты исследования
Субъективное улучшение (табл. 6) при проведении противовирусной терапии отметили практически все пациенты. Так, 29% больных, получавших ламивудин, и 45%, получавших циклоферон, сообщили о значительном улучшении самочувствия, но наиболее высоко субъективно оценили больные комбинированную терапию циклофероном и ламивудином — 59%.
Таблица 6. Субъективная оценка эффективности препаратов у больных ХВГВ
Препарат Эффективность лечения Слабая Умеренная Значительная Циклоферон 15% 40%* 45%* Ламивудин 10% 61%* 29%* Циклоферон + ламивудин 8% 33%* 59%*
* Значения, существенно (р<0,005) отличающиеся от групп сравнения.Использование любой схемы терапии сопровождалось положительными результатами: пациенты 1-й и 3-й групп отмечали более быстрое, чем у больных 2-й группы, повышение работоспособности и исчезновение слабости. У пациентов, получавших комбинированную противовирусную терапию, после лечения увеличение печени регистрировалось достоверно реже, лишь в 22%, а после монотерапии в 59 и 45% случаев соответственно.
Снижение уровня ферментов (АЛТ) до нормы регистрировалось не только у больных с комбинированной терапией, но и у получавших монотерапию циклофероном, нормализация в этих группах происходила достоверно быстрее в сравнении с монотерапией ламивудином (см. рисунок). Худшие биохимические результаты у больных, получавших ламивудин, по-видимому, связаны с отсутствием у этого препарата прямого противовоспалительного действия на ткань печени.
Динамика АЛТ у исследуемых больных в течение первых шести месяцев терапии
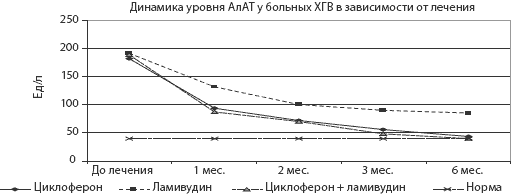
Первичная биохимическая ремиссия регистрировалась у 25% больных, получавших комбинированную терапию, и у 20% получавших монотерапию циклофероном, без статистически достоверной разницы между этими двумя группами.
Используемые препараты оказывали выраженное действие и на частоту наступления сероконверсии. Элиминация HBeAg и появление анти-НВе регистрировалось в разных группах от 33 до 54% — самое высокое у больных, получавших комбинированную терапию. Вирусологический ответ (снижение ДНК ВГВ до неопределяемых цифр) после курса циклоферона был чуть ниже применения ламивудина (33% против 44%).
Таблица 7. Эффективность терапии противовирусными препаратами больных хроническим гепатитом В
Ремиссия 1-я группа, % 2-я группа, % 3-я группа, % Первичная полная 5 8 11 Первичная биохимическая 20* 13 25* Отсутствие 8 11* 3 Рецидив 22 45* 7 Стабильная 33 44* 54*
Значения (р<0,005), отличающиеся от параметров групп сравнения.Нами зарегистрирован 1 случай элиминации HBsAg у больной, получавшей комбинированную терапию.
В целом препараты хорошо переносились и давали минимальные побочные эффекты. Нежелательные реакции на фоне лечения противовирусными препаратами были зафиксированы у 2 пациентов, получавших циклоферон (2%), 4 человек, принимавших ламивудин (4%), и 3 больных, лечившихся комбинированным курсом терапии ламивудин+ циклоферон (3%). Наиболее часто встречались обострения сопутствующей соматической патологии, особенно со стороны желудочно-кишечного тракта; исключение составляет один пациент, у которого на поздних сроках применения ламивудина развилась тромбоцитопения с резким снижением тромбоцитов, потребовавшая отмены препарата.
Обсуждение результатов
Исследование показало, что монотерапия циклофероном дает хороший первичный эффект (первичная ремиссия) в виде быстрой нормализации печеночных ферментов (1-3-й месяцы лечения), что говорит о высоком противовоспалительном действии препарата. Однако устойчивый биохимический и вирусологический ответ после циклоферонотерапии не превышает 33%. Использование ламивудина по результатам исследования не совсем оправдало наши ожидания. Первичная биохимическая ремиссия регистрировалась еще реже, чем при применении циклоферона (13% против 20%), а полная стабильная ремиссия лишь у 44% больных. Основная причина низкой эффективности ламивудина, по-видимому, вирусная резистентность мутантов по YMDD-мутации в ВГВ-полимеразе. Следствие этих процессов — возобновление репликации вируса и повышение АЛТ в сыворотке крови, несмотря на продолжающуюся терапию. В то же время ведение пациентов с возникшей мутацией неоднозначно. Некоторые специалисты предпочитают продолжение терапии даже после формирования резистентности с целью поддержания более низкого уровня ДНК ВГВ, АЛТ и гистологического улучшения, а также реактивации дикого штамма ВГВ. Другие считают, что продолжение лечения пациентов с наступившей резистентностью к ламивудину неэффективно.
В данном исследовании мутация в pre С-зоне HBV регистрировалась у 8 человек, YMDD-мутации в ВГВ-полимеразе у 44 чел. (табл. 8), причем 6 больным пришлось отменить терапию. В то же время необходимо обратить внимание, что у больных, получавших циклоферон, мутантные вирусы не возникали, а применение комбинированной терапии снижало их появление до 14%, эффективность же терапии за счет этого возрастала до 54%, то есть применение комбинированной терапии и, в частности, циклоферона и ламивудина — перспективное направление.
Таблица 8. Частота появления мутантных вирусов при различных схемах терапии
Схема лечения Нет мутаций, % Мутации в pre C-зоне HBV, % YMDD-мутант, % Циклоферон 100 - - Ламивудин 44 8 47* Циклоферон+ Ламивудин 86 1 14*
* Значения, существенно (р<0,005) отличающиеся в группе сравнения на данном этапе лечения.Выводы
- Установлена высокая клиническая эффективность исследуемых препаратов (циклоферон и ламивудин) при терапии больных ХВГВ. Полная стойкая ремиссия (со снижением ДНК ВГВ до неопределяемых цифр и сохранением нормализации АЛТ в течение 6 месяцев после окончания лечения) составила: с применением циклоферона — 33%, с применением ламивудина — 44%, с применением комбинированной терапии (циклоферон+ламивудин) — 54%.
- В процессе лечения ламивудином появляются мутантные вирусы и формируется резистентность к этому препарату. Применение циклоферона препятствует этому.
- Таблетки циклоферона (в дозе 10-15 мг/кг массы) при длительном применении (12 месяцев) не вызывали побочных и аллергических реакций при назначении как в виде монотерапии, так и в комбинации с ламивудином.
Список литературы
1. Kobayashi M., Suzuki E, Arase Y. et al. Infection with hepatitis В virus genotype A in Tokyo, Japan during 1976 through 2001 // J. Gastroenterol. 2004. Vol. 39. N 9. P. 844-50.
2. Ohata K., Hamasaki K., Toriyama K. et al. High viral load is a risk factor for hepatocellular carcinoma in patients with chronic hepatitis В virus infection // J. Gastroenterol. Hepatol. 2004. Vol. 6. P. 670-675.
3. Norder H., Courouce A. M., Coursaget P. et al. Genetic diversity of hepatitis В virus strains derived worldwide: genotypes, subgenotypes, and HBsAg subtypes // Intervirology 2004. Vol. 47. N 6. P. 289-309.
4. Hess G., Weber C, Rossol S. Treatment of hepatitis В surface antigen (HBsAg) — positive chronic hepatitis with recombinant alpha-A-interferon. Results of a phase II study// Z. Gastroenterol. 1988. Vol. 26. N 7. P. 380-387.
5. Seo Y, Yoon S., Hamano K. et al. Response to interferon-alpha in chronic hepatitis В with and without precore mutant strain detected by mutation site-specific assay. // J. Clin. Gastroenterol. 2004. Vol. 38. N 5. P. 460-464.
6. Cooksley W. G. Treatment with interferons (including pegylated interferons) in patients with hepatitis В // Semin Liver Dis. 2004. Vol. 24. Suppl 1. P. 45-53.
7. Kaygusuz I., Ozturk Kaygusuz Т., Ozturk A. Effects of interferon-alpha2b on hearing. // Int. J. Audiol. 2004. 43. N 8. P. 438-441.
8. Foldes I., David K., Horvath G. et al. Thyroid dysfunctions in patients with viral hepatitis treated with interferon-alpha // Orv. Hetil. 2004. Vol. 145. N 23. P. 1211-1216.
9. Tazulakhova E. В., Parshina O. V., Guseva T. S., Ershov F. I ssian experience in screening, analysis, and clinical application of novel interferon inducers // J. Interferon Cytokine Res. 2001. Vol. 21. N 2. P. 65-73.
10. Zarubaev V. V., SlitaA.V., Krivitskaya V. Z. Direct antiviral effect of cycloferon (10-carboxymethyl-9-acridanone) against adenovirus type 6 vitro // Antiviral Res. 2003. Vol. 58. N 2. P131-137.
11. Sokolova T. M., Uryvaev L. V., Tazulakhova E. В., Ershov F. I., Malyshenko-va I. K., Didkovskii N. A. Individual changes of gene expression in the interferon system in human blood cells due to amixin and cycloferon // Vopr Virusol. 2005. Vol. 50. N 2. P. 32-36.
12. Gaia S., Marzano A., Smedile A. Four years of treatment with lamivudine: clinical and virological evaluations in HBe antigen-negative chronic hepatitis В // Aliment Pharmacol. Ther. 2004. Vol. 20. N 3. P. 281-287.
13. Yeh С. Т., Chien R. N., Chu C. M. Clearance of the original hepatitis В virus YMDD-motif mutants with emergence of distinct lamivudine-resistant mutants during prolonged lamivudine therapy // Hepatology 2000. Vol.31. N6. P. 1318— 1326.
14. Ide Т., Kumashiro R., Kuwahara R., Koga H. Hepatitis В study group. Clinical course of patients with chronic hepatitis В with viral breakthrough during long-term lamivudine treatment // J. Gastroenterol. 2005. Vol. 40. N 6. P. 625-630.
15. Liaw Y. F, Chien R. N., Yeh С. Т. No benefit to continue lamivudine therapy after emergence of YMDD mutations // Antivir Ther. 2004. Vol. 9. N 2. P. 257-262.
16. Kiyosawa К., Тапака Е. Strategy for lamivudine-resistant YMDD mutant-associated chronic hepatitis В // J. Gastroenterol. 2001. Vol. 36. N 2. P. 139-141.
17. Cooksley W G. Treatment of hepatitis В with interferon and combination therapy //Clin. Liver Dis. 2004. Vol. 8. N 2. P. 353-370.
18. Danalioglu A., Kaymakoglu S., Cakaloglu Y, Demir K., Karaca V. Efficacy of alpha interferon therapy for lamivudine resistance in chronic hepatitis В // Int. J. Clin. Pract. 2004. Vol. 58. N 7. P. 659-61.
19. Chan H. L., HuiA. Y, Wong V. W, Chim A. M., Wong M. L., Sung J. J. Long-term follow-up of peginterferon and lamivudine combination treatment in HBeAg-positive chronic hepatitis В // Hepatology. 2005. Vol. 41. N 6. P. 1357-1364.
20. Jang M. K., Chung Y H., Choi M. H. Combination of alpha-interferon with lamivudine reduces viral breakthrough during long-term therapy // J. Gastroenterol. Hepatol. 2004 Vol. 19. N 12. P. 1363-1368.
21. Someya Т., Suzuki Y, Arase Y Interferon therapy for flare-up of hepatitis В virus infection after emergence of lamivudine-induced YMDD motif mutant // J. Gastroenterol. 2001. Vol. 36. N 2. P. 133-136.
| Август 2009 г. |