Опубликовано в журнале:
«Инфекционные болезни», 2010, т. 8, №1, с. 21-26Адаптогенные свойства метаболитного пребиотика Хилак-форте
А.А.Плоскирева, Д.В.Усенко, А.В.Горелов
Центральный НИИ эпидемиологии Роспотребнадзора, МоскваШирокое использование иммуномодулирующих препаратов в терапии инфекционных болезней у детей, недостаточная изученность их адаптационных реакций привлекает внимание большого количества специалистов. Было проведено многоплановое исследование адаптогенных свойств метаболитного пребиотика Хилак-форте при острых респираторных инфекциях (ОРЗ) у детей, изучена его клиническая, микробиологическая эффективность и способность изменять неспецифическую резистентность организма. Ключевые слова: острые респираторные инфекции, пребиотики, неспецифическая резистентность, адаптация
The adaptogenic properties of the metabolite prebiotic Hilak-forte
A.A.PIoskireva, D.V.Usenko, A.V.Gorelov, V.A.Vovk
Central Research Institute of Epidemiology, Federal Supervision Service for Control of Consumer Rights and People's Welfare, MoscowA wide use of immunomodulating drugs in the therapy of infectious diseases in children and insufficient knowledge of their adaptational reactions attracts the attention of many specialists. A multicenter study of the adaptogenic properties of the metabolite prebiotic Hilak-forte in acute respiratory infections (ARIs) in children was carried out, the clinical and microbiological efficacy of the preparation and its capability to change nonspecific resistance of the body was studied. Key words: acute respiratory Infections, prebiotics, nonspecific resistance, adaptation
Проблемы иммунодезадаптационных состояний организма в настоящее время привлекают внимание большого числа специалистов. К защитно-приспособительным свойствам организма человека относится неспецифическая резистентность, отвечающая за адаптацию к различным факторам внешней среды, в том числе к инфекции [1-4].
Изучением адаптационных реакций и резистентности организма традиционно занимались патофизиологи, иммунологи, такие, как Мечников И.И., Вернадский В.И., Лазарев Н.В., Селье Г., Смородинцев А.А., Гаркави Л.Х. и др.
Общая теория адаптации формировалась в трудах Н.А. Агаджаняна (1983, 1990), В.П.Казначеева (1973, 1974, 1980), Ф.З.Меерсона (1973, 1981, 1988), Г. Селье (1960, 1982).
В 1975 г. теорию, объясняющую механизм неспецифических реакций организма в процессе адаптации, предложила Л.Х.Гаркави с соавторами [1-5]. Эта теория позволила определить различные типы реакций адаптации, каждая из которых характеризуется определенными, присущими только ей комплексными изменениями в нейроэндокринной, иммунной, кроветворной системах организма. Среди них выделяют реакции тренировки, спокойной активации, повышенной активации и переактивации [1, 2].
Адаптационная реакция на слабые повторяющиеся раздражители называется неспецифической реакцией тренировки, она характеризуется стабильным состоянием всех регуляторных систем организма, при этом показатели, ее характеризующие (в частности показатели гемограммы), находятся в нижних пределах нормы. Если изменений в силе, частоте или интенсивности раздражающего воздействия не происходит, то организм перестает реагировать на него.
Более интенсивные раздражители вызывают в организме реакцию активации, которая подразделяется на подтипы: реакцию спокойной активации, повышенной активации и переактивации. Напряжение защитно-приспособительных возможностей организма возрастает от первой реакции к последующим.
Наиболее неблагоприятной является реакция стресса, открытая в 1936 году Г.Селье, которая характеризуется ответом на сильные, чрезвычайные воздействия не только усилением защитно-приспособительных функций, но и развитием выраженного напряжения и повреждения организма [1, 2].
Одну из ведущих ролей в защитных реакциях организма играет система иммунитета. Однако оценить состояние отдельных звеньев иммунитета не всегда представляется возможным. Поэтому особую актуальность приобретает определение лейкоцитарных индексов, позволяющих переводить гемограмму в соизмеримые числовые показатели, дающие возможность оценить реакцию системы крови и косвенно судить о состоянии иммунокомпетентной системы и ее реактивности.
Проблемы иммунодезадаптационных состояний организма тесно связаны с дисбактериозом различных биотопов (толстый и тонкий кишечник, слизистые оболочки полости рта, наружных половых органов и т.п.). Многочисленные экспериментальные данные и клинические наблюдения свидетельствуют о том, что совокупность биотопов организма человека является своеобразным экстракорпоральным органом, и формирование дисбиотических нарушений на определенном участке слизистой неизбежно будет распространяться на другие отделы, нарушая функционирование системы иммунного гомеостаза и повышая вероятность возникновения осложнений [6]. Ключевым в данной системе является обеспечение колонизационной резистентности, проявляющейся в антагонизме к чужеродным микроорганизмам и препятствию их адгезии к слизистым. В то же время нормальная микрофлора слизистых является одним из ключевых регуляторов иммунной системы организма. Так, например, стимуляция предшественников IgA плазматических клеток в кишечнике ведет к диссеминации антигенспецифических В- и Т- лимфоцитов во все эффекторные участки иммунной системы слизистых - в кишечнике, респираторном тракте, мочеполовой системе и др. [7, 8]. Данный механизм реализуется при применении пробиотиков в терапии инфекций ЖКТ. Нормализация состава кишечной микрофлоры обеспечивает восстановление колонизационной резистентности и стимуляцию мукозального иммунитета, играющих ключевую роль в процессах саногенеза, обеспечивая ускорение выздоровления. Поэтому в настоящее время в клинической практике все чаще используют различные про- и пребиотические препараты, позиционирующиеся как средства, обладающие иммуномодулирующей активностью и повышающие неспецифическую резистентность организма.
В последние годы получены объективные данные об эффективности использования пробиотиков в профилактике и лечении ОРЗ. Так, в исследовании de Vrese M. при использовании комплекса пробиотических бактерий (Lactobacillus gasseri PA 16/8, Bifidobacterium longum SP 07/3, B. bifidum MF 20/5) наблюдали существенное снижение выраженности основных симптомов ОРЗ, средней продолжительности заболевания, а также длительность лихорадочной реакции [9]. Ведущим механизмом полученных эффектов явилась биоценозопосредованная активация клеточного иммунитета- повышение уровня цитотоксических Т лимфоцитов (CD8+) и Т-хелперов (CD4+). В ходе другого исследования прием мультипробиотического комплекса (Lactobacillus GG, Streptococcus thermophilus, Lactobacillus acidophilus и Bifidobacterium), сопровождался снижением числа потенциально патогенных бактерий (Staphylococcus aureus, Streptococcus pneumoniae и бета-гемолитический стрептококк группы А) на слизистых оболочках верхних дыхательных путей [10]. Учитывая тот факт, что в этих исследованиях пробиотические микроорганизмы не обнаруживали в микрофлоре полости носа после их приема, полагают, что этот феномен обусловлен не конкурентным или бактерицидным действием пробиотиков, а повышением иммунного ответа организма.
Становится очевидным, что терапевтическая эффективность пробиотиков не ограничивается только коррекцией микроэкологических нарушений в отдельно взятом биотопе, а, посредством активации системы иммунологического гомеостаза, способна повысить эффективность лечения различных заболеваний, в том числе ОРЗ.
Цель настоящего исследования - оценка эффективности пребиотика метаболического типа Хилак-форте в комплексной терапии острых респираторных заболеваний у детей.
Пациенты и методы
Под наблюдением находились 104 больных со среднетяжелыми и осложненными формами ОРЗ в возрасте 0-13 лет, госпитализированных в профильные отделения Детской инфекционной больницы №5 г. Москвы. Все больные с поступления в стационар получали общепринятую базисную терапию, включавшую антибактериальные (амоксициллин/клавуланат, цефалоспорины 1, 3 поколения), муколитические, десенсибилизирующие препараты, сосудосуживающие капли в нос, щелочные ингаляции. Из них 32 пациента (4 мес - 1 года - 9 человек, 1-3 года - 10 детей, 4-7 лет - 8 и старше 7 лет - 5 детей) - составили основную группу, которая дополнительно к стандартной терапии с первого дня стационарного лечения получала Хилак-форте в возрастной дозировке (длительность курса 8-10 дней). В группы детей, получавших иммуномодулирующую терапию, вошли 42 пациента, в том числе 22 ребенка - Виферон в свечах в возрастной дозировке и 20 детей - Генферон в свечах.
В группу сравнения вошли 30 детей (4 мес-1 год - 6 человек, 1-3 года - 13 детей, 4-7 лет - 6 и старше 7 лет -5 детей), получавших стандартную терапию. Подбор больных проводился методом случайной выборки.
У всех пациентов заболевание протекало в среднетяжелой или тяжелой форме; чаще регистрировались поражения дыхательных путей в виде острого бронхита у 18 (56,3%) и 15 (50%) больных соответственно и пневмонии - у 4 (12,5%) и 3 (10%) пациентов соответственно. У 5 (15,6%) больных основной и 2 (6,6%) - группы сравнения ОРЗ сопровождалось развитием лакунарной ангины; катаральный средний отит диагностирован у 2 (6,2%) больных основной группы. Таким образом, сравниваемые группы были вполне сопоставимы для статистической обработки по возрасту, тяжести и формам заболевания.
Основными критериями оценки эффективности проводимой терапии были сроки купирования основных клинических симптомов и синдромов: «отличная» - при полном регрессе симптомов ОРЗ; «хорошая» - при значительном улучшении состояния больного (при возможном сохранении редкого кашля и/или единичных свистящих хрипов); «удовлетворительная» -уменьшение выраженности клинических симптомов к 7-м сут. от начала лечения. При отсутствии положительной клинической динамики лечение считалось неэффективным.
Помимо этого в план обследования 32 больных основной группы и 10 - группы сравнения было включено изучение состава микрофлоры толстой кишки (взятие исследуемого материала, посев его на селективные питательные среды, выделение чистых культур микроорганизмов и определение их видового и количественного состава по стандартной методике) двукратно - в первые сутки стационарного лечения и повторно через 8-10 дней.
У всех пациентов проводилось изучение индексов крови: лейкоцитарного индекса интоксикации (ЛИИ) по Кальф-Калифу, индекс Рейса, Островского, сдвига, эндотоксикоза по Даштаянц, аллергизации.
Обработка цифрового материала результатов исследования проводилась с использованием программы статистической обработки Primer of Biostatistics (V. 4.03). Вычисляли следующие величины: среднюю арифметическую «М»; среднюю ошибку средней величины «m» (ошибку репрезентативности). Достоверность различий «р» результатов исследования оценивали по критерию Стъюдента. Различие считали достоверными при р < 0,05.
Результаты исследования и их обсуждение
Клиническая эффективность Хилак-форте в комплексной терапии ОРЗ
Анализ динамики симптомов ОРЗ показал, что включение в комплексную терапию препарата Хилак-форте сопровождалось сокращением длительности интоксикационного синдрома. Так, продолжительность лихорадки составила 3,7 ± 0,3 против 4,6 ± 0,4 сут в группе сравнения (р = 0,049), при достоверно более низкой средней температуре - 38,1 ± 0,1 и 38,9 ± 0,1 °С соответственно (р = 0,001). У больных основной группы более чем на 1,5 сут быстрее восстанавливался аппетит - 3,4 ± 0,4 и 5,0 ± 0,4 сут, соответственно (р = 0,007).
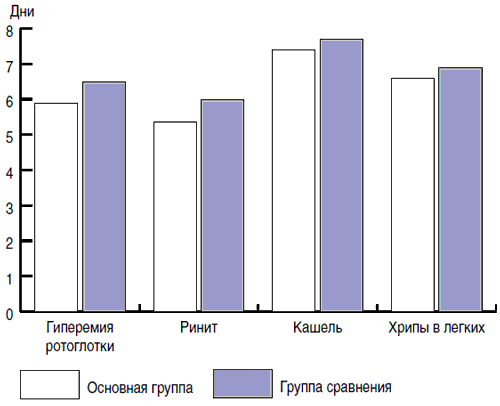
При применении Хилак-форте отмечена тенденция к сокращению длительности катаральных проявлений ОРЗ (рис. 1): гиперемии ротоглотки (5,9 ± 0,4 и 6,5 ± 0,4 сут соответственно р = 0,237) и ринита (5,4 ± 0,3 и 6 ± 0,3 сут соответственно, р = 0,318). Не было выявлено существенной разницы в длительности кашля и хрипов в легких.
Рис. 1. Продолжительность основных симптомов ОРЗ.
Проведение антибактериальной терапии у 4 больных группы сравнения сопровождалось развитием антибиотико-ассоциированной диареи (ААД), в виде учащения и изменения характера стула. В то же время, у пациентов основной группы, получавших аналогичные антибактериальные препараты на фоне приема Хилак-форте, не было отмечено симптомов ААД.
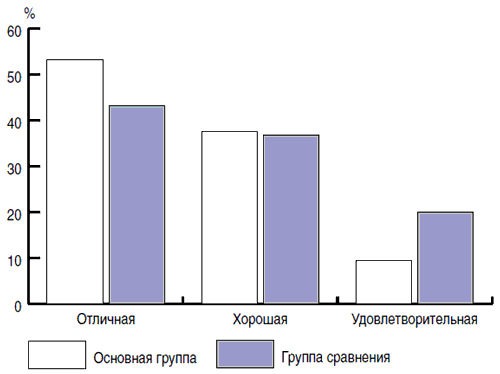
Таким образом, данные о сокращении длительности ряда симптомов (лихорадки, интоксикации и анорексии), снижении риска ААД, в совокупности сданными о клинической эффективности проведенного лечения (рис. 2), подтверждают целесообразность использования пребиотика метаболического типа Хилак-форте в комплексной терапии ОРЗ у детей.
Рис. 2. Клиническая эффективность терапии проведенного лечения.
Микробиологическая эффективность Хилак-форте у детей, больных ОРЗ
Комплексная оценка эффективности Хилак-форте при ОРЗ помимо изучения динамики клинических проявлений заболевания включала изучение состояния микрофлоры толстой кишки (у всех больных основной группы и 10 - группы сравнения). Было установлено, что у подавляющего большинства детей течение ОРЗ сопровождалось развитием выраженных нарушений микробиоценоза ЖКТ уже в остром периоде (таблица). Наибольшие изменения были выявлены в популяции бифидофлоры - лишь у 12,5% больных основной группы и 10% - группы сравнения ее уровень определялся выше 108 КОЕ/гр. Дефицит лактобактерий был обнаружен у 43,8 и 40% больных соответственно. Доля больных с выявленными нарушениями в популяции энтерококков была еще более высока - 75 и 90%. При этом одинаково часто был отмечен как избыточный их рост (у 40,6 и 50% соответственно), так и их дефицит (у 34,3 и 40% пациентов соответственно). В основной группе дефицит колифлоры был выявлен у половины больных, в то время как в группе сравнения только у 30% обследованных. Данные нарушения сопровождались появлением кишечной палочки с измененной ферментативной активностью, в том числе лактозонегативной (у 12,5 и 30% больных соотв.) и гемолизирующей (у 15,6 и 10% соответственно).
Таблица. Частота дисбиотических нарушений микрофлоры кишечника у детей с ОРЗ (%)
Название микроорганизмов Уровень микроорганизмов Основная группа
(n = 32)Группа сравнения,
(n = 10)до лечения после лечения до лечения после лечения Lactobacillus <106 43,8 15,6 40 40 Bifidobacterium <108 87,5 25 90 70 Е. coll с измененной ферментативной активностью >105 28,1 21,9 40 30 Staphylococcus >103 18,8 3,1 20 30 Дрожжеподобные грибы >104 46,9 21,9 10 40 Clostridium >105 3,1 0 0 30 Энтерококк >25% 75 46,9 90 80 УПФ (Proteus, Citrobacter, Enterobacter и др.) >104 9,3 0 0 30 Исследуя состояние микрофлоры кишечника на фоне проводимого лечения, мы установили, что в группе больных, получавших Хилак-форте, несмотря на проведение антибактериальной терапии, нормализация уровня бифидобактерий к концу лечения констатирована в 62,5%, лактобактерий - у 28,2% больных, энтерококков - 28,1%, элиминация стафилококков, Proteus, Clostridium, более чем в два раза реже обнаруживали повышенные титры дрожжеподобных грибов (с 46,9 до 21,9%). У больных группы сравнения на фоне проводимой антибактериальной терапии сохранялись выявленные дисбиотические нарушения как в составе облигатной, так и факультативной микрофлоры.
Проведен интегральный анализ состояния микрофлоры желудочного кишечного тракта у детей на фоне терапии Хилак-форте с помощью разработанного нами индекса колонизационной резистентности (заявка на патент №2008130937 от 2008 г.) [11].
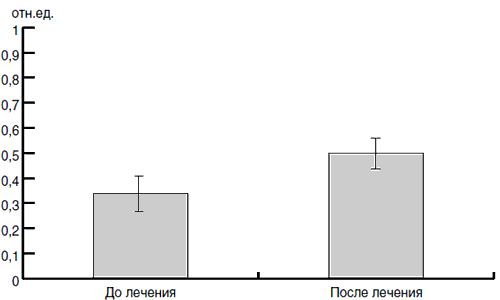
При сравнении среднего показателя индекса колонизационной резистентности в группе детей, получавших в составе комплексной терапии ОРЗ Хилак-форте, достоверных отличий в уровне этого показателя до лечения и после получено не было (рис. 3).
Рис. 3. Средний индекс колонизационной резистентности в группе детей, получавших Хилак-форте, до и после лечения.
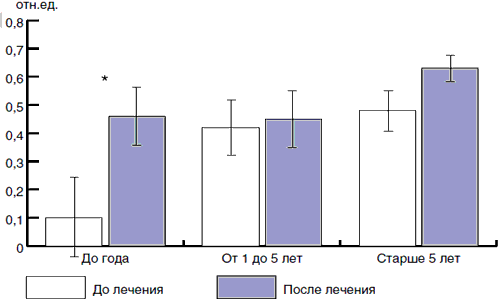
Однако при более детальном рассмотрении этого показателя в различных возрастных группах нами было получено достоверное увеличение его после лечения у детей первого года жизни, для которых изменения в составе микрофлоры являются наиболее прогностически значимыми (рис. 4).
Рис. 4. Зависимость уровня индекса колонизационной резистентности до лечения и после в зависимости от возраста пациентов, получавших Хилак-Форте (здесь и на рис. 5-8: * - различия достоверны при р < 0,05).
При динамичном изучении состояния микрофлоры желудочно-кишечного тракта в различные сроки после выздоровления нами была получена линейная зависимость с высоким индексом корреляции индекса колонизационной резистентности (рис. 5). При этом к 8-27 сут после выздоровления наблюдали достоверное повышение этого индекса по сравнению с исходным состоянием.
Рис. 5. Динамика индекса колонизационной резистентности у детей, больных ОРЗ и получавших Хилак-форте.
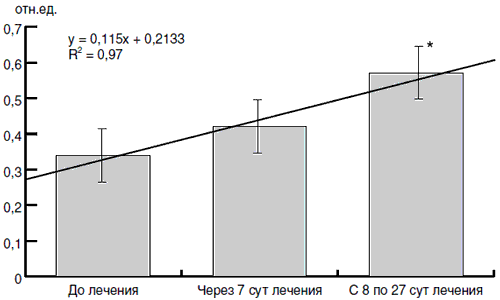
Таким образом, пребиотик метаболитного типа Хилак-форте способствовал улучшению состояния измененной микрофлоры желудочно-кишечного тракта у детей, больных ОРЗ, получавших антибактериальную терапию. При этом наиболее значимый эффект отмечался у детей первого года жизни.
Изучение адаптационных свойств Хилак-форте у детей, больных ОРЗ
Для изучения способности Хилак-форте изменять неспецифическую резистентность организма на фоне ОРЗ, проведено сравнение эффективности данного препарата и препаратов с доказанным иммунотропным эффектом Виферон в свечах (22 ребенка) и Генферон в свечах (20 детей).
На рис. 6-8 приведены данные динамики изменения показателя ЛИИ у детей, получавших Хилак-Форте, Виферон и Генферон.
Рис. 6. Влияние Виферона на основные индексы крови у детей, больных ОРЗ.
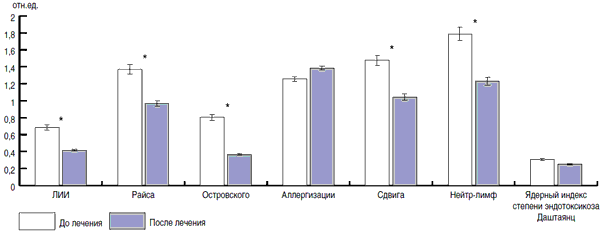
Рис. 7. Влияние Генферона на основные индексы крови у детей, больных ОРЗ.
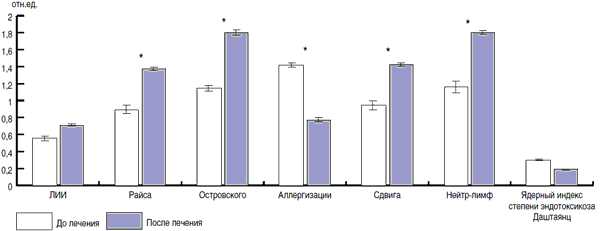
Рис. 8. Влияние Хилак-форте на основные индексы крови у детей, больных ОРЗ.
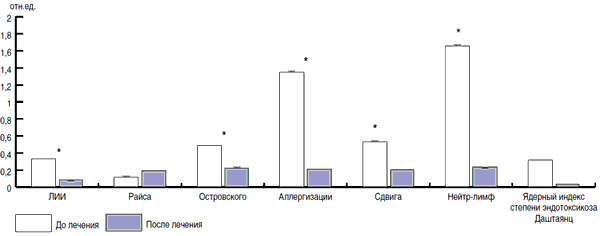
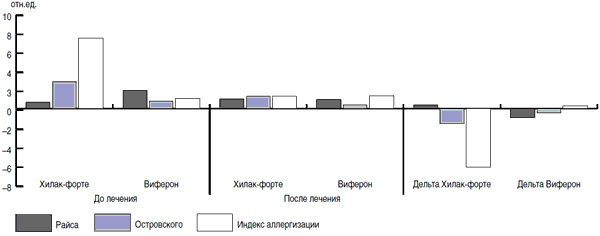
На первый взгляд, действие препаратов Виферон, Генферон и Хилак-Форте разнонаправлено и несопоставимо. Однако, используя адаптационно-энтропийный подход [12], удалось выявить способность этих препаратов изменять неспецифическую резистентность организма человека. При расчете ЛИИ были получены данные (рис. 9), демонстрирующие «стягивание» показателей в зону средних значений на фоне проводимой терапии. Эти данные подтверждают адаптивный характер изменений, развивающихся на фоне терапии иммуномодуляторами и препаратом Хилак-Форте. Анализируя полученные данные между показателями после лечения и начальным уровнем, можно видеть, что зависимость носит обратный характер, т.е. отмечается зеркальная симметрия (отражено в показателе разности - дельта). Учитывая тот факт, что этот феномен наблюдается на фоне реакции переактивации адаптации и характеризуется уменьшением таких показателей, как лейкоцитарный индекс интоксикации, индекс сдвига лейкоцитов, соотношения нейтрофилов и лимфоцитов (рис. 10, 11), можно говорить о том, что Хилак-Форте обладает способностью изменять неспецифическую резистентность организма.
Рис. 9. Динамика изменений ЛИИ у детей на разных видах терапии с использованием метода подсчета разности.
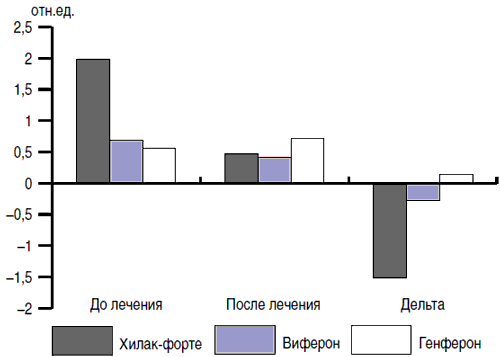
Рис. 10. Динамика индексов крови у пациентов, находящихся на разных видах терапии в зависимости от уровня изучаемого показателя.
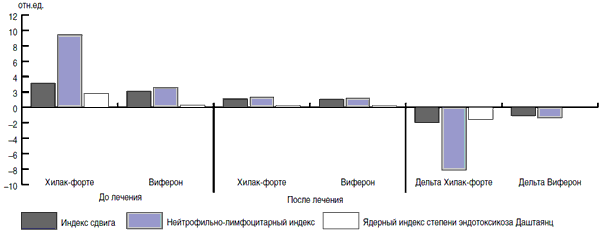
Рис. 11. Динамика индексов крови у пациентов, находящихся на разных видах терапии.
Подводя итог проведенным исследованиям, можно заключить, что препарат Хилак-Форте обладает отчетливыми адаптивными свойствами. Для оценки изменений неспецифической резистентности под воздействием иммунотропных лекарственных средств наиболее приемлем адаптационно-энтропийный подход и метод подсчета разности, т.к. они позволяют отразить динамику изменений показателей неспецифической резистентности.
Выводы
- Включение пребиотика Хилак-Форте в комплексную терапию осложненных форм острых респираторных инфекций у детей приводит к сокращению длительности основных клинических симптомов, осложнений, уменьшает выраженность дисбиотических нарушений, повышая уровень облигатной микрофлоры кишечника, обеспечивает профилактику антибиотико-ассоциированных диарей.
- Пребиотик метаболитного типа Хилак-Форте у детей, больных ОРЗ, вызывает изменение неспецифической резистентности организма путем развития адаптационных реакций.
- Полученные результаты наглядно свидетельствуют о целесообразности использования метаболического пребиотика Хилак-форте в комплексной терапии ОРЗ у детей, в качестве средства, оказывающего адаптивный эффект и восстановление микробиоценоза ЖКТ, что и повышает эффективность проводимой терапии.
ЛИТЕРАТУРА
1. Гаркави Л.Х., Квакина Е.Б., Уколова М.А. Адаптационные реакции и резистентность организма. 1979; 128.
2. Гаркави Л.Х., Квакина Е.Б., Кузьменко T.C., Шихлярова А.И. Антистрессор-ные реакции и активационная терапия. Екатеринбург: РИА «Филантроп», 2002; 194.
3. Гречко A.T. Физиологические механизмы адаптации и ее фармакологическая коррекция «быстродействующими адаптогенами». Междунар. мед. обзоры 1994; 5(2): 330-3.
4. Шабанов П.Д., Ганапольский В.П., Зарубина И.В. и др. Метаболический активатор трекрезан: изучение адаптогенных и иммуномодулирующих свойств. Международный научно-практический журнал «Нейронауки» 2006; 3(5): 43.
5. Зарубина И.В., Шабанов П.Д. Молекулярная фармакология антигипоксантов. СПб.: Н-Л, 2004; 368.
6. Шендеров Б.А. Медицинская микробная экология и функциональное питание. Т. 2. Социально-экологические и клинические последствия дисбаланса микробной экологии человека и животных. М.: Грантъ, 1998; 420.
7. Беляев И.М. Иммунная система слизистых. Иммунология 1997; 4: 7-13.
8. Хаитов P.M., Пинегин Б.В. Иммунная система желудочно-кишечного тракта: особенности строения и функционирования в норме и при патологии. Иммунология 1997; 5: 4-7.
9. de Vrese M., Winkler P., Rautenberg P., et al. Effect of Lactobacillus gasseri PA 16/8, Bifidobacterium longum SP 07/3, B. bifidum MF 20/5 on common cold episodes: a double blind, randomized, controlled trial. Clin Nutr. 2005; 24(4):479-80.
10. Gluck U., Gebbers J.O. Ingested probiotics reduce nasal colonization with pathogenic bacteria (Staphylococcus aureus, Streptococcus pneumoniae, and P-hemolytic streptococci). Am J Clin Nutr 2003; 77: 517-20.
11. Плоскирева А.А. Индекс колонизационной резистентности, как один из методов комплексной оценки дисбактериоза кишечника. Материалы Российской научно-практической конференции «Инфекции, вызываемые условно-патогенными микроорганизмами». М., 2007; 79.
12. Кирилличева Г.Б. Адаптационно-биоритмологические основы вариабельности иммуномодулирующего эффекта. Автореф. дисс. ... докт. мед. наук. М., 2000; 48.
| Февраль 2012 г. |