Динамика клинико - иммунологических показателей в оценке эффективности применения Мексидола при пояснично-крестцовой радикулопатии
Лихачева Е.Б., Шоломов И.И.
Саратовский государственный медицинский университет. Кафедра нервных болезней.Проведен анализ эффективности применения препарата Мексидол® в комплексном лечении пояснично-крестцовых радикулопатий. Доказано превосходство данного метода по сравнением с традиционным лечением с помощью клинико-иммунологических методик. Выявлена зависимость скорости ремиелинизации нервных волокон вследствие применения цитопротекторной антигипоксической терапии.
Заболевания периферической нервной системы занимают второе место в структуре всей неврологической патологии у взрослых. При этом, пояснично-крестцовые радикулопатии (ПКР) занимают ведущее место среди всех заболеваний периферической нервной системы, и составляют 70% [8].
Патологические изменения межпозвонковых дисков в 90 % случаев являются причиной радикулопатии на уровне пояснично-крестцового отдела позвоночника. В этой группе следует особо выделить дискогенные радикулопатии, занимающие ведущее место в структуре неврологических заболеваний как по тяжести процесса, так и по их биосоциальным последствиям. При этом на долю дискогенных поясничных радикулопатий приходится от 70 до 86 % от общего количества потерь рабочего времени по нетрудоспособности из-за заболеваний нервной системы при нарастании инвалидизации.
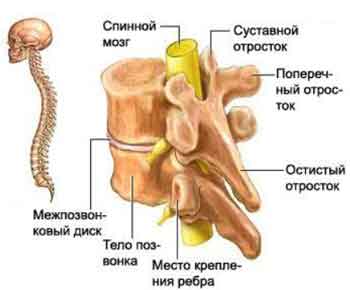
Согласно общим представлениям, основным патологическим субстратом остеохондроза является дегенеративно-дисторофический процесс в межпозвонковых дисках.
По данным Антонова И.П. остеохондроз развивается в результате врожденной или приобретенной функциональной недостаточности соединительной ткани и протекает как ее системное, хроническое поражение.
По современным представлениям, причиной ПКР могут быть вертеброгенные (чаще всего остеохондроз позвоночника (ОП)) и невертеброгенные факторы. Корешковые синдромы выявляются у 37,4% больных с дегенеративно-дистрофическими изменениями межпозвонковых дисков [11].
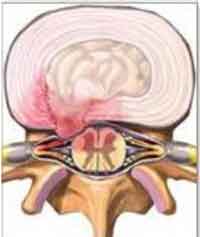
При вертеброгенном поражении корешка, связанного со сложностью взаимоотношений его с образованиями позвоночного канала, проявляется действие вегетативно-сосудистых, реактивно-воспалительных, застойных и других факторов, и клинические проявления корешковых расстройств зависят от степени вовлечения корешков в патологический процесс [1]. При повреждении волокон нервного корешка в результате механического воздействия в одной части волокон отмечается сегментарная демиелинизация, в другой части наблюдается Валлеровское перерождение клеток [20, 22].
Повреждение ультраструктуры нервных волокон корешка приводит к нарушению проведения электрических импульсов и аксонального транспорта, то есть при ПКР в условиях гипоксии и отека корешка страдает обеспечение трофическими факторами и обмен веществ между телом нейрона и его отростками. У больных ПКР отмечается активация перекисного окисления липидов, проявляющаяся в повышении уровня диеновых конъюгатов, малонового диальдегида [7, 17]. При ПКР продукты распада и токсины из мест дегенерации корешка за счет большего проксимально-дистального аксоплазменного градиента переносятся в нижние отделы сплетения, периферические нервы, вызывая там те же процессы, которые клинически проявляются дистальными парезами. С помощью ретроградного транспорта те же продукты распада попадают в тело нервной клетки, нарушая работу ее цитоплазменных структур и изменяя защитную функцию всего неврального аппарата. В результате происходит уменьшение выработки миелина, дальнейшее повреждение гемато-неврального барьера (вторичная демиелинизация), и, в итоге, хронизация заболевания [8].
Нейроиммуные механизмы играют значимую роль в формировании генераторов патологически усиленного возбуждения и формировании патологической алгической системы [5, 15]. Выявлены общие для нервных и иммунокомпетентных клеток молекулярные рецепторы, через которые осуществляется сочетанная регуляция систем контроля боли и иммунных реакций. Нарушения нейроэндокринноиммунных взаимоотношений являются типовыми механизмами патогенеза любых болевых синдромов. Циркуляция в крови больных различными формами патологии нервной системы аутоантител к разнообразным антигенам нервной ткани свидетельствует об аутоиммунном процессе, патогенетическая значимость которого в развитии указанных заболеваний остается невыясненной [13]. В настоящее время теория аутоиммунных механизмов развития ОП и ПКР является актуальной [6]. Развивающиеся в организме при ПКР иммунные реакции имеют как патогенетическую, так и саногенетическую направленность. При первом виде реакций возможны прогрессирование дистрофического процесса в МПД в результате аутоагрессивного действия антител [10], распространение дистрофии на другие структуры позвоночного сегмента вследствие перекрестной аутоагрессии к тканям, близким диску по антигенным свойствам [14]. Кроме того, развивается аутоиммунный воспалительный процесс в корешках спинномозговых нервов, прилегающих к диску, эпидуральной клетчатке, оболочках спинного мозга [12]. Саногенетические иммунные механизмы заключаются в усилении Т -супрессорной активности лимфоцитов, способствующей уменьшению образования АТ, элиминации АГ и иммунных комплексов из крови и тканей [10]; рассасывании тканей выпавшей грыжи под влиянием макрофагов и лимфоцитов; усилении регенеративных процессов в диске. Чем раньше включаются механизмы саногенеза, тем более благоприятно протекает заболевание. Длительно текущие болевые синдромы при ОП приводят к вторичным иммунодефицитным состояниям, при которых страдают и клеточная, и гуморальная системы иммунитета [16]. Ряд исследователей показывает повышение иммунологических показателей при ПКР, в частности интерлейкина -1 (ИЛ-1), фактора некроза опухоли (ФНО), антител (АТ) к основному белку миелина (ОБМ) и фактору роста нерва (ФРН) [8]. Наличие АТ к ФРН и ОБМ могут свидетельствовать об аутоиммунном воспалении в нервной ткани.
В последние годы возрастает интерес к выявлению антинейтрофильных цитоплазмагических антител (АНЦА). Основным компонентом р-АНЦА являются антитела к миелопероксидазе (МПО). МПО представляет собой гемопротеин, содержащийся в азурофильных гранулах полиморфноядерных лейкоцитов и играющий важную роль в их антибактериальной и цитотоксической активности. АТ к МПО обнаруживаются при васкулитах, гломерулонефрите, узелковом периартериите, системной красной волчанке, ревматоидном артрите, титр этих антител возрастает во время обострения болезни. АНЦА могут обнаруживаться и при других заболеваниях. Положительный тест на ANCA отмечен у 2-4% здоровых людей. В последнее время высказывается гипотеза об участии АНЦА в патогенезе микроваскулитов. Аутоантитела к коллагену наиболее часто обнаруживают при ревматоидном артрите (вследствие иммунокомплексного внутрисуставного воспаления), системной красной волчанке, системной склеродермии, болезни Бехтерева, болезни Бехчета, гранулематозе Вегенера и др. Поскольку аутоагрессия является отражением патогенетических иммунных реакций и может быть направлена не только на нервные элементы корешка и периферического нерва, но и на окружающие их образования, то есть сосуды и костно-суставную систему позвоночника, нам представилось интересным изучить уровень АТ к коллагену и миелопероксидазе в сыворотке крови больных ПКР, их динамику в результате проводимого лечения.
Лечение больных с данной патологией комплексное. Важнейшим должно быть этиологическое лечение, однако принципы его в настоящий момент недостаточно разработаны.
Основными направлениями лекарственной терапии являются:
купирование основных механизмов раздражения синувертебрального нерва и устранение сосудистых и дистрофических изменений в области экстравертебральных очагов (стероидные и нестероидные противовоспалительные средства, сосудистые препараты, миорелаксанты); активизация трофических процессов (биогенные стимуляторы, хондропротекторы, препараты витаминов, анаболические препараты); симптоматическая терапия (транквилизаторы, антидепрессанты, гастропротекторы). Этот далеко не полный перечень основных медикаментозных средств, которые можно применять при лечении ПКР, позволяющий выбрать индивидуальную схему для конкретного больного в зависимости от патогенеза ведущих клинических симптомов. Основная часть лекарственных препаратов, используемых для консервативной терапии ПКР, имеет много противопоказаний и побочных эффектов. Поэтому тактика лечения должна быть направлена на рациональное назначение лекарственных препаратов, не допуская полипрагмазии.
В связи с этим, лечение нервных расстройств, в основе которых лежит дефицит трофических веществ, должно заключаться в восполнении этого дефицита. Учитывая общность патогенетических механизмов поражения центральной и периферической нервной системы при ряде заболеваний, представляет интерес изучить эффективность нейропротекторного препарата "Мексидол" при ПКР.
Мексидол (3-окси-6-метил-2-этилпиридина сукцинат) является антигипоксантом прямого действия, антиоксидантом и мембранопротектором, обладающим стресспротективным, ноотропным, противосудорожным и анксиолитическим действием. Препарат повышает резистентность организма к кислородозависимым патологическим состояниям (шок, гипоксия и ишемия, нарушения мозгового кровообращения, интоксикация алкоголем и антипсихотическими средствами (нейролептиками)) и к воздействию различных повреждающих факторов.
Мексидол эффективен при разных видах гипоксии, защищает нервные клетки от гибели, вызываемой ишемией, нормализуя метаболизм мозговой ткани, улучшает усвоение кислорода в мозговой ткани, усиливает аэробный гликолиз в мозге, повышает устойчивость организма к кислородзависимым патологическим процессам. При этом мексидол обладает свойством стабилизировать мембраны и облегчает проникновение молекулы в клетку и использование остатка пиридина и сукцината в качестве энергетических субстратов. В присутствии мексидола происходит активация сукцинатоксидазного пути окисления, который в условиях ограничения НАД-зависимого окисления на ранних стадиях гипоксии позволяет сохранить в митохондриях определенный уровень окислительного фосфорилирования. Активация сукцинатоксигеназного пути окисления при гипоксии способствует повышению резистентности клеток мозга, миокарда, печени к дефициту кислорода и определяет механизм антигипоксического действия мексидола. Ингибирование перекисного окисления вследствие повышения резервных возможностей системы антиоксидантной защиты, благоприятно влияет на липидный спектр крови и агрегационную активность тромбоцитов, снижает увеличенную гемостатическую активность за счет повышения деформируемости эритроцитов, снижения вязкости крови.
Целью настоящей работы стал анализ эффективности комплексной терапии ПКР с применением мексидола, оценка влияния цитопротекторной антигипоксической терапии на скорость ремиелинизации нервных волокон, сопоставление сроков наступления клинической и иммунологической ремиссии.
Материал и методы. На базе неврологического отделения городской клинической больницы № 9 г. Саратова за период 2002-2005 гг. обследовано 205 человек больных с клиническими проявлениями ПКР. Возраст больных составил от 18 до 74 лет; женщин - 104, мужчин - 101 чел. Больные были разделены на две сравнимые по полу и возрасту группы - основную (ОГ) и группу сравнения (ГС). Численность ОГ составила 110 человек (56 мужчин и 54 женщины), ГС - 95 (49 мужчин и 46 женщин). Также в исследовании участвовали 30 практически здоровых людей в качестве группы контроля. Всем больным проведен курс общепринятой медикаментозной и физиотерапии, в ОГ дополнительно применялся мексидол по 2-4 мл 5% раствора 2 раза в день внутримышечно или внутривенно, 10 -15 дней. До начала лечения в обеих группах проведены тщательное неврологическое обследование, клинико-лабораторное (общий анализ крови) и биохимическое исследования (сиаловые кислоты, фибриноген, С-реактивный белок), стимуляционная электронейромиография (ЭНМГ), нейровизуализирующие (КТ, ЯМРТ) методики. По окончании лечения повторно проводилась та же программа исследования, не включая рентгенологические методы и МРТ. Кроме того, у части пациентов определялись АТ к миелопероксидазе (МПО) в сыворотке крови методом иммуноферментного анализа (ИФА) с использованием тест-систем фирмы ''Хема - медика'' (Россия). Ауто-АТ к коллагену в сыворотке крови определялись с помощью реакции преципитации (РП). Статистическая обработка полученных данных осуществлялась с использованием программы С. Гланца ''Медико-биологическая статистика'' [9].
Результаты исследования и их обсуждение.
Диагноз ПКР был поставлен пациентам обеих групп на основании подробного сбора анамнеза и тщательного неврологического обследования. Следует отметить, что в ОГ у 19 (17,3%) больных заболевание выявлялось впервые, у остальных 91(82,7%) - повторно, в ГС - 14 (14,7%) и 81 (85,3%) соответственно. Провоцирующим фактором развития ПКР явилось переохлаждение (16 чел. (14,6%) в ОГ и 12 (12,6%) в ГС), перенесенная вирусная инфекция (5 чел. (4,5%) в ОГ и 4 (4,2%) в ГС), тяжелая физическая нагрузка (33 чел. (30%) в ОГ и 30 (31,6%) в ГС) или сочетание факторов (56 чел. (50,9%) в ОГ и 49 (51,6%) в ГС). Практически всем обратившимся за стационарной помощью был проведен курс амбулаторного лечения, который или не дал положительного результата, или ожидаемый эффект был неполным. Так как все больные в сравниваемых группах испытывали болевые ощущения в той или иной мере, большое внимание уделялось оценке регресса болевого синдрома. Наиболее простым и информативными тестом для количественной оценки восприятия боли, по мнению ряда исследователей [4], является визуальная аналоговая шкала (ВАШ). ВАШ представляет собой отрезок прямой линии длиной 10 см, где начальная точка (ноль) соответствует отсутствию боли, а конечная (десять) - невыносимым болевым ощущениям. С помощью ВАШ мы регистрировали изменение болевых ощущений во время ходьбы по ровной поверхности и лестнице, при сидении, стоянии, в покое. Результаты исследования болевого синдрома представлены в таблице 1.
Таблица 1. Интенсивность боли по ВАШ при повседневной активности у пациентов с ПКР до и после лечения
Средние показатели ВАШ (баллы) ОГ, (M±m) ГС, (M±m) До лечения (n=110) После лечения (n=110) До лечения (n=95) После лечения (n=95) 1. Ходьба по плоской поверхности 5,2±0,4 2,2±0,5* 4,9±0,7 4,2±0,9 2. Ходьба по лестнице 6,4±0,6 3,4±0,3* 6,7±0,2 6,3±0,5 3. Ночью в постели 2,1±0,5 1,5±0,6* 3,0±0,4 2,4±0,6* 4. Положение сидя 6,7±0,3 2,6±0,8* 6,9±0,4 5,6±0,9* 5. Положение стоя 4,8±0,6 2,2±0,7* 4,6±0,4 3,9±0,8 6. Уровень боли в наилучшие периоды болезни (как близко к нулю) 2,3±0,5 0,5±0,1* 2,1±0,4 2,0±0,5 7. Уровень боли в наихудшие периоды болезни (как близко к десяти) 8,6±0,7 5,3±0,4* 8,7±0,2 8,4±0,6 Примечание: * - статистически достоверная разница между показателями у пациентов до и после лечения, р<0,05.Из таблицы видно, что наиболее интенсивные болевые ощущения пациенты испытывали при сидении и ходьбе по лестнице. По первым пяти параметрам для каждого пациента при ежедневном осмотре высчитывался средний балл болевых ощущений. В ГС выраженный болевой синдром (7-10 баллов) наблюдался у 29,4% пациентов, средней интенсивности (4-6 баллов) у 53,6%, умеренный (1-3 балла) в 16,8% случаев (28, 51 и 16 человек соответственно). В ОГ эти же показатели распределились следующим образом: 7-10 баллов -26,4 % (29 чел.), 4-6 балла - 51,8% (57 чел.) и 1-3 балла -21,8 % (24 чел.). После завершения курса лечения при оценке болевого синдрома в ОГ снижение боли на 5 и более баллов отмечалось у 48 (43,6%) пациентов, снижение на 1-4 балла - у 62 (56,4%). В ГС снижение на 5 баллов и более наблюдалось у 8 (8,4%) пациентов, на 1-4 балла - у 48 (50,5%), без динамики - у 38 (40%), усиление боли отмечалось в 1 (1,05%) случае. Динамика снижения интенсивности болевого синдрома в процессе лечения представлена на диаграммах (рис.1, 2). Из рисунка 1 видно, что в ОГ наибольший темп снижения боли происходит с 10 по 20 дни лечения, причем к дню выписки (25-30-й день) более чем у 50% пациентов болевой синдром полностью купируется, у остальных становится умеренным, требующим лишь периодического приема обезболивающих средств. В ГС мы также наблюдаем регресс болевого синдрома, но менее значительный, чем в ОГ. К моменту завершения курса лечения в ГС преобладает количество больных с умеренным болевым синдромом (51,6%), однако остается значительным количество лиц с болью средней интенсивности(25,3%), требующей постоянного приема обезболивающих средств.
Рисунок 1.
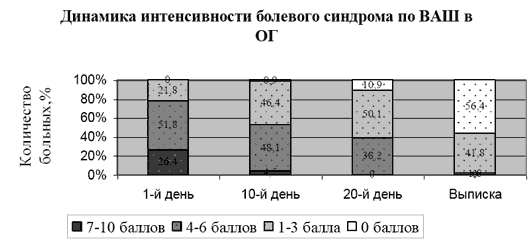
Рисунок 2.
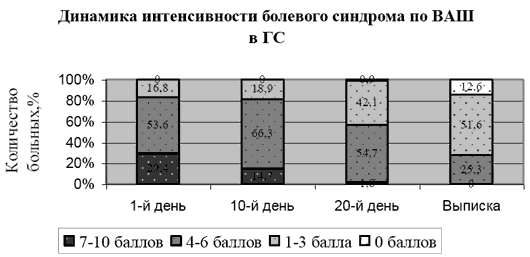
Таким образом, при проведении комплексной терапии с использованием мексидола результаты по уменьшению интенсивности болевого синдрома в ОГ значительно оптимистичнее, нежели в ГС. У больных с ПКР в сравниваемых группах до лечения выявлялась различная неврологическая симптоматика в виде анизорефлексии, симптомов натяжения (Ласега, Нери, Дежерина, Бонне, Вассермана, Сикара), изменения статики и динамики позвоночника, мышечно-тонический синдром, выпадение чувствительности в соответствующих дерматомах, вегетативно -трофические расстройства (сухость кожи, поредение волосяного покрова на нижних конечностях, гиперкератоз стоп), в ряде случаев отмечалось снижение силы в отдельных мышечных группах. Подавляющее большинство пациентов (92 (83,6%) в ОГ и 88(92,6%) в ГС) имели одностороннее поражение, 18 (16,4%) и 7 (7,4%) человек соответственно - двустороннее. Динамика клинических симптомов в обеих группах представлена в таблице 2. Из таблицы видно, что в ОГ у всех пациентов, кроме одного, претерпел обратное развитие мышечно-тонический синдром, тогда как в ГС - только у 6 из 18 (33,3%); у 72 больных ОГ (69,2%) купировались симптомы натяжения, в ГС - лишь у 11 (11,6%). Динамика в рефлекторной сфере: восстановление (полное или частичное) зарегистрировано в ОГ у 40 (42,6%) больных, в ГС - у 14 (16,3%). У остальных пациентов динамики не отмечено. Положительная динамика в восстановлении чувствительности отмечалась в ОГ у 36 (36,7%) пациентов, в ГС - у 13 (14,6%), мышечной силы - в ОГ у 5 (21,7%) пациентов, в ГС - у 1 (6,3%). Отрицательной динамики не отмечено.
Таблица 2. Динамика клинических симптомов у больных ПКР в результате лечения
СИМПТОМЫ ДО ЛЕЧЕНИЯ ПОСЛЕ ЛЕЧЕНИЯ % УЛУЧШЕН ИЯ ОГ (n=110) ГС (n=95) ОГ (n=110) ГС (n=95) ОГ ГС абс % абс % абс % абс % Симптомы натяжения 104 94,5 95 100 38 34,5 84 88, 4 60 11,6 Нарушение чувствительности 98 89,1 89 93,7 62 56,4 76 80, 0 32,7 13,7 Отсутствие или снижение рефлексов 94 85,5 86 90,5 54 49,1 72 75, 8 36,4 14,7 Парезы 23 20,9 16 16,8 18 16,4 15 15, 8 4,5 1,0 Мышечно-тонический синдром 21 19,1 18 18,9 1 0,9 12 12, 6 18,2 6,3 Вегетативно-трофические расстройства 24 21,8 19 20 20 18,2 18 18, 9 3,6 1,1 Таким образом, более значительный регресс неврологического дефицита был достигнут в ОГ, особенно в отношении мышечно-тонического синдрома и симптомов натяжения, которые вкупе с болью причиняют наибольшие страдания больным. Также следует отметить более быстрое, нежели в ГС, восстановление рефлексов и чувствительности, что может свидетельствовать об уменьшении воспалительных и гипоксических нарушений в корешке и периферических нервах, уменьшении отека, а также начавшихся процессах ремиелинизации. Столь незначительная динамика в обеих группах в отношении дистальных парезов и вегетативно-трофических расстройств может говорить о значительном поражении миелиновой оболочки двигательных волокон корешков и периферических нервов, для восстановления которых требуется больший, чем 15-30 дней стационарного лечения, временной промежуток и поддерживающая медикаментозная и физиотерапия в амбулаторных условиях. При субъективной оценке эффективности лечения в ОГ "улучшение" отметили 108 пациентов (98,2%), в ГС - 37 (38,9%).
По данным рентгенологического исследования и МРТ, в обеих группах у всех больных были выявлены признаки остеохондроза позвоночника, спондилеза и спондилоартроза, захватывающих от 1 -2 позвонков до полного поражения пояснично-крестцового отдела. Диагностированы грыжи Шморля в 9 (4,4%) случаях, у одного больного множественные, а также в 100% случаев - межпозвонковые задние протрузии и (или) грыжи: у 28 человек -срединная (13,7%), у 147 - парамедианная (71,7%), у 30 - боковая (14,6%), в том числе множественные - у 25 (12,2%). Локализация протрузий и грыж: у 128 (62,4%) пациентов на уровнях L5-S1, 71 (34,6%) - L4-L5, 4 (1,95%) - L3-L4, по одному (0,5%)- на уровнях L2-L3 и L1-L2. В 64,8% (133 чел.) случаев протрузии и грыжи компремировали переднюю стенку дурального мешка, в 9,8% (20 чел.) отмечалось нарушение ликвородинамики. Поясничный стеноз был выявлен в 22,9% (47 чел.) случаев.
При сопоставлении клинической картины с результатами МР-томографии, в 88,3% (181 чел.) случаев было выявлено соответствие уровня локализации и направления выпячивания с уровнем выявленной радикулопатии, что говорит о высокой чувствительности данного метода обследования. В остальных случаях локализация протрузии или грыжи не соответствовала стороне и уровню радикулопатии. К примеру, у больного З. были выявлены задние срединные протрузии дисков L1-L2 и L2-L3 размером 3 и 3,5 мм, без признаков компрессии дурального мешка, а клинически и по результатам ЭНМГ определялась двусторонняя радикулопатия L5, S1 c вторичным аксонально-демиелинизирующим поражением обоих большеберцовых нервов. Результаты ЭНМГ представлены в таблице 3.
Таблица 3
ЭНМГ - феномен Точки стимуляции ОГ, M±m ГС, M±m Конт роль, M±m % восстановлени я, ОГ / ГС До лечения После лечения До лечения После лечения Амплитуда М-ответа, мВ Большеберцов ый нерв 3,75±0, 44 4,12± 0,25* 3,71± 0,4 3,8± 0,69 5,78± 1,2 8,9/2,6 Малоберцовы й нерв 2,78± 0,65 3,5± 0,49* 2,87± 0,42 2,99± 0,47 5,65± 1,05 20,4/3,7 5 Латентность F-волны, мс Большеберцов ый нерв 44,01± 3,86 33,65± 8,2* 43,89± 3,54 42,04± 3,87 37,0± 3,9 23,5/4,2 Малоберцовы й нерв 44,14± 3,93 37,77± 5,2* 44,2± 3,85 41,99± 3,15 34,8± 3,1 14,4/5 СПИ по двигательным Большеберцов ый нерв 29,3± 4,1 35,1± 2,2* 29,9± 5,1 32,6± 4,9 47,8± 6,1 16,5/8,3 Малоберцовы й нерв 30,1± 4,8 36±4,1 * 31,1± 4,6 33,05± 3,9 42,3± 5,1 17,1/5,9 Примечание: * - статистически достоверная разница между показателями у пациентов до и после лечения, р<0,05.По результатам ЭНМГ, в обеих группах до лечения отмечались достоверные (р<0,05), по сравнению с контрольной группой, изменения амплитудно-скоростных показателей и увеличение латентности F-волны, что свидетельствует об аксонально-демиелинизирующем процессе как в проксимальном, так и в дистальном участке ветвей пояснично-крестцового
Динамика показателей ЭНМГ больных ПКР сплетения. В результате проведенного лечения в ОГ зафиксировано достоверное (р<0,05), по сравнению с ГС, увеличение амплитуды М-ответа, уменьшение латентности F-волны, увеличение скорости проведения импульса (СПИ). Особенно заметно (в 2-4 раза по сравнению с ГС) восстановилась амплитуда М-ответа и уменьшилась латентность F-волны, примерно в 2 раза возросла СПИ по двигательным волокнам. Это свидетельствует о возможном частичном или полном восстановлении аксонального транспорта и ускорении ремиелинизации поврежденных нервных волокон. Этим объясняется более быстрый регресс неврологической симптоматики в ОГ, нежели в ГС. Хотя значения исследованных параметров и не достигли результатов контрольной группы, они соответствуют нижним границам нормы, описанным в литературе.
Части больным (45 чел.) обеих групп (25 из ОГ и 20 из ГС) проводилось исследование антител (АТ) к миелопероксидазе (МПО) в сыворотке крови методом ИФА в динамике. При мониторинге терморегуляции и дополнительных биохимических исследованиях у данной группы больных было отмечено отсутствие повышения температуры тела, эритематозных кожных высыпаний, полиорганной симптоматики, повышения уровня сиаловых кислот, фибриногена, наличия С-реактивного белка, ускорения СОЭ и воспалительных изменений в лейкоцитарной формуле. АТ к МПО у 15 человек контрольной группы (практически здоровые люди) составил 0,8±0,02 ед. ОП (единиц оптической плотности), до лечения в исследуемых группах 5,5±0,28 ед. ОП в ОГ и 5,1± 0,31 ед. ОП в ГС. После проведенной терапии показатели АТ к МПО составили в ОГ 3,2±0,24 ед. ОП, в ГС -4,3±0,52 ед. ОП (рис.3).
Рисунок 3.
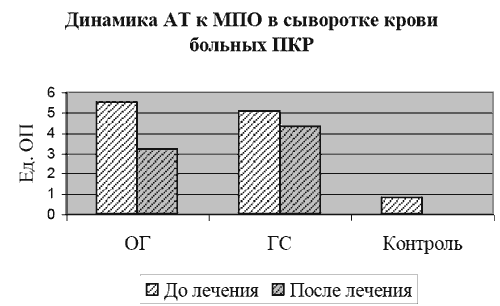
Хотя в ОГ отмечена достоверная (p<0,05) положительная динамика, ни в одной из групп показатели АТ к МПО не достигли значений контрольной группы. Это может свидетельствовать о продолжающемся, не смотря на значительное клиническое улучшение, воздействии патогенетических иммунных механизмов, недостаточности механизмов саногенеза и, как следствие, хроническое течение заболевания. Этим же больным исследовали АТ к коллагену в сыворотке крови с помощью реакции преципитации (РП). В контрольной группе данный вид АТ обнаруживался в титре 1:10 в 13,3% (2 чел.) случаев, у остальных - отрицательный результат. Значения АТ к коллагену представлены в таблице 4.
Таблица 4. Распределение больных в группах по титрам обнаруженных АТ к коллагену
Титры АТ к коллагену ОГ (до / после лечения), n=25 ГС (до / после лечения), n=20 Абсолютное кол-во, чел. % Абсолютное кол-во, чел. % 1:10 1 / 4 4 / 16 1 / 1 5 / 5 1:20 7 / 10 28 / 40 4 / 4 20 / 20 1:40 1 / 3 4 / 12 2 / 3 10 / 15 1:80 1 / 2 4 / 8 0 / 2 0 / 10 1:160 4 / 2 16 / 8 2 / 2 10 / 10 1:320 2 / 2 8 / 8 3 / 1 15 / 5 1:640 5 / 2 20 / 8 4 / 4 20 / 20 1:1280 4 / 0 16 / 0 4 / 3 20 / 15 Согласно данным таблицы, в обеих группах отмечается уменьшение под влиянием терапии АТ к коллагену, однако в ОГ мы видим более значительное уменьшение количества определяемых АТ, они в основном определяются при небольшом разведении. При этом в ГС сохраняется достаточно интенсивная их продукция, практически сохраняется количество больших разведений, где они определяются. Анализируя полученные результаты по определению АТ к МПО и коллагену, можно сделать заключение, что сроки наступления иммунологической ремиссии при ПКР не соответствуют срокам клинической ремиссии, то есть больные нуждаются в продолжении комплексной терапии, включающей мексидол в таблетированной форме (по 0,5 (2 таблетки) 3 раза в сутки в течение 6-8 недель) на амбулаторном этапе.
Выводы:
Результатами проведенного исследования доказано превосходство комплексного лечения ПКР с применением мексидола по сравнению с традиционными методиками. Выявлено положительное влияние цитопротекторной антигипоксической терапии на скорость ремиелинизации нервных волокон. Обнаруженная продукция аутоантител к МПО и коллагену при ПКР свидетельствует не о локальном, а о системном процессе, затрагивающим сосудистую, костно-суставную (в данном случае позвоночник) системы организма. Мексидол при такой аутоагрессии обеспечивает (помимо трофической и антиоксидантной) иммунологическую защиту нервных клеток и их отростков от аутоантител и образовавшихся иммунных комплексов, чем объясняется значительный клинический эффект.
Библиография
1. Антонов И.П. Вопросы классификации и формулировка диагноза вертеброгенных (спондилогенных) заболеваний нервной системы / И.П. Антонов // Периферическая нервная система. - Минск. - 1983.-Вып.6.- С.49-56.
2. Бадалян Л.О. Клиническая электронейромиография: Руководство для врачей / Л.О. Бадалян, И.А. Скворцов. - М.: Медицина, 1986. - 365с.
3. Байкушев С.Т. Стимуляционная электромиография и электронейрография в клинике нервных болезней / С.Т. Байкушев, З.Х. Манович, В.П. Новикова. - М.: Медицина, 1974. - 144с.
4. Белова А.Н. Шкалы, тесты и опросники в медицинской реабилитации / А.Н. Белова, О.Н. Щепетова. - М.: антидор, 2002г. - 440с.
5. Василенко А.М. Корреляции болевой чувствительности и гуморального иммунного ответа при термораздражении у мышей / А.М. Василенко, Л.А. Захарова, Е.Е. Метакса, О.Г. Яновский // Бюллетень экспериментальной биологии и медицины. - 1995. - Т.119, №4. - С. 405-409.
6. Веселовский В.П. Клиническая классификация вертеброневрологических синдромов / В.П. Веселовский, А.П. Ладыгин, О.С. Кочергина // Неврологический вестник. - 1995. - Т. XXVII, вып. 3-4. - С.45-50.
7. Воронина Т.А. Механизм действия и обоснование применения препарата мексидол в неврологии / Т.А. Воронина, Л.Д. Смирнов, И.И. Горейнова // Научно-практическая конференция по неврологии. - М., 2000. - С. 2-4.
8. Герасимова М.М. Цитомедины в комплексной терапии пояснично-крестцовых радикулопатий. В кн.: Кортексин - пятилетний опыт отечественной неврологии /Под ред. А.А. Скоромца, М.М. Дьяконова. - СПб.: Наука, 2005. - С. 156-167.
9. Гланц С. Биомедицинская статистика. Перевод с англ. / С. Гланц. -1999. - 459 с.
10.Дривотинов Б.В. Роль аутоиммунных реакций в патогенезе рецидивов и ремиссий корешкового болевого синдрома при поясничном остеохондрозе / Б.В. Дривотинов, В.М. Ходосовская // Периферическая нервная система. - Минск. - 1978. - Вып.1. - С.62-67.
11. Жулев Н.М. Остеохондроз позвоночника: Руководство для врачей / Н.М. Жулев, Ю.Д. Бадзгарадзе, С.Н. Жулев. - С-Пб.: Издательство "Лань", 2001. - 592 с.
12. Заславский Е.С. Болевые мышечно-дистрофические синдромы (этиология, патогенез, клиника, лечение): Автореф. дисс... докт. мед. наук / Е.С. Заславский. - М. - 1980. -34 с.
13. Клюшник Т.П. Аутоантитела к фактору роста нервов при нервно-психических заболеваниях и нарушениях развития нервной системы Автореф. дисс... докт. мед. наук М., 1997
14. Коган О.Г. Иммунопатологические аспекты остеохондроза позвоночника и его неврологических синдромов / О.Г. Коган // Проблемы аутоаллергии. - Таллин. - 1975. - С. 224-225.
15. Крыжановский Г.Н. Общая патофизиология нервной системы: Руководство / Г.Н. Крыжановский. - М.: Медицина, 1997 - 352 с.
16. Сороковиков В.А. Хирургическое лечение дискогенного пояснично-крестцового радикулита с иммунокоррекцией: Автореф. дисс. . канд. мед. наук / В.А. Соровиков. - Иркутск. - 1995. - 24 с.
17. Применение мексидола при дискогенных радикулопатиях / Н.В. Бабенков, В.А. Халецкая, Л.Б. Клачкова, Т.С. Ваулина // Кремлевская медицина: Клинический вестник. - 2001. - №2. - С.59-62.
18. Brunner C., Lassman H., Waehneldt T.V. Differential ultrastructural localization of myelin basic protein, myelin - oligodendroglial glicoprotein and 2,3-cyclic nucleotid 3- phosphodiesterase in the CNS of adult rats / C. Brunner, H. Lassman, T.V. Waehneldt et al.// Neurochem. - 1989. - Vol.52. - P. 296-304.
19. Giles L.G.F. Innervation of spinal structures. In: Clinical anatomy and management of low back pain / Ed. Giles L.G.F. - Oxford, Butterworth- Heinemann, 1997. - P.219-231.
20. Ochoa J. Histopathology of common mononeuropathies. In: Nerve Repair and Regeneration / Edited by D.L. Jewett, H.R. McCarroll, Jr.- St. Louis, C.V. Mosby. - 1980. - P. 36-52.
21. Ross J. S., Masaryk T. J., Schrader M. et al. MR imaging of the postoperative lumbar spine: assessment with gadopentetate dimeglumine // Amer. J. Roentgenol. - 1990. - Vol. 155. - P. 867-872.
22. Rydevik В. Effects of graded compression on intraneural blood flow - an in vivo study on rabbit tibial nerve / В. Rydevik, G. Lundborg, U. Bagge // J. Hand. Surg. - 1981. - Vol.6. - P.3-12.
23. Wilder R.L. Neuroendocrine-immune system interactions and autoimmunity / R.L. Wilder // Ann. Rev. Immunol. - 1995. - V.13. - P.307-338.
| Июнь 2008 г. |