Опубликовано в журнале:
Кардиоваскулярная терапия и профилактика, 2009; 8(4)Сравнение рекомендованных доз блокаторов рецепторов ангиотензина и ингибиторов ангиотензин-превращающего фермента (исследование CORD)
J. Spinar*, J. Vitovec, M. Soucek, L. Dusek, T. Pavlik для исследования CORD
Медицинский Факультет Университета Масарика. Брно, Чешская РеспубликаComparing recommended doses of angiotensin receptor blockers and ACE inhibitors (CORD Study)
J. Spinar*, J. Vitovec, M. Soucek, L. Dusek, T. Pavlik for CORD Study
Masarik University, Medical Faculty. Brno, the Czech RepublicЦель. В исследовании CORD оценивались эффективность и переносимость лозартана и рамиприла у пациентов с артериальной гипертонией (АГ).
Материал и методы. В исследовании участвовали две группы: В группе A больных переводили с лечения ингибиторами ангиотензин-превращающего фермента (ИАПФ) на лозартан; участвовали 4016 больных с АД < 160/100 мм рт.ст., принимавших различные ИАПФ в течение > 3 мес.; средний возраст пациентов - 62,6±11,6 лет; 53,1% этой выборки составляли женщины. АД, частота сердечных сокращений, биохимические показатели, общий анализ крови и ЭКГ контролировались в первый день и затем через 1, 3, 6 и 12 мес. В группе B сравнивались эффективность и переносимость лозартана и рамиприла. В эту группу вошли 3813 больных с АД ≥ 140/90 мм рт.ст., ранее не принимавших блокаторы рецепторов ангиотензина (БРА) или ИАПФ; средний возраст пациентов - 60,5±12,2 лет; 50,5% из них были женщины. Пациенты случайным образом разделены на группы лечения лозартаном 50 мг/сут. (n=1887) или рамиприлом 5 мг/ сут. (n=1926).
Результаты. Через 1 мес. лечения в группе А понизилось АД со 147,4±14,8/87,7±9,3 мм рт.ст. до 139,7±11,8/83,0+9,3 мм рт.ст. (p<0,001), а через 1 год - до 133,7±11,3/79,1±7,06 мм рт.ст. (p<0,001). Частота развития побочных эффектов не увеличилась. Через 1 год в группе В, подгруппе лозартана АД снизилось со 156,5±13,1/93,4±8,8 до 134,55±11,3/80,16±6,6 мм рт.ст. (p<0,001), а в подгруппе рамиприла - со 155,9±13,1/93,0±8,9 мм рт.ст. до 134,1±11,2/81,5±6,8 мм рт.ст. (p<0,001). Серьезных побочных эффектов не наблюдалось, но в подгруппе рамиприла сухой кашель появился в 8 раз чаще.
Заключение. Переход с терапии ИАПФ на лозартан безопасен и эффективен. Лозартан и рамиприл обладают равной антигипертензивной эффективностью и тенденцией к улучшению метаболических показателей; терапия лозартаном переносилась значительно лучше по сравнению с рамиприлом.
Ключевые слова: артериальная гипертензия, изолированная систолическая гипертензия, рамиприл, лозартан, метаболические параметры, кашель.
Aim. The CORD Study compared effectiveness and tolerability of losartan and ramipril in patients with arterial hypertension (AH).
Material and methods. The study included two groups, A and B. In Group A (n=4016; mean age 62,6±11,6 years; 53,1% women), the patients with blood pressure (BP) <160/100 mm Hg and ACE inhibitor therapy lasting for >3 months were switched from ACE inhibitors to losartan. At baseline and 1, 3, 6, and 12 months later, BP, heart rate, and biochemical parameters were measured; general blood assay and electrocardiography (ECG) were also performed. In group B (n=3813; mean age 60,5±12,2 years; 50,5% women), the patients with BP ≥140/90 mm Hg and no previous ACE inhibitor or angiotensin receptor blocker (ARB) therapy were randomly administered either losartan (50 mg/d; n=1887) or ramipril (5 mg/d; n=1926).
Results. Group A demonstrated a decrease in BP - from 147,4±14,8/87,7±9,3 to 139,7±11,8/83,0±9,3 mm Hg (p<0,001) after one month of the treatment, and to 133,7±11,3/79,1±7,06 mm Hg (p<0,001) after one year. Adverse effect prevalence did not increase. After one year, Group B demonstrated a reduction in BP levels - in losartan subgroup, from 156,5±13,1/93,4±8,8 to 134,55±11,3/80,16±6,6 mm Hg (p<0,001), and in ramipril subgroup - from 155,9±13,1/93,0±8,9 to 134,1±11,2/81,5±6,8 mm Hg (p<0,001). No severe adverse effects were registered, but in ramipril subgroup, cough was 8 times more prevalent.
Conclusion. ACE inhibitor substitution with losartan was safe and effective. Losartan and ramipril demonstrated equal antihypertensive effectiveness and a tendency to improve metabolic parameters. Losartan therapy was better tolerated than ramipril.
Key words: Arterial hypertension, isolated systolic hypertension, ramipril, losartan, metabolic parameters, cough.
Препараты, блокирующие ренин-ангиотензин-альдостероновую систему (РААС), являются предпочтительными в лечении артериальной гипертензии (АГ), особенно осложненной наличием ассоциированных клинических состояний (АКС) [1]. Они показаны пациентам с АГ и сахарным диабетом (СД), метаболическим синдромом (МС), ишемической болезнью сердца (ИБС), с сердечной недостаточностью (СН) и пароксизмальной мерцательной аритмией, а также молодым пациентам с неосложненной АГ. В ряде клинических исследований было продемонстрировано благоприятное влияние этих препаратов не только для контроля артериального давления (АД), но также для снижения частоты развития новых случаев СД. В них сравнивали блокаторы рецепторов ангиотензина (БРА) и ингибиторы ангиотензин-превращающего фермента (ИАПФ) с β-адреноблокаторами (β-АБ) и/или диуретиками (Д) [2-4], а также с блокаторами кальциевых каналов (АК) [5,6]. Рандомизированные, контролируемые исследования с участием - 150 тыс. пациентов, убедительно показали, что ИАПФ уменьшают смертность и частоту инфарктов миокарда (ИМ), инсульта (МИ) и СН у пациентов с СН, дисфункцией левого желудочка (ЛЖ) и предшествующими сердечно-сосудистыми заболеваниями (ССЗ) или с СД [7-12]. Проведено прямое сравнение БРА и ИАПФ у пациентов с хронической СН, перенесших ИМ и со стабильной ИБС [13-18]. Результаты этих исследований свидетельствуют о том, что эти два класса препаратов одинаково эффективны. Наблюдается равная антигипертензивная эффективность лозартана 50 мг один раз в сут. и каптоприла 25 мг 3 раза в сут., а также их способность к уменьшению ремоделирования ЛЖ у пациентов, перенесших ИМ [19-20].
CORD (COmparison of Recommended Doses) - многоцентровое, проспективное, сравнительное, рандомизированное исследование у пациентов с АГ (лечение назначалось по дате рождения), в котором тестировались две гипотезы:
- Переход с терапии ИАПФ на лозартан у пациентов, принимающих ИАПФ в течение > 3 мес., безопасен и не сопровождается развитием побочных эффектов или повышением АД (группа A).
- Назначение лозартана или рамиприла в эквивалентных дозах для лечения плохо контролируемой АГ приведет к одинаковому снижению АД с одинаковой частотой побочных эффектов (группа B).Материал и методы
Дизайн исследования:
В исследование CORD в группу A были включены пациенты, принимавшие различные ИАПФ по поводу АГ степеней (ст.) в течение > 3 мес., и уровнем АД < 160/100 мм рт.ст. Нижней границы уровня АД при включении пациентов в группу А не существовало. Пациентов с любым документированным сердечно-сосудистым событием за последние 3 мес. из исследования исключали. Допускалась сопутствующая терапия различными антигипертензивными препаратами (АГП), за исключением БРА.После подписания информированного согласия пациенты прекращали прием своего ИАПФ сразу же и на второй день начинали принимать лозартан (Лозап®, ЗЕНТИВА, Чешская Республика) в дозе 50 мг один раз в сутки. АД, частота сердечных сокращений (ЧСС), биохимические показатели, общий анализ крови и электрокардиограмма (ЭКГ) регистрировались в первый день, и затем через 1, 3, 6 и 12 мес. При необходимости дозу лозартана титровали, а также добавляли гидрохлортиазид (ГХТ), если АД было ≥ 140/90 мм рт.ст. (в группе А - 13, 7% больным) (рисунок 1).
Рис. 1 Дизайн исследования.
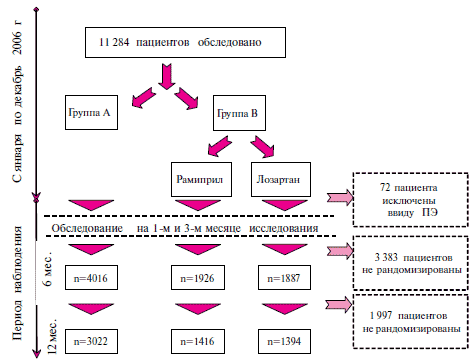 Примечание: ПЭ - побочные эффекты.
Примечание: ПЭ - побочные эффекты.В группу B включали пациентов с АД ≥ 140/90 мм рт.ст., если их состояние было стабильным в течение последних 3 мес., и они не принимали ранее БРА или ИАПФ. Любая другая антигипертензивная терапия (АГТ) допускалась.
Критериями исключения служили непереносимость ИАПФ, креатинин сыворотки > 250 ммоль/л или беременность.
Пациенты прошли рандомизацию, в основу которой была положена дата их рождения. После этого они получали терапию лозартаном (рожденные в четный день) или рамиприлом (рожденные в нечетный день) (рисунок 1). Рекомендуемые стартовые дозы препаратов составляли 50 мг/сут. для лозартана и 5 мг/сут. для рамиприла.
Добавление ГХТ к терапии лозартаном потребовалось у 21,1% больных; к терапии рамиприлом - у 27,7%. В процессе исследования у пациентов в группах А и В допускалась коррекция сопутствующей АГТ, но только не препаратами классов ИАПФ и БРА. Первичной конечной точкой являлось снижение или нормализация АД < 140/90 мм рт.ст., включая пациентов с СД и ИБС при условии отсутствия различий в сопутствующей терапии; вторичной конечной точкой - частота развития побочных эффектов как клинических, так и лабораторных. Она рассчитывалась как доля пациентов в процентах с отклонениями лабораторных параметров, в т.ч. показателей функции почек, метаболических параметров и калия.
Исследование CORD было выполнено в Чешской Республике. В нем участвовали 585 врачей. Скрининг начался в январе 2006г, а рандомизация продолжалась до декабря 2006г. Рандомизацию должны были пройти > 5 тыс. пациентов в группе лозартана [2]. Всего скрининг прошли 11284 человека; 7829 человек были рандомизированы. Данные 72 пациентов с серьезными побочными эффектами и преждевременно выключенные из исследования касались только начала исследования. Эти пациенты вошли в анализ побочных эффектов. Поскольку среди нерандомизированных пациентов были также такие, которые имели недостаточно исходных данных, они не могли быть включены в статистический анализ. По истечении 6 мес. лечения полные данные были получены у 4016 пациентов группы A и у 3813 пациентов группы B: 1887 в группе лозартана и 1926 в группе рамиприла. По истечении 12 мес. полная информация была по 3022 пациентам группы A и 2810 пациентам группы B: 1394 в группе лозартана и 1416 в группе рамиприла.
Статистический анализ.
Для анализа использовались средние значения показателей и их стандартные отклонения, а также таблицы частот. Снижение АД как первичная конечная точка оценивалось для разных групп больных с использованием парного критерия Стьюдента (t-критерий). Различия между группами лозартана и рамиприла по степени снижения АД оценивали при помощи t-критерия для двух независимых выборок. Оценка различий между группами по долям пациентов с нормализовавшимся АД проводилась при помощи точного критерия Фишера для таблиц сопряженности.
Этическое одобрение.
Исследование было одобрено многоцентровым этическим комитетом, а пациенты подписали информированное согласие перед тем, как принять участие в исследовании. Исследование контролировалось независимой мониторинговой компанией, Институтом биостатистического анализа Университета Масарика, Брно. Комитет безопасности был представлен членами Академического Совета медицинского факультета Университета Масарика, Брно, Чешская Республика. Исследование не имело спонсорской поддержки от каких-либо фармацевтических компаний; сбор данных проводился Институтом биостатистического анализа, медицинским факультетом Университета Масарика. Препараты выписывались обычным официальным способом, с учетом рекомендаций для применения.
Результаты
Исходные показатели пациентов с полным набором результатов после 6 мес. лечения представлены в таблице 1. Различий в сопутствующей АГТ между группами не было; 47,8% пациентов в группе A и 42,8% в группе B получали Д; 43,0% и 41,6% -β-АБ; 33,6% и 34,1% - АК (различия между лозартаном и рамиприлом недостоверны). Динамика АД представлена в таблицах 2 (сидя) и 3 (стоя). Снижения АД по сравнению с исходным через 6 и 12 мес. были высоко достоверными. Статистически достоверные различия в уровнях АД между лозартаном и рамиприлом в группе B отсутствовали. Снижение АД было достоверно больше в группе B, чем в группе A (p<0,001). Изменения степени тяжести АГ представлены в таблицах 4 и 5.
Taблица 1. Характеристика пациентов, включенных в исследование
Показатель Группа A - Лозартан
(n=4016)Группа B
(n=3813)Группа B - Рамиприл
(n=1926)Группа B - Лозартан
(n=1887)Общие показатели (М±SD) Возраст (лет) 62,6±11,6 60,5±12,2 60,4±12,5 60,6±11,8 Женский пол (%) 53,1 50,5 49,0 52,1 Вес (кг) 84,1±14,5 84,6±14,9 84,5±15,4 84,6±14,5 Рост (cм) 170,0±8,6 170,7±8,8 170,9±8,8 170,6±8,9 % положительных ответов Положительный семейный анамнез 67,0 66,7 67,8 65,5 Курильщик 20,3 23,3 23,0 23,5 Бывший курильщик 21,4 19,9 21,3 18,5 СД 33,0 29,3 28,6 30,1 Анамнез ИБС 30,3 25,4 26,7 24,1 Перенесенный ИМ 13,2 11,7 13,0 10,4 ДКМП 1,6 1,4 1,6 1,2 СН 7,1 5,7 6,0 5,3 Выявленная ДЛП 60,5 55,0 55,6 54,4 Выявленный кашель 34,5 6,8 5,3 8,4 Ошутствующая терапия (%) β-АБ 43,0 41,6 39,9 43,3 АК ДГП 28,3 28,4 29,7 27,0 АК неДГП 5,3 5,8 5,0 6,7 Мочегонные 47,8 42,8 41,6 44,0 Альфа-блокаторы 4,4 4,0 4,1 3,9 Аспирин 35,6 30,9 31,8 29,9 Клопидогрел 0,7 1,1 1,4 0,7 Варфарин 4,1 3,4 3,2 3,5 Статин 43,6 38,2 39,6 36,8 Нитрат 15,3 12,0 11,5 12,5 Пероральные сахароснижающие 15,3 12,0 20,0 20,8 Другие препараты 46,2 42,7 43,2 42,2 Примечание: ДГП - дигидропиридин; ДЛП - дислипидемия, ДКМП - дилатационная кардиомиопатия.Таблица 2. Динамика САД, ДАД и ЧСС за время исследования в положении сидя
Месяцы Группа A - лозартан
M ± SDГруппа B
M ± SDГруппа B - рами прил
M ± SDГруппа B - лозартан
M ± SDр-значение
Рамиприл vs, лозартанСАД (мм рт.ст.) 0 147,4±14,8 156,2±13,1 155,9±13,1 156,5±13,1 6 134,2±10,5 134,9±10,5 134,9±10,5 134,8±10,5 0,176 12 133,6±10,3 134,3±11,2 134,1±11,2 134,5±11,3 0,631 ДАД (мм рт.ст.) 0 87,7±9,3 93,2±8,8 93,0±8,9 93,4±8,8 6 79,9±6,4 80,5±6,5 80,3±6,5 80,6±6,5 0,883 12 79,0±6,5 79,7±6,8 79,3±6,9 80,1±6,6 0,359 ЧСС (уд/мин) 0 73,6±9,6 74,9±9,6 74,7±9,3 75,1±10,0 6 71,6±7,5 71,9±7,0 71,8±7,0 72,1±7,0 0,971 12 71,0±7,8 71,2±7,4 71,3±7,4 71,2±7,5 0,114 Taблица 3. Динамика САД, ДАД и ЧСС в положении стоя за время исследования
Месяцы Группа A - лозартан
M±SDГруппа B
M±SDГруппа B - рамиприл
M±SDГруппа B - лозартан
M±SDp-значение
Рамиприл vs, лозартанСАД (мм рт.ст.) 0 146,6±15,5 155,5±13,4 155,3±13,3 155,7±13,5 6 134,1±11,6 134,9±11,5 134,8±11,5 135,1±11,5 0,818 12 133,3±11,3 134,1±11,7 134,0±12,1 134,2±11,3 0,994 ДАД (мм рт.ст.) 0 87,2±9,5 92,5±8,9 92,5±9,0 92,5±8,8 6 79,9±7,1 80,4±7,2 80,3±7,2 80,6±7,2 0,528 12 79,1±7,0 79,7±7,3 79,4±7,4 80,0±7,2 0,209 ЧСС (уд/мин) 0 76,0±8,7 77,3±9,6 77,3±9,8 77,3±9,3 6 73,9±7,4 74,4±7,4 74,3±7,5 74,5±7,2 0,427 12 73,7±7,4 74,1±7,7 74,3±7,9 74,0±7,5 0,564 Таблица 4. Динамика степени тяжести АГ за 6 мес
Группа A - лозартан Группа B Группа B - рамиприл Группа B - лозартан От ИСАГ к нормальному АД (%) 15,9 13,4 14,2 12,6 От АГ к нормальному АД (%) 31,7 46,1 45,6 46,6 От АГ к ИСАГ (%) 14,4 21,8 21,2 22,3 Уменьшение ≥ 1 степени тяжести без достижения нормаль- ного АД 4,0 7,0 7,2 6,9 Без динамики (%) 34,0 11,7 12,8 11,6 Таблица 5. Динамика степени тяжести АГ за 12 мес
Группа A - лозартан Группа B Группа B - рамиприл Группа B- лозартан От ИСАГ к нормальному АД (%) 8,6 7,4 7,6 7,8 От АГ к нормальному АД (%) 39,8 53,8 54,7 53,0 От АГ к ИСАГ (%) 6,0 7,7 7,6 7,2 Уменьшение ≥ 1 степени тяжести без достижения нормального АД 9,4 15,8 15,3 16,2 Без динамики (%) 36,2 15,3 14,8 15,8 Через 6 мес. 64,2% пациентов в группе A и 59,5% в группе B достигли нормальной величины АД. Через 12 мес. у 64,5% пациентов группы A и у 61,2% группы B отмечен нормальный уровень АД. 59,1% пациентов на лозартане и 59,9% пациентов на рамиприле через 6 мес. имели нормальное АД (различия между группами недостоверны). У 60,5% пациентов на лозартане и 62,2% на рамиприле АД нормализовалось через 12 мес. (различия между группами недостоверны).
Динамика лабораторных показателей представлена в таблицах 6 и 7.
Таблица 6. Динамика клинических показателей через 12 мес (все нд)
Показатель Группа A Группа B Исходно 12 мес, Исходно 12 мес, ХС (ммоль/л) 5,44,4±0,4 5,2±0,8 5,5±1,0 5,2±0,8 Гликемия (ммоль/л) 5,9±1,6 5,7±1,4 5,9±1,7 5,7±1,4 TT (ммоль/л) 1,9±0,9 1,8±0,8 1,9±0,9 1,8±0,7 МК (ммоль/л) 322,8±82,9 319,3±74,8 323,1±84,6 319,5±78,2 Натрий (ммоль/л) 139,9±3,7 139,6±3,8 140,2±3,7 139,7±3,8 Калий (ммоль/л) 4,4±0,5 4,4±0,4 4,4±0,4 4,4±0,4 Креатинин (ммоль/л) 91,5±20,7 91,6±19,5 90,3±19,3 90,7±19,7 Мочевина (ммоль/л) 6,3±2,1 6,4±2,2 6,3±2,0 6,3±1,9 Эритроциты (106/л) 4,5±0,5 4,5±0,5 4,6±0,6 4,5±0,5 Гемоглобин (г/дл) 141,1±12,6 140,4±11,6 142,3±12,6 141,7±11,5 Гематокрит (%) 42,0±5,0 42,0±4,0 42,0±5,0 42,0±5,0 Таблица 7. Динамика клинических показателей через 12 мес (все нд)
Показатель Группа B - Исходно Рамиприл 12 мес. Группа B -Исходно Лозартан 12 мес. ХС (ммоль/л) 5,4±1,0 5,2±0,8 5,5±1,0 5,3±0,9 Гликемия (ммоль/л) 5,9±1,8 5,7±1,3 5,8±1,6 5,7±1,5 ТГ (ммоль/л) 1,9±0,9 1,8±0,7 1,9±0,9 1,8±0,7 МК (ммоль/л) 324,8±81,4 320,0±76,5 321,4±87,7 318,9±79,9 Натрий (ммоль/л) 140,4±3,7 169,7±3,9 140,1±3,7 139,7±3,8 Калий (ммоль/л) 4,4±0,5 4,4±0,4 4,4±0,4 4,4±0,4 Креатинин (ммоль/л) 89,5±18,5 90,2±18,4 91,1±20,1 91,2±20,2 Мочевина (ммоль/л) 6,3±1,9 6,4±1,9 6,3±2,0 6,3±2,0 Эритроциты (106/л) 4,6±0,6 4,5±0,5 4,6±0,5 4,6±0,5 Гемоглобин (г/дл) 142,6±12,5 141,9±11,5 142,0±12,6 141,5±11,5 Гематокрит (%) 42,0±4,0 42,0±4,0 42,0±5,0 42,0±5,0 Серьезные побочные эффекты приведены в таблице 8. Частота развития побочных эффектов < 1%, за исключением кашля в группе рамиприла. 72 человека выбыли из исследования в связи с развитием побочных эффектов: 25 в группе A и 47 в группе B: 14 из группы лозартана и 34 из группы рамиприла. У 21 (1%) пациента, принимавшего рамиприл, причиной отмены терапии стал сухой кашель.
Таблица 8. Серьезные побочные эффекты (n)
Смерть ИМ МИт Новые случаи СД Кашель Группа A - Лозартан 6 7 14 9 3 Группа B 9 7 17 11 37 Группа B - Рамиприл 4 4 8 6 33 (2%) Группа B - Лозартан 5 3 9 5 4 Обсуждение
Убедительно доказано, что ИАПФ уменьшают смертность, частоту ИМ, МИ, СН и реваскуляризации у пациентов с ССЗ и СД с высоким риском осложнений [12,21,22]. БРА и ИАПФ снижают риск развития МИ и новых случаев СД у больных АГ [2-4,23,24]. Поэтому, для получения клинически значимой информации исследования, оценивающие эффективность БРА у пациентов с АГ, должны включать ИАПФ в эквивалентных дозах в качестве сравнения [18,19]. Была проверена гипотеза о том, что лозартан не уступает по результату ИАПФ в двух разных ситуациях. В исследовании CORD в группе A больные были переключены с приема ИАПФ в стандартных дозах на прием лозартана. Гипотеза нашла подтверждение, т. к. было доказано, что такая смена терапии не сопровождается развитием новых побочных эффектов, ухудшением функции почек или гипотонией.
АД в ходе исследования CORD в группе A снизилось, вероятно, за счет эффекта "исследования". Недавно был представлен мета-анализ клинических работ, сравнивающих новый ингибитор ренина алискирен с плацебо у 3500 пациентов. В нем показано, что при приеме плацебо АД снизилось на 6,2/5,9 мм рт.ст., и это снижение было более выраженным у пациентов > 65 лет, которые составляли треть выборки [25].
В группе B оценивались антигипертензивная эффективность, безопасность и переносимость лозартана и рамиприла у пациентов с легкой или умеренной АГ, ранее не леченных или принимавших другие классы АГП, кроме блокаторов РААС: ИАПФ, БРА, блокаторы альдостерона или прямые ингибиторы ренина. Лечение начинали с низких или средних доз выбранных препаратов с последующим увеличением, если не удавалось нормализовать АД. Антигипертензивная эффективность двух препаратов была одинаковой и обеспечила снижение АД на - 15% от исходного уровня. Это очень близко к результатам, полученным в исследованиях LIFE (Losartan Intervention For Endpoint reduction in hypertension) и ASCOT (Anglo-Scandinavian Cardiac Outcomes Trial), где оно было чуть больше и составляло 16-17%, вероятно, за счет более широкого использования комбинированной терапии. Не было обнаружено различий между лозартаном и рамиприлом, что подтвердило результаты исследований ONTARGET (Ongoing Telmisartan Alone and in combination with Ramipril Global Endpoint Trial) или VALIANT (Val sartan in Acute Myocardial Infarction Trial) [2-4,17,18].
К окончанию исследования CORD в группе B примерно две трети пациентов достигли нормальной величины АД: 60,2% лозартан, 62,2% рамиприл; у - 10% сохранялась АГ с уровнем АД > 140/90 мм рт.ст.: 11,9% лозартан, 10,1% рамиприл; примерно у четверти пациентов зарегистрирована изолированная систолическая АГ (ИСАГ): 27,3% лозартан, 27,2% рамиприл. Количество пациентов с ИСАГ в подгруппе лозартана увеличилось с 18,6% до 27,3%, а в подгруппе рамиприла - с 22,6% до 27,2%. Это свидетельствует о переходе АГ из I-II степеней в ИСАГ. В литературе уже есть ссылки, как трудно достичь уровня систолического АД (САД) < 140 мм рт.ст. (130 мм рт.ст. у пациентов с СД), даже если диастолическое АД (ДАД) < 90 мм рт.ст. (80 мм рт.ст. у пациентов с СД) [26]. Во многих крупных клинических исследованиях, таких как HOT (Hypertension Optimal Treatment Study), UKPDS (UK Prospective Diabetes Study), INSIGHT (International Nifedipine GITS Study Intervention as a Goal in Hypertension Treatment), VALUE (Valsartan Antihypertensive Long-term Use Evaluation) и STOP-Hypertension 2 (Swedish Trial in Old Patients with Hypertension 2), большинство пациентов достигали конечной точки - ДАД < 90 мм рт.ст., но при этом их САД оставалось > 140 мм рт.ст., таким образом переходя в ИСАГ. В исследовании LIFE 89% пациентов достигли ДАД < 90 мм рт.ст., но только 46% больных достигли уровня САД < 140 мм рт.ст. В настоящем исследовании у 22,3% в группе лозартана и у 21,2% человек в группе рамиприла развилась ИСАГ. Но даже у таких пациентов удалось добиться снижения САД более чем на 10%, что является показателем определенного успеха. Ни у кого из пациентов со сниженным ДАД не было сопутствующего повышения САД, что являлось бы маркером ухудшения прогноза [27,28]. Через 12 мес. лечения пульсовое АД (ПАД) в группе лозартана снизилось на 9,0 мм рт.ст. - с 63,2 до 54,2 мм рт.ст. и на 8,2 мм рт.ст. - с 62,8 до 54,6 мм рт.ст. в группе рамиприла, что свидетельствует об улучшении прогноза для пациентов [29]. Тем не менее, последующие исследования по лечению АГ должны быть сосредоточены на улучшении контроля САД [1,30].
АГ является компонентом МС по всем его определениям [1]. Оптимальный АГП должен обеспечивать контроль АД, обладать положительными метаболическими эффектами и минимальным количеством побочных действий. В исследованиях LIFE, ASCOT и VALUE описано снижение частоты развития новых случаев СД у пациентов, принимавших БРА или ИАПФ, по сравнению с β-АБ или АК. В этой работе также наблюдали улучшение по всем метаболическим показателям - гликемии, содержанию холестерина (ХС), триглицеридов (ТГ) и мочевой кислоты (МК), что подтверждает точку зрения об улучшении метаболической чувствительности при блокаде РААС, высказанную в других исследованиях. Также не было отмечено увеличения случаев почечной недостаточности или клинически значимого повышения уровня калия в крови, что подтверждают результаты исследования ONTARGET, где монотерапия сопровождалась менее чем на 1,0% снижением функции почек.
Мета-анализ АГТ показал одинаковое АД-зависимое влияние БРА и ИАПФ в отношении риска возникновения МИ, ИБС и СН, а также независимое от уровня АД влияние на риск крупных коронарных событий ИАПФ, но не БРА [31]. В настоящее время отсутствует подтверждение независимого от АД влияния на частоту ИМ, что созвучно результатам исследования ONTARGET, где частота ИМ составляла 4,8% для рамиприла и 5,2% для телмисартана. В этой работе частота развития ИМ, МИ или смерти оказалась очень низкой, что, возможно, связано с небольшой продолжительностью наблюдения.
По данным многих исследований самым частым побочным эффектом у пациентов, принимающих ИАПФ, является кашель [7,8,11,13, 16,17]. В исследовании частота развития кашля оказалась в 8 раз выше при приеме рамиприла, чем лозартана. Пациентов специально не расспрашивали о наличии кашля, поэтому частота развития = 2% соответствует спонтанным сообщениям о кашле, существенно влияющем на качество жизни (КЖ). 21 (1%) пациент в группе рамиприла и ни одного в группе лозартана прекратили лечение из-за развития кашля. БРА и иАПФ считаются АГП, обладающими высокой степенью приверженности пациентов к их приему [32]. Настоящая работа позволяет считать, что это утверждение верно: частота выбытия из исследования из-за развившихся побочных эффектов оказалась небольшой, а переносимость лечения отмечена как хорошая.
Наблюдали небольшое уменьшение ЧСС на 2-3 уд/мин, что согласуется с ранее опубликованными данными, такими как исследование LIFE, где снижение ЧСС в группе лозартана составило 1,9 уд/мин.
Заключение
Исследование CORD - самое большое клиническое исследование, в котором сравнивается антигипертензивная эффективность БРА и ИАПФ; оно подтвердило, что терапия этими препаратами является безопасной, эффективной и хорошо переносимой.
Исследование CORD показало, что перевод пациентов с ИАПФ на лозартан эффективен и безопасен; БРА и ИАПФ обладают равной антигипертензивной эффективностью.
Еще раз было продемонстрировано, что гораздо легче добиться контроля ДАД, чем САД. Лечение переводит пациентов из разряда комбинированной систоло-диастолической АГ в разряд умеренной ИСАГ при снижении ПАД, что можно оценивать как положительный результат контроля АД.
Отмечены нейтральное влияние лозартана и рамиприла на ряд метаболических параметров, отсутствие неблагоприятного эффекта на функцию почек и большую частоту кашля при приеме рамиприла.
Лозартан и рамиприл являются эффективными препаратами первого выбора для лечения пациентов с АГ, особенно в сочетании с МС, СД, микроальбуминурией, гипертрофией миокарда левого желудочка и ИБС. При этом лечение лозартаном сопровождается меньшим количеством побочных эффектов, т. е. лучшей переносимостью по сравнению с рамиприлом.
Литература
1. Task Force Members 2007. Guidelines for the management of arterial hypertension. J Hypertens 2007; 25: 1105-87.
2. Dahlof B, Devereux RB, Kjeldsen SE, for the LIFE investigators. Cardiovascular morbidity and mortality in the Losartan Intervention For Endpoints reduction in hypertension study (LIFE): a randomised trial against atenolol. Lancet 2002; 359: 995-1003.
3. Dahlof B for the ASCOT investigators. Prevention of coronary stroke events with atorvastatin in hypertensive patients who have average or lower-than-average cholesterol concentrations, in the Anglo-Scandinavian Cardiac Outcomes Trial-Lipid Lowering Arm (ASCOT-LLA): a multicenter randomised controlled trial. Lancet 2003; 361: 1149-58.
4. Poulter NR for the ASCOT investigators. Role of blood pressure and other variables in the differential cardiovascular event rate noted in the Anglo-Scandinavian Cardiac Outcomes Trial-Blood Pressure Lowering Arm (ASCOT^LA). Lancet 2005; 366: 907-13.
5. Julius S, Kjeldsen SE, Weber M, et al. Outcomes in hypertensive patients at high cardiovascular risk treated with regimens based on valsartan or amlodipine: the VALUE randomised trial. Lancet 2004; 363: 2022-31.
6. The ALLHAT Officers and Coordinators for the ALLHAT Collaborative Research Group. Major outcomes in high-risk hypertensive patients randomised to angiotensin-converting enzyme inhibitor or calcium channel blocker vs diuretic; the Antihypertensive and Lipid Lowering Treatment to Prevent Heart Attack Trial (ALLHAT). JAMA 2002; 288: 2981-97.
7. The SOLVD investigators. Effect of enalapril on survival in patients with reduced left ventricular ejection fractions and heart failure. N Engl J Med 1991; 325: 293-302.
8. Pfeffer MA, Braunwald E, Moye LA, et al. Effect of captopril on mortality and morbidity in patients with left ventricular dysfunction after myocardial infarction: results of the Survival and Ventricular Enlargement study. N Engl J Med 1992; 327: 66977.
9. Flather MD, Yusuf S, Kober L, et al. Long term ACE-inhibitor therapy in patients with heart failure or left-ventricular dysfunction: a systematic overview of data from individual patients. Lancet 2000; 355: 1575-81.
10. Pfeffer MA, Domanski M, Rosenberg Y, et al. Prevention of events with angiotensin-converting enzyme inhibition (the PEACE study design). Prevention of Events with Angiotensin-Converting Enzyme Inhibition. Am J Cardiol 1998; 82: 25H-30.
11. Pitt B. ACE inhibitors for patients with vascular disease without left ventricular dysfunction - may they rest in peace? N Engl J Med 2004; 351: 2115-7.
12. Yusuf S, Sleight P, Pogue J, et al. The Heart Outcomes Prevention Evaluation Study Investigators. Effects of an angiotensin-converting-enzyme inhibitor, ramipril, on cardiovascular events in high-risk patients. N Engl J Med 2000; 342: 145-53.
13. Pitt B, Segal R, Martinez FA, et al. Randomized trial of losartan versus captopril in patients over 65 with heart failure (Evaluation of Losartan in the Elderly study, ELITE). Lancet 1997; 349: 74752.
14. Pitt B, Poole-Wilson PA, Segal R, et al. Effect of losartan compared with captopril on mortality in patients with symptomatic heart failure: randomized trial: the Losartan Heart Failure Survival Study ELITE II. Lancet 2000; 355: 1582-7.
15. Valsartan Heart Failure Trial Investigators. A randomized trial of the angiotensin-receptor blocker valsartan in chronic heart failure. New Engl J Med 2001; 345: 1667-75.
16. Dickstein K, Kjekshus J and the OPTIMAAL Study Group. Effects of losartan and captopril on mortality and morbidity in high-risk patients after acute myocardial infarction: the OPTIMAAL randomised trial. Lancet 2002; 360: 752-60.
17. Pfeffer MA, McMurray JJV, Velazquez EJ for the VALIANT Investigators. Valsartan, captopril, or both in myocardial infarction complicated by heart failure, left ventricular dysfunction, or both. N Engl J Med 2003; 349: 1893-906.
18. The ONTARGET investigators. Telmisartan, ramipril, or both in patients at high risk for vascular events. N Engl J Med 2008; 358: 1547-59.
19. Spinar J, Vitovec J, Spinarova L, et al. A comparison of intervention with losartan or captopril in acute myocardial infarction. Eur J Heart Failure 2000; 2(1): 91-100.
20. Spinar J, Vitovec J, Pluhacek L, et al. First dose hypotension after angiotensin converting enzyme inhibitor captopril and angiotensin II blocker losartan in patients with acute myocardial infarction. Int J Cardiol 2000; 75: 197-204.
21. The EURopean trial On reduction of cardiac events with Perindopril in stable coronary Artery disease investigators. Efficacy of perindopril in reduction of cardiovascular events among patients with stable coronary artery disease: randomised, double-blind, placebo-controlled, multicenter trial (the EUROPA study). Lancet 2003; 362: 782-8.
22. Pepine CJ for the INVEST Investigators. INVEST: International Verapamil SR/ Trandolapril Study. JAMA 2003; 290: 2805-16.
23. Nissen SE, Tuzcu EM, Libby P, for the CAMELOT investigators. CAMELOT (Effect of antihypertensive agents on cardiovascular events in patients with coronary disease and normal blood pressure). JAMA 2004; 292: 2217-26.
24. Bakris G, Molitch M, Hewkin A, et al. Differences in glucose tolerance between fixed-dose antihypertensive drug combinations in people with metabolic syndrome. Diabetes Care 2006; 29: 2592-7.
25. Dahlof B, Anderson DR, Arora V, et al. Aliskiren, a direct renin inhibitor, provides antihypertensive efficacy and excellent toler-ability independent of age or gender in patients with hypertension. J Clin Hypertens 2007; 9 Suppl A (5): A157, P-376.
26. Mancia G, Grassi G. Systolic and diastolic blood pressure control in hypertensive drug trials. J Hypertens 2002; 20: 1461-4.
27. Benetos A, Zurek M, Morcet J, et al. A decrease in diastolic blood pressure combined with an increase in systolic blood pressure is associated with a higher cardiovascular mortality in men. JACC 2000; 35: 673-80.
28. Waeber B. Targeting systolic blood pressure: the key to controlling combined systolic/diastolic hypertension. AHJ 2006; 19: 985-6.
29. Blacher J, Staessen JA, Girerd X, et al. Pulse pressure not mean pressure determines cardiovascular risk in elderly hypertensive patients. Arch Intern Med 2000; 160: 1085-9.
30. Staessen JA, Gasowski J, Wang JG, et al. Risk of untreated and treated isolated systolic hypertension in the elderly: meta-analysis of outcome trials. Lancet 2000; 355: 865-72.
31. Blood Pressure Lowering Treatment Trialists' Collaboration. Blood pressure-dependent and independent effects of agents that inhibit the renin-angiotensin system. J Hypertens 2007; 25(5): 951-8.
32. Veronesi M, Cicero AFG, Prandin МГ, et al. A prospective evaluation of persistence on antihypertensive treatment with different antihypertensive drugs in clinical practice. Vasc Health Risk Manag 2007; 3 (5): 1-7.
| Февраль 2010 г. |