Опубликовано в журнале:
Сердце Том 4 № 1
Выбор гипотензивной терапии для профилактики ишемической болезни сердца и других сердечнососудистых осложнений у больных с гипертрофией левого желудочка: сравнение тактики терапии, основанной на применении "новых" и "старых" лекарственных препаратов
С.Р. Гиляревский, РМАПО, Москва
Степень снижения артериального давления (АД) "представляется более важным фактором, определяющим клинический исход, по сравнению с выбором гипотензивного препарата". Так звучал один из выводов второго цикла мета-анализа, проведенного Объединением исследователей гипотензивной терапии в 2003 г. [1]. В целом в мета-анализ были включены данные более чем о 160 ООО больных, поэтому он представляет собой самый крупный анализ эффективности вмешательств при сердечно-сосудистых заболеваниях (ССЗ). Тем не менее можно ли, несмотря на большое число больных, данные о которых были включены в мета-анализ, считать его вывод универсальным? Применим ли он к больным с гипертрофией левого желудочка (ГЛЖ), наличие которой в 1,5-3,5 раза увеличивает риск развития ССЗ и 1,5-8,0 раз риск смерти? [2].
Давно существующее мнение о высокой эффективности низких доз тиазидных диуретиков для профилактики тяжелых ССЗ, в том числе и ишемической болезни сердца (ИБС), еще задолго до получения результатов исследования ALLH AT (Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial) [3] основывалось на данных мета-анализа плацебо-контролируемых исследований, включавших более 15 ООО больных [4-8]. Результаты мета-анализа плацебо-контролируемых исследований, включавших более 27 ООО больных послужили основанием для выводов об эффективности β-блокаторов [5, 9-14]. Однако следует отметить, что в соответствующих документах Администрации США по контролю за качеством пищевых продуктов и лекарственных препаратов [15] подчеркивается, что "безопасным медицинским продуктом может считаться такой, применение которого сопровождается приемлемым риском, позволяет получить достаточно выраженный ожидаемый положительный эффект и имеет доступные альтернативы". Это означает, что выпуск нового препарата предполагает тщательное количественное сравнение его эффективности с доступными альтернативными средствами (т.е. с уже имеющимися на рынке препаратами, применяемыми по тем же показаниям).
В действительности же при поступлении на рынок нового препарата существует мало данных о его сравнении с препаратами, уже применяемыми по тем же показаниям [16]. Положение о том, что "применение вмешательства, более эффективного, чем его отсутствие, лучше полного отсутствия лечения", основанное на результатах плацебо-контролируемых исследований, во многих случаях может служить лишь компромиссом. Часто оценка эффективности препарата сомнительна и основывается лишь на "статистически значимом отличии от плацебо" [17-21]. Все это ставит врача, выписывающего рецепт, перед весьма трудной задачей обоснованного выбора.
В течение последнего десятилетия предпринималось несколько попыток сравнить эффективность применения "новых" (антагонистов кальция и иАПФ) и "старых" (диуретиков и β-блокаторов) гипотензивных препаратов для профилактики ССЗ, включая ИБС [22-25]. При этом применение "новых" препаратов по сравнению со "старыми" не приводило к дополнительному снижению частоты развития как ИБС, так и других тяжелых ССЗ.
Лозартан стал первым гипотензивным препаратом, относящимся к "новым" средствам, преимущество которого перед β-блокатором было доказано в крупном рандомизированном клиническом исследовании (РКИ) LIFE (Losartan Intervention For Endpoint reduction in hypertension study) [26]. Напомним, что в целом в исследование LIFE были включены 9193 больных (возраст от 55 до 80 лет) с эссенциальной АГ (в положении сидя систолическое АД от 160 до 200 мм рт. ст. и диастолическое АД от 95 до 115 мм рт. ст.) и электрокардиографическими признаками ГЛЖ, которые затем получали либо лозартан, либо атенолол. Основным критерием оценки эффективности гипотензивной терапии был комбинированный показатель частоты развития инфаркта миокарда (ИМ), инсульта и смертности от ССЗ. Прием лозартана по сравнению с атенололом статистически значимо снижал этот показатель на 13%; при этом частота развития смертельного или несмертельного инсульта снижалась на 25%, а частота развития смертельного или несмертельного ИМ была одинаковой в обеих группах. Таким образом, результаты исследования LIFE свидетельствуют о том, что при артериальной гипертонии (АГ) с ГЛЖ применение блокатора рецепторов ангиотензина II (АН) лозартана снижает заболеваемость и смертность в большей степени, чем применение β-блокатора атенолола. На момент рандомизации клинические признаки ССЗ имелись у 25,1% больных, включенных в это исследование. После получения результатов исследования LIFE оставалось неясным, насколько эффективным было применение лозартана в подгруппе больных без явных клинических признаков ССЗ, т.е. насколько различается эффективность применения лозартана и атенолола для первичной профилактики ССЗ, включая ИМ.
В ходе вторичного анализа данных о больных, включенных в исследование LIFE, было установлено, что на момент рандомизации 6886 больных (средний возраст 66 лет; 57% женщины; средний уровень АД 174/98 мм рт. ст.) не имели явных клинических признаков ССЗ [27]. У таких больных степень снижения АД на фоне приема лозартана и атенолола была одинаковой. Прием лозартана по сравнению с атенололом статистически значимо снижал комбинированный показатель частоты развития ИМ, инсульта и смертности от ССЗ (эти неблагоприятные клинические события отмечены у 282 и 355 больных соответственно; 17,5/1000 и 21,8/1000 человеко-лет соответственно; относительный риск (ОР)=0,81 при 95% ДИ от 0,69 до 0,95; р=0,008), а также смертность от ССЗ (умерли 103 и 132 больных соответственно; ОР=0,80 при 95% ДИ от 0,62 до 1,04; р=0,092) и частоту развития смертельного или несмертельного инсульта (125 и 193 больных соответственно; ОР=0,66 при 95% ДИ от 0,53 до 0,82; р<0,001), но не влиял статистически значимо на частоту развития смертельного или несмертельного ИМ (110 и 100 больных соответственно; ОР=1,14 при 95% ДИ от 0,87 до 1,49; р>0,2). Кроме того, прием лозартана по сравнению с атенололом статистически значимо снижал частоту выявления новых случаев сахарного диабета (СД) (173 и 254 больных соответственно; ОР=0,69 при 95% ДИ от 0,57 до 0,84; р<0,001). Таким образом, в подгруппе больных с АГ и ГЛЖ, но без явных клинических признаков ССЗ, применение лозартана снижает сердечно-сосудистую заболеваемость и смертность в большей степени, чем применение атенолола, несмотря на одинаковое гипотензивное действие этих препаратов.
Таким образом, во вторичный анализ были включены данные почти о 75% участников исследования LIFE, у которых на момент рандомизации не было явных клинических признаков ССЗ. Установлено, что в этой подгруппе больных применение лозартана по сравнению с атенололом статистически значимо снижало комбинированный показатель частоты развития ИМ, инсульта и смертности от ССЗ (снижение ОР=19%). Большая эффективность применения лозартана для первичной профилактики ССЗ, связанных с развитием атеросклероза, представляется особенно примечательной, поскольку в плацебо-контролируемых исследованиях показано, что применение β-блокаторов снижает частоту развития ССЗ как у больных с АГ, так и у больных, перенесших ИМ или имеющих явные признаки других ССЗ [28-30]. Важным результатом этого вторичного анализа можно считать то, что снижение риска развития инсульта на фоне приема лозартана в подгруппе больных без явных признаков ССЗ оказалось более выраженным, чем в целом у участников исследования LIFE (на 34 и 25% соответственно). При этом необходимо отметить, что у больных с АГ, включенных в исследование LIFE, частота развития инсульта была на 44% выше, чем частота развития ИМ; это совпадает с результатами других испытаний гипотензивной терапии [31]. Профилактика инсульта становится особенно актуальной, поскольку в индустриально развитых странах период неуклонного снижения частоты развития инсульта сменился периодом плато и даже тенденцией к увеличению его распространенности.
Результаты вторичного анализа результатов исследования LIFE могут повлиять на тактику первичной профилактики ССЗ у больных с АГ и ГЛЖ.
Аспирин нередко используется для первичной и вторичной профилактики ИБС у больных с АГ. Еще один вторичный анализ результатов исследования LIFE [32] был проведен в связи с появлением противоречивых сообщений о возможных негативных взаимодействиях между аспирином и иАПФ, применяемыми одновременно у больных с АГ [33-35]. Цель этого вторичного анализа состояла в проверке гипотезы о том, что прием аспирина не оказывает отрицательного влияния на кардиопротективное действие лозартана. В ходе вторичного анализа данных установлено, что с самого начала исследования аспирин принимали 1004 (22%) больных в группе лозартана и 966 (21%) больных в группе атенолола. Среди получавших аспирин доля женщин составила 46% (среди всех участников исследования LIFE -54%); при этом доля больных, имевших какое-либо сосудистое заболевание, составила 60% (среди всех участников исследования LIFE - 26%). Между подгруппами больных, получавших и не получавших аспирин, а также между подгруппой больных, получавших аспирин, и всеми участниками исследования LIFE не было выявлено различий в проводимой гипотензивной терапии (как в отношении применяемых препаратов, так и их доз).
Частота развития побочных эффектов в подгруппе больных, получавших аспирин, и у всех участников исследования была практически одинаковой. Между подгруппами сочетанного применения лозартана и аспирина или атенолола и аспирина не выявлено различий в степени снижения как систолического, так и диастолического АД. Таким образом, одновременный прием аспирина не ослаблял гипотензивное действие лозартана или атенолола.
В целом комбинированный показатель частоты развития ИМ, инсульта и смертности от ССЗ в подгруппе лозартана и аспирина составил 128, а в подгруппе атенолола и аспирина - 180 (28,3/1000 и 42,1/1000 больных соответственно; р=0,001). При этом различие было статистически значимым при сравнении частоты развития инсульта, но не достигало уровня статистической значимости при сравнении смертности от ССЗ, частоты развития ИМ или выявления новых случаев СД.
При оценке комбинированного показателя частоты развития ИМ, инсульта и смертности от ССЗ установлено также, что в подгруппе лозартана и аспирина ОР снизился на 32%, а в группе лозартана в целом - лишь на 13%. Прием аспирина в целом не оказывал статистически значимого влияния на смертность от ССЗ, причем в подгруппе лозартана и аспирина отмечена тенденция к ее снижению. Риск развития инсульта оказался ниже на фоне приема лозартана (в подгруппе лозартана и аспирина снижение ОР составило 37%, а в группе лозартана в целом - 25%). Риск развития ИМ в группе лозартана был статистически незначимо ниже, чем в группе атенолола; одновременный прием аспирина не влиял на этот показатель. Риск возникновения новых случаев СД в группе лозартана в целом был статистически значимо ниже, чем в группе атенолола; однако при одновременном приеме лозартана и аспирина статистически значимых различий не выявлено.
Результаты теста на взаимодействие были статистически значимыми и свидетельствовали о том, что применение лозартана более эффективно на фоне приема аспирина (при сравнительной оценке комбинированного показателя частоты развития ИМ, инсульта и смертности от ССЗ р=0,016; при сравнительной оценке частоты развития ИМ р=0,037). При анализе кривых Каплана-Мейера установлено, что в целом частота развития неблагоприятных клинически исходов была выше на фоне приема аспирина, однако этот показатель статистически значимо снижался при сочетанном приеме лозартана и аспирина; расхождение кривых начиналось сравнительно рано и нарастало в течение всего периода наблюдения. Таким образом, сочетанное применение лозартана и аспирина при АГ снижает комбинированный показатель частоты развития ИМ, инсульта и смертности от ССЗ, а также частоту развития ИМ. Подобная терапия хорошо переносится больными.
Снижение ОР развития ИМ на 28% за счет применения лозартана по сравнению с плацебо было отмечено в исследовании RENAAL (Reduction of Endpoints in NIDDM with the Angiotensin II Antagonist Losartan) [36], включавшем 1513 больных с СД 2 типа и нефропатией. В группе лозартана и плацебо ИМ развился у 50 (6,7%) и 68 (8,9%) больных соответственно (р=0,08).
К положительным свойствам лозартана следует отнести его высокую безопасность и хорошую переносимость. В последние годы данным о безопасности лекарственной терапии уделяется особое внимание, что обусловлено в целом высокой частотой связанных с ней осложнений. В 1994 г. среди основных причин смерти 4-6 места занимали неблагоприятные реакции, связанные с применением лекарственных препаратов; на их долю пришлись 160 000 смертельных исходов и экономические потери в 100 млрд. долларов США [37]. Только в 1998 г. 108 000 американцев умерли от побочных реакций при использовании препаратов, одобренных к применению Администрацией США по контролю за качеством пищевых продуктов и лекарственных препаратов и правильно назначенных лицензированными медицинскими работниками; в целом в том же году побочные реакции при использовании разрешенных к применению препаратов отмечались у 2,2 млн. американцев [38-41].
При сравнении переносимости лозартана, эналаприла и плацебо в РКИ длительностью 8 нед была отмечена одинаковая частота развития кашля на фоне блокатора рецептора АII и плацебо (3% больных), в то время как прием иАПФ сопровождался более высокой частой развития кашля (8%) [42]. При этом отмечено одинаковое гипотензивное действие 50 мг лозартана и 20 мг эналаприла.
Ретроспективный анализ данных об амбулаторных больных, получавшихся гипотензивную терапию, показал, что через год частота продолжения начатой терапии блокатором рецепторов АII была существенно выше, чем при использовании иАПФ, антагонистов кальция, β-блокаторов и тиазидных диуретиков (64, 58, 50, 43 и 38% больных соответственно) [43].
Мнение о том, что "степень снижения АД представляется более важным фактором, определяющим клинический исход, по сравнению с выбором гипотензивного препарата" не подтверждается и результатами недавно выполненного мета-анализа эффективности применения атенолола при АГ. Действительно, как уже отмечалось выше, β-блокаторы в течение длительного времени рассматриваются, как препараты первого ряда при лечении АГ, а эффективность их применения при этом заболевании считалась доказанной
[44]. Атенолол относится к наиболее часто применяемым β-блокаторам, а также нередко используется как эталонный препарат сравнения в РКИ гипотензивной терапии [5, 26, 45, 46]. Однако в последнее время стали высказываться сомнения в обоснованности применения представителей этого класса в качестве препаратов первого ряда для лечения АГ [47]. Эффективность использования атенолола у больных, перенесших ИМ [48], также подвергалась сомнениям
Для оценки влияния приема атенолола на смертность и частоту развития сердечно-сосудистых осложнений у больных с АГ был проведен мета-анализ РКИ [49]. В мета-анализ были включены данные о 24 496 больных с АГ, принимавших участие в 8 РКИ гипотензивных препаратов. Для мета-анализа отбирали только те РКИ, в которые включали больных с эссенциальной АГ; проводили запланированный анализ таких клинических исходов, как частота развития ИМ, инсульта и смерти от ССЗ; в которых в качестве гипотензивного препарата первого ряда в одной из групп вмешательства использовали атенолол. Поиск статей осуществляли в базах данных Cochrane Library, MEDLINE, печатных изданиях, кроме того, использовали и личные контакты с исследователями. Применяли следующий алгоритм поиска статей в базах данных: atenolol (MESH) OR atenolol "text" AND cerebrovascular disorders (MESH) OR myocardial infarction (MESH); atenolol AND systematic; beta-blocker AND hypertension AND systematic.
Несмотря на существенные различия в степени снижения АД, не было отмечено статистически значимых различий между группой применения атенолола и контроля по таким показателям, как общая смертность (ОР=1,01 при 95% ДИ от 0,89 до 1,15), смертность от ССЗ (ОР=0,99 при 95% ДИ от 0,83 до 1,18), частота развития ИМ (ОР=0,99 при 95% ДИ от 0,83 до 1,19) и инсульта (0,85 при 95% ДИ от 0,72 до 1,01). В целом не отмечено статистически значимого различия по степени снижения АД между группами атенолола и других гипотензивных препаратов. Результаты мета-анализа 5 РКИ, включавших 17 671 больных, свидетельствуют о статистически значимо более высокой смертности при использовании (в среднем в течение 4,6 лет) атенолола по сравнению с другими препаратами (ОР=1,13 при 95% ДИ от 1,02 до 1,25). Более того, применение атенолола по сравнению с другими гипотензивными средствами сопровождалось тенденцией к увеличению риска смерти от ССЗ (ОР=1,16 при 95% ДИ от 1,00 до 1,34) и статистически значимым повышением частоты развития инсульта (ОР=1,30 при 95% ДИ от 1,12 до 1,50).
Поскольку в исследование LIFE было включено почти такое же число больных, как в целом во все остальные исследования, его данные оказывали сильное статистическое влияние на результаты мета-анализа 8 отобранных исследований. Поэтому дополнительно был проведен мета-анализ, не включавший данные исследования LIFE. В целом результаты этих мета-анализов совпадали. Таким образом, результаты мета-анализа 8 РКИ свидетельствуют о том, что применение атенолола при лечении АГ не влияет на клинические исходы.
Результаты представленного мета-анализа, по мнению его авторов, смогут положить конец сомнениям в целесообразности применения атенолола в качестве препарата первого ряда для лечения АГ, а также использования его как эталонного препарата сравнения в контролируемых испытаниях гипотензивных средств. Следует отметить, что преимущество применения атенолола по сравнению с плацебо или отсутствием терапии в снижении АД не сопровождалось снижением смертности или частоты развития ИМ. При сравнении эффективности применения атенолола с другими гипотензивными препаратами было установлено его статистически значимо меньшее влияние на частоту развития большинства клинических исходов, за исключением ИМ, частота развития которого оказалась сходной независимо от применяемого вмешательства.
Известно, что гипотензивный эффект атенолола существенно не отличается от эффекта других гипотензивных препаратов [50, 51]. Полученные в представленном мета-анализе результаты, свидетельствующие об отсутствии влияния терапии атенололом на клинические исходы, по-видимому, в первую очередь могут быть объяснены его невысокой липофильностью. Данные экспериментальных исследований на животных свидетельствуют о том, что способность β-блокаторов предотвращать развитие фибрилляции желудочков зависит от содержания препарата в центральной нервной системе [52, 53]. Атенолол, характеризующийся высокой гидрофильностью, обладает очень низкой способностью проникать в ткани нервной системы. В отличие от атенолола применение липофильного β-блокатора метопролола по сравнению с тиазидными диуретиками в исследовании МАРНY (Metoprolol Atherosclerosis Prevention in HYpertensives) [54] сопровождалось статистически значимым снижением риска развития ИБС у больных с АГ (ОР=0,76 при 95% ДИ от 0,58 до 0,98) [55]. Кроме того, данные, полученные при проведении мета-анализа исследований по оценке эффективности применения β-блокаторов после ИМ, свидетельствовали о статистически значимом снижении смертности за счет приема метопролола, тимолола и пропранолола, в то время как терапия атенололом не давала такого положительного эффекта [48]. Однако следует отметить, что низкой липофильностью вряд ли можно объяснить отсутствие статистически значимого влияния атенолола на другие клинические исходы.
Другим объяснением невысокой эффективности атенолола может служить его недостаточно выраженное влияние на ГЛЖ. В самом крупном мета-анализе, проведенном для оценки влияния гипотензивных препаратов разных классов на ГЛЖ, было показано, что в целом β-блокаторы влияют на обратное развитие ГЛЖ в меньшей степени, чем препараты других классов [56]. Применение атенолола, в отличие от многих других гипотензивных препаратов, не влияет на ремоделирование мелких сосудов и не улучшает функцию их эндотелия [57-59]. При переводе больных с длительной гипотензивной терапии атенололом на прием блокатора рецепторов АII отмечено статистически значимое уменьшение соотношения толщины средней оболочки артерий (медии) и диаметра просвета резистивных артерий, а также увеличение степени расслабления артерий, зависящего от эндотелия [60]. Результаты представленного мета-анализа могут указывать на нецелесообразность дальнейшего применения атенолола в качестве препарата первого ряда для лечения АГ, а также эталонного препарата сравнения в контролируемых клинических испытаниях гипотензивных средств.
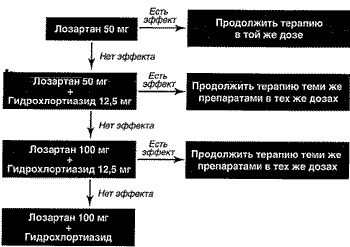
Таким образом, имеющиеся данные доказательной кардиологии свидетельствуют о том, что эффективное снижение АД является необходимым, но не достаточным условием эффективности антигипертензивных препаратов. По крайней мере, не вызывает сомнений, что, при лечении АГ у больных с ГЛЖ необходимо применять препараты, не только оказывающие гипотензивное действие, но имеющие также доказанную способность к снижению риска развития тяжелых ССЗ (рис. 1).
Рис 1. Алгоритм выбора гипотензивной терапии для профилактики ССЗ у больных с ГЛЖ.
| Апрель 2008 г. |