НОВЫЕ ВОЗМОЖНОСТИ ЛЕЧЕНИЯ АСТЕНИЧЕСКИХ РАССТРОЙСТВ В ПСИХИАТРИЧЕСКОЙ, НЕВРОЛОГИЧЕСКОЙ И СОМАТИЧЕСКОЙ ПРАКТИКЕ
В.Э.Медведев
ФГБОУ ВПО Российский университет дружбы народов, МоскваРезюме.
Подходы к терапии астенических проявлений до настоящего времени остаются дискуссионными. В статье обсуждается возможность применения препарата с широким спектром действия Нооклерина в комплексной и монотерапии астенических расстройств различного генеза в психиатрической, неврологической и общей медицинской практике.Ключевые слова:
астения, нооклерин, психиатрия, гепатопротектор, деанола ацеглумат.В последние годы появляется все больше данных о возможности применения ноотропных лекарственных средств, обладающих широким спектром психофармакотерапевтической активности (ноотропы, нейропротекторы) в моно- или комплексной терапии различных психических расстройств.
Многими авторами подчеркивается целесообразность включения препаратов этого ряда, обладающих не только активирующим действием на когнитивные функции, но и антиастеническим, стимулирующим, тимолептическим эффектами, в терапию соматогений, астенических депрессий, а также для купирования и профилактики кардионев ротического и неврастенического симптомокомплексов (В.Э.Медведев, К.А.Албантова, 2009; В.Э.Медведев, 2010; И.Н.Шакирова, Г.МДюкова, 2012; В.В.Гусев, О.А.Львова, 2013).
Астенические расстройства могут значительно снижать работоспособность пациентов, нарушать их привычную жизнедеятельность, а иногда выступать в качестве фона, на котором формируются другие, более тяжелые психические или соматические нарушения. Все это приобретает особое значение, когда речь заходит об имеющихся в настоящее время возможностях терапии астенических состояний. Использование психостимуляторов у этой группы больных представляется крайне нежелательным в связи с установленными данными о возможности злоупотребления ими с формированием явлений зависимости (А.С.Аведисова, 2005).
В качестве альтернативы психостимуляторам в данном случае рассматриваются препараты нейрометаболическо го действия, в психофармакологическом спектре которых выявляется отчетливый психостимулирующий эффект. Такие лекарственные средства обладают свойствами психостимуляторов (повышение психомоторной активности) и ноотропов (улучшение когнитивных функций) и могут быть выделены в особую группу антиастенических средств.
К этой группе препаратов относится Нооклерин (деанола ацеглумат), разработанный во Всероссийском научном центре по безопасности биологически активных веществ - ФГУП ВНЦ БАВ (ранее производился под торговыми названиями Глютабианц, Нооклер).
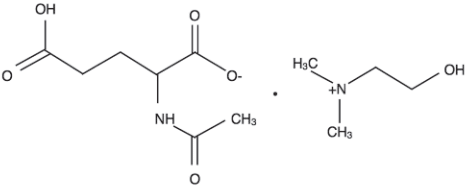
По химической структуре Нооклерин близок к естественным метаболитам мозга - гамма-аминомасляной кислоте, глутаминовой кислоте (см. рисунок). Нейрофизиологические механизмы препарата связаны с облегчением передачи возбуждения по моносимпатическим путям, в результате чего сглаживаются межполушарные различия, что, по всей видимости, приводит к улучшению интегративной деятельности мозга.
Фармакокинетика
Деанола ацеглумат обладает высокой биодоступностью и быстрым распределением: уже через 30-60 мин после приема внутрь 20% раствора Нооклерина его концентрации в плазме крови, головном мозге и печени достигают максимальных показателей. Выводится почками, период полувыведения составляет 24 ч. Рекомендуемый режим применения: внутрь после еды по 1-2 г препарата 2-3 раза в день. Максимальная разовая доза - 2 г, суточная - 10 г.
Спектр клинического применения Нооклерина
Нооклерин оказывает ноотропный эффект в сочетании с выраженным психостимулирующим и церебропротек тивным действием. Облегчает процессы фиксации, консолидации и воспроизведения информации, улучшает способность к обучению.
Основными показаниями к применению Нооклерина являются когнитивные, астенические и астено-депрессив ные расстройства различного генеза, последствия черепно-мозговых травм и сосудистые заболевания мозга (дис циркуляторная энцефалопатия и постинсультные расстройства). Препарат оказывает положительное влияние при астенических и адинамических расстройствах, повышая двигательную и психическую активность пациентов и улучшая процессы памяти и внимания.
Кроме того, деанола ацеглумат рекомендуется в качестве дополнительного корректора при лечении хронической нейролепсии, особенно акинетических нарушений (В.И. Дикая, 1992; V.Pennington, 1959; L.Levine, 1960).
Химическая структура деанола ацеглумата.
Отдельные авторы указывают на возможность коррекции деанолом ацеглуматом резидуально-неврологических расстройств детского возраста в виде заикания, синдрома нарушения внимания с гиперактивностью, энуреза, блефароспазма (М.И. Лохов и соавт., 2005; E.Miller, 1971).
Нооклерин (деанола ацеглумат) был всесторонне изучен в доклинических и клинических исследованиях (цит. по А.С. Аведисовой, 2005).
В клинике его изучали более чем у 1 тыс. больных г. Москвы по следующим показаниям:
нарушения когнитивных функций различного генеза в разных возрастных группах, включая детей и лиц пожилого возраста; астенические и астено-депрессивные расстройства при функциональной астении и пограничных состояниях; астено-адинамические расстройства в рамках шизофренического дефекта; алкогольный абстинентный синдром; легкие проявления нейролептического синдрома; коррекция нарушений работоспособности у спортсменов; влияние на зрительные функции. Церебропротективный эффект Нооклерина
Как было показано в работе Т.И.Макаровой (2007 г.), введение Нооклерина животным в дозах 1, 10, 20, 50 и 100 мг/кг способствовало увеличению выживаемости белых крыс при билатеральной окклюзии сонных артерий, причем наиболее эффективными являлись дозы 10, 20 и 50 мг/кг, которые увеличивали выживаемость с 20% в контроле до 80, 70 и 60% соответственно.
Деанола ацеглумат повышает устойчивость организма к недостатку кислорода (G.Malanga и соавт., 2012). При исследовании влияния Нооклерина на устойчивость животных к дефициту кислорода при циркуляторной гипоксии отмечается выраженное противогипоксическое действие в дозах 10 и 50 мг/кг: Нооклерин увеличивает данный показатель до 83 и 50% соответственно (Т.И.Макарова, 2007).
Нооклерин препятствует депрессии биоэлектрической активности мозга в период ишемии и активирует восстановление суммарной мощности и максимальной амплитуды в период реперфузии. Введение Нооклерина в условиях острой ишемии мозга ограничивает развитие фазы реактивной гиперемии и нивелирует фазу гипоперфузии. Нооклерин в условиях ишемических повреждений мозга активирует ферменты антиоксидантной защиты, препятствует накоплению как первичных, так и вторичных продуктов перекисного окисления липидов в церебральной ткани (С.Я.Скачилова и соавт., 2006; Т.И.Макарова, 2007).
По данным других авторов, также подтверждается наличие у Нооклерина церебропротективных свойств (предупреждение или ослабление амнезии, вызванной максимальным электрошоком, скополамином, лишением парадоксальной фазы сна). Препарат способствует улучшению обучения, облегчает процессы фиксации, консолидации и воспроизведения памятного следа; оказывает влияние на процессы тканевого обмена, увеличивает амплитуды транскаллогеального вызванного потенциала, улучшает организацию основного ритма электроэнцефалографии, сглаживает межполушарную асимметрию (С.Я.Скачилова и соавт., 2006; J.Moriarty, J.Mebane, 1959; E.Levin и соавт., 1995).
По результатам собственного исследования А.З.Файзуллоев (1997 г.) устанавливает, что динамический профиль психофизиологического действия Нооклерина достоверно характеризуется синергической оптимизацией параметров внимания, краткосрочной памяти, микрокоординации движений, сенсомоторной координации и функциональной подвижности зрительного анализатора.
Влияние Нооклерина на когнитивную дисфункцию
Положительное влияние Нооклерина на уменьшение выраженности когнитивных расстройств показано в исследовании Ю.А. Александровского и соавт. (1992 г.). Дифференцированная динамическая оценка влияния разовых и курсовых доз Нооклерина на психофизиологические характеристики проводилась до начала терапии (фоновые исследования), спустя 2 ч после однократного приема препарата и на 7, 14 и 28-й дни курсовой монотерапии. При обследовании пациентов использовались автоматизированные системы психофизиологической диагностики -Венская тестовая система и КПФК-99, с помощью которых оценивали параметры краткосрочной памяти, внимания и времени реакции.
На фоне приема разовой дозы Нооклерина в течение 2 ч установлено улучшение характеристик краткосрочной памяти с увеличением правильных ответов. Аналогичные изменения фиксировались для характеристик продуктивности оперативной памяти, о чем свидетельствует снижение количества ошибочно названных ответов при проведении теста «Арифметические действия».
На 7-й день курсовой терапии улучшались характеристики объема, продуктивности краткосрочной памяти (по росту общего числа ответов с увеличением доли правильных ответов). Интегративные параметры внимания также улучшались уже на 7-й день курсовой монотерапии, на что указывали результаты «Корректурной пробы с кольцами Ландольта» (рост объема внимания, улучшение его продуктивности и позитивные сдвиги параметров распределения и переключения внимания). Кроме того, отмечалось дальнейшее улучшение параметров сенсомоторной активности (сокращение времени дифференцированной сенсомоторной реакции различия).
В дальнейшем на 14 и 28-й дни монотерапии Нооклерином параметры психофизиологического состояния больных отражали позитивную динамику и указывали на улучшение параметров когнитивной деятельности - краткосрочной памяти, внимания и времени реакции (Ю.А.Александровский, 1992).
Антиастенический эффект Нооклерина при функциональных расстройствах
В исследовании приняли участие 60 пациентов (18 мужчин, 42 женщины) в возрасте 18-65 лет (средний возраст 36,3 года), в состоянии которых выявлялись астенические нарушения (12 баллов и более по пунктам шкалы астении MFI-20) функционального характера. Средняя продолжительность наличия признаков функциональной астении составила 6 мес.
Нооклерин назначали при астенических нарушениях, обусловленных соматическими заболеваниями (пневмония, острый холецистит, астматический бронхит, обострения язвенной болезни желудка и двенадцатиперстной кишки, эндокринная патология вне обострения), перенесенными инфекциями, органическим поражением центральной нервной системы, соматоформными дисфункциями вегетативной нервной системы (Ю.А.Александров ский и соавт., 2004).
Нооклерин назначался в течение 28 дней после периода отмены предшествующей терапии, достаточного для элиминации. Дозировка Нооклерина составила по 2-3 раза в сутки.
Наиболее выраженная динамика в ходе терапии Ноокле рином отмечалась по показателям шкалы самооценки функционального состояния.
В течение 1 -й недели терапии среднее значение данного показателя продемонстрировало тенденцию к быстрому росту, в течение последующих 3 нед лечения Нооклерином интенсивность этой динамики снижалась незначительно, что свидетельствовало о существенном положительном влиянии препарата на субъективное восприятие состояния пациентами даже при сохраняющихся на начальных этапах терапии нарушениях астенического круга, регистрируемых шкалами объективной оценки. В целом выраженный положительный результат лечения регистрировался у 38 (63,3%) человек.
Анализ динамики среднего суммарного показателя шкалы субъективной оценки астении MFI-20 на 28-й день терапии позволил констатировать его снижение на 54%. Среднее значение показателей визуальной аналоговой шкалы астении в ходе терапии уменьшилось на 57,2%.
Отмечалось также улучшение параметров когнитивной деятельности (краткосрочная память, внимание и время реакции), что является объективным проявлением выраженности собственно ноотропного действия препарата.
Авторы приходят к выводам о том, что Нооклерин является высокоэффективным и безопасным средством, показанным для терапии широкого круга состояний, сопровождающихся явлениями функциональной астении.
Более того, сравнивая полученные результаты с данными литературы, исследователи находят, что в процессе терапии Нооклерином подвержены максимальному обратному развитию считающиеся резистентными к проводимой терапии состояния с преобладанием гипостеническо го варианта астенического синдрома.
Сходные результаты были получены и при клинических исследованиях Нооклерина в других клиниках, в том числе НИИ клинической психиатрии НЦПЗ РАМН, психиатрической клинике им. С.С.Корсакова, ММА им. И.М.Сечено ва, НЦПЗ РАМН и ГНЦ наркологии Минздрава РФ. Проведенные исследования продемонстрировали, что благоприятный эффект Нооклерина максимально проявляется при астенических, астено-депрессивных и астеноипо хондрических расстройствах. Постепенная частичная редукция астенических проявлений, выражавшаяся уменьшением слабости, утомляемости, дневной сонливости, повышением работоспособности и улучшением внимания, развивалась вскоре после начала лечения и была отчетливо выражена уже к 3-10-му дню терапии.
Активирующий эффект нарастал к концу 2-3-й недели приема препарата. При этом повышался общий физический тонус, восстанавливалась умственная работоспособность, улучшалось настроение, а также значительно уменьшались вегетативные нарушения, сопутствующие астеническим состояниям (повышенная потливость, частые головные боли, головокружения, нарушенное сердцебиение и др.). У больных с выраженными гипостеническими проявлениями наряду с активирующим эффектом уменьшались раздражительность и слезливость.
Исследование антиастенического действия Нооклерина при функциональной астении различного генеза было проведено также на амбулаторном контингенте 30 подростков 13-17 лет на базе отделения подростковой психиатрии СПб НИПНИ им. В.М.Бехтерева, (Ю.В.Попов, 2004).
Состояние больных оценивалось по шкале субъективной оценки астении MFI-20 и визуальной налоговой шкале астении. Во время исследования запрещалось применение антиастенических препаратов, психостимуляторов, нейролептиков, ноотропов, гипнотиков, миорелаксантов, стероидов, седативных средств.
У подростков с функциональной астенией непсихотического характера отмечались быстрая истощаемость, плохая концентрация внимания, рассеянность, снижение активности и настроения, общая слабость, вялость. Длительность указанных проявлений к моменту исследования составляла от 3 мес до 4 лет. Из сопутствующих расстройств преобладали коморбидные психопатологические расстройства (63,3%) в виде невротических расстройств (рубрика F4 по Международной классификации болезней 10-го пересмотра), а также поведенческих и эмоциональных расстройств, начинающихся в детском и подростковом возрасте (F9). Коморбидные соматические расстройства выявлены у 46,7% больных. У большинства это были хронические заболевания ЛОР-органов.
Полученные данные свидетельствовали о том, что Но оклерин является эффективным и безопасным средством терапии у этого контингента больных. При этом эффективность препарата не зависела от пола, возраста (в пределах исследованной группы) и социального статуса пациента. Нонреспондерами оказались 25,9% подростков, среди которых преобладали пациенты с астеническими проявлениями на фоне длительных невротических расстройств (свыше 2 лет). Других факторов, влияющих на эффективность Нооклерина, у исследуемого контингента не отмечалось.
Важно заметить, что автор подчеркивает необходимость длительного приема препарата (не менее 4 нед), так как отчетливый антиастенический эффект регистрируется к 28-му дню терапии.
В геронтопсихиатрической практике изучение применения Нооклерина у больных с функциональной астенией было проведено М.П.Андрусенко и Г.П.Пантелеевой (1992 г.). В работе исследовалась эффективность Нооклерина (800 мг/сут) и сопоставление его с пирацетамом при нарушениях умственной деятельности в рамках психоорганического синдрома и астенических состояниях, развивающихся после черепно-мозговых травм, нейроинфекций, интоксикаций, острых и хронических нарушений мозгового кровообращения.
В группе больных, получающих Нооклерин (36 пациентов: 27 женщин, 9 мужчин в возрасте 54-87 лет; средний возраст 69±1,2 года), достоверное улучшение общего состояния наблюдалось уже с 7-го дня (p<0,05), психического состояния (уменьшение вялости, слабости, истощаемости, рассеянности, неустойчивости внимания, увеличение умственной продуктивности) - с 14-го дня (p<0,05) (М.П.Андрусенко, Г.П.Пантелеева, 1992).
Антиастенический эффект Нооклерина при психических расстройствах
В ряде работ подчеркивается высокая эффективность терапии Нооклерином астенических расстройств различного генеза, таких как органическая патология ЦНС, соматические заболевания, психические и личностные расстройства (Ю.А. Александровский и соавт., 2003; А.С.Аведисова, 2005).
Клиническое изучение эффективности Нооклерина при различных астено-невротических (астенодепрессивных, астеноипохондрических) расстройствах было проведено Ю.А. Александровским и соавт. (1992 г.).
Исследуемую группу составили 40 пациентов обоего пола в возрасте 19-75 лет. Терапевтический эффект, выражавшийся в постепенной редукции астенических проявлений (уменьшение слабости, утомляемости, дневной сонливости, головных болей, головокружений, повышение работоспособности, улучшение внимания), при приеме Нооклерина наблюдался к 3-10-му дню терапии. Применение его было наиболее эффективным у больных с нетяжелыми психогенно- и соматогенно обусловленными расстройствами в виде простых по психопатологической структуре астенических нарушений.
Кроме того, анализ результатов лечения Нооклерином, по мнению авторов, свидетельствует о выраженном активирующем и стимулирующем действии, нарастающем к концу 2-3-й недели приема препарата.
Одним из первых отечественных исследований эффективности и переносимости Нооклерина у больных с астеническими расстройствами на фоне эндогенно-процессуального заболевания является работа В.И.Дикой и соавт. (1992 г.), выполненная в НЦПЗ РАМН.
Авторы сравнивали Нооклерин с ноотропилом при лечении астенодепрессивных нарушений в рамках шубообразной шизофрении (на стадии обратного развития психоза) и при проявлениях астенического дефекта (вяло-апатические проявления, трудности сосредоточения с жалобами на расстройства памяти, с картиной «юношеской несостоятельности»). Группу больных, получавших Нооклерин (1000-6000 мг/сут), составили 66 женщин и 63 мужчины. При этом монотерапия Нооклерином проводилась 55 больным, остальным Нооклерин назначался на фоне предшествующей терапии антидепрессантами, транквилизаторами и небольшими дозами нейролептиков. Длительность приема Нооклерина варьировала от 14 до 40 дней (в среднем 1 мес).
Согласно полученным результатам терапевтическое действие Нооклерина обнаруживается уже начиная с 7-го дня лечения и проявляется в уменьшении вялости и слабости, истощаемости и активации поведения, оживлении мимики, моторики, облегчении процессов мышления.
Наибольшую терапевтическую эффективность Ноокле рин оказывает при астено-депрессивных состояниях (75%) и проявлениях астенического дефекта (100%), а также при адинамических депрессивных расстройствах (88%).
Также высокую эффективность Нооклерин обнаруживает при лечении нейролептического синдрома в виде акинетических и реже гиперкинетических нарушений, что реализуется в уменьшении явлений мышечной скованности, оживлении мимики и двигательной сферы (В.И. Дикая, 1992).
Результаты данного исследования указывают на то, что по особенностям терапевтического воздействия Ноокле рин соответствует препаратам ноотропного действия, обладает отчетливым стимулирующим и активирующим эффектами, сходными с ноотропилом. Активизирующий эффект Нооклерина в сравнении с ноотропилом оказывается несколько более выраженным по влиянию на психическую сферу и примерно идентичным по влиянию на со матоневрологические проявления, особенно в отношении редукции таких вегетативных нарушений, как головокружение, потливость, нарушение сна и аппетита.
Проведенное исследование терапевтической активности Нооклерина в сравнении с ноотропилом (В.И.Дикая и соавт., 1992) показывает, что Нооклерин обладает отчетливой ноотропной и психостимулирующей активностью у больных с нарушениями интеллектуальной деятельности и астеническими расстройствами, возникшими в структуре шизофренического дефекта, аффективных и невротических расстройств, психоорганического синдрома.
Авторы также обнаруживают способность Нооклерина корригировать побочные явления антипсихотической терапии у больных шизофренией.
Коррекция нарушений работоспособности у спортсменов
В плацебо-контролируемом исследовании было показано положительное действие Нооклерина на физическую работоспособность и ее восстановление у спортсменов (легкоатлеты-мужчины в возрасте от 19 до 26 лет: средние и длинные дистанции), тренирующихся в циклических видах спорта на развитие выносливости (плавание на длинные дистанции, гребля, лыжный спорт, конькобежный спорт, велосипедный спорт, спортивные игры, единоборств и др.), что позволяет рекомендовать препарат для применения в спортивной медицине (Р.Д.Сейфулла, И.М.Кондратьева, 1999).
Было показано, что препарат помогает снять переутомление в результате интенсивных физических нагрузок, усталость, депрессивные состояния, способствует усвоению запоминания новых навыков в учебно-тренировочном процессе, в соревнованиях для повышения спортивной работоспособности.
Гепатопротективный и антиабстинентный эффекты Нооклерина при алкоголизме
Сравнительное исследование гепатопротекторных свойств Нооклерина было проведено Б.Альтшулером и ГЮ.Абдуллаевым в НИИ наркологии (1999 г.). Были обследованы 22 пациента (20 больных, страдающих алкоголизмом, 2 пациента - героиновой наркоманией). У больных алкоголизмом диагностировались жировая дистрофия печени и алкогольный гепатит (по 10 пациентов); у больных наркоманией - острый токсический гепатит. Ноокле рин (100 мг 3 раза в день) назначался курсом от 14 до 16 дней в виде монотерапии на 10- 14-й день воздержания от приема алкоголя и наркотиков после купирования острых абстинентных расстройств.
По наблюдению авторов, результаты исследования гепа тозащитного эффекта Нооклерина указывают на гораздо более выраженную положительную динамику, более явный клинический эффект, достигаемый за более короткий срок, чем в контрольной группе больных, получающих стандартную на тот момент гепатопротекторную терапию (Т.Ю. Абдуллаев, 2001; В.Б.Альтшулер, Т.Ю.Абдуллаев, 1999, 2000).
Некоторые авторы находят возможным и оправданным назначение больших доз Нооклерина для быстрого купирования абстинентного синдрома у больных хроническим алкоголизмом (Н.М. Жариков, 1993).
К.Э.Воронин (1999 г.) изучал влияние Нооклерина на проявлении алкогольного абстинентного синдрома (ААС) и признаки патологического влечения к алкоголю (ПВА). Участники исследования (60 больных алкоголизмом в возрасте от 24 до 53 лет) были разделены на 3 группы: 1-ю составили 26 больных, которым Нооклерин назначался с целью купирования ААС; 2-ю (20 больных) - пациенты, получавшие Нооклерин для купирования ПВА, актуализировавшегося в стационаре на этапе становления ремиссии; 3-ю (14 больных) - больные, которым Нооклерин назначался для улучшения интеллектуально-мнестических функций, нарушенных в результате длительной интоксикации этанолом.
По заключению автора, Нооклерин демонстрирует высокую эффективность как для купирования ААС с преобладанием соматовегетативного и астенического компонентов, так и для улучшения интеллектуально-мнестических функций у больных алкоголизмом без признаков тяжелого органического поражения ЦНС.
Исследование, проведенное в отделении клинических исследований алкоголизма ФГБУ «ННЦ наркологии» МЗ РФ (Альтшулер В.Б. и соавт., 2013) показало, что прием Нооклерина внутрь в суточной дозе 2000 мг у больных алкоголизмом оказывает лечебный эффект, в структуре которого преобладает благоприятное ноотропное действие. Действие Нооклерина в направлении улучшения функций печени дает основание считать данный препарат эффективным гепатозащитным средством.
Наряду с этим, отмечено позитивное влияние препарата на психопатологическую, висцеральную и нейровегета тивную симптоматику алкогольного абстинентного синдрома.
Влияние деанола ацеглумата на зрительные функции
Зрительный анализатор несет основную нагрузку по восприятию и переработке огромного потока визуальной информации и, следовательно, постоянно подвергается информационным перегрузкам, особенно у лиц с невротическими расстройствами, что подчеркивает актуальность целенаправленного клинико-фармакологического исследования активности препаратов нейрометаболиче ского действия для обоснования их применения.
Был проведен сравнительный динамический анализ влияния однократного приема плацебо, разовой дозы и курсового приема деанола ацеглумата и пикамилона на интегративные параметры функционального состояния зрительного анализатора у больных с невротическими расстройствами (О.М.Манько, 1997). Исследование проводилось на базе клинического отделения отдела пограничной психиатрии ГНЦССП им. В.П.Сербского Минздрава РФ и в поликлинике ГУВД МО.
Были обследованы 107 больных в возрасте 20-45 лет с невротическими расстройствами (неврастения, невротическое развитие личности, невроз навязчивых состояний). В течение 2 нед до начала монотерапии нейрометаболи ческими стимуляторами (деанола ацеглумат и пикамилон) пациенты не получали никаких других медикаментозных средств. Из исследования исключались больные с наличием изначальной функционально-органической офтальмопатологии.
Курсовой прием деанола ацеглумата оказывал позитивное воздействие на функциональное состояние зрительного анализатора у больных с невротическими расстройствами: в частности, отмечалась более выраженная в сравнении с пикамилоном оптимизация параметров абсолютной дифференциальной цветовой чувствительности и порога функциональной подвижности.
Полученные результаты авторы объясняют свойственной деанолу ацеглумату как стимулятору пресинаптиче ской передачи более выраженной активацией процессов синаптической передачи в ЦНС, способствующей облегчению транслокальной передачи между поверхностными и глубокими слоями коры полушарий головного мозга. Деанола ацеглумат, стимулируя нейронную активность, вероятно, способствует существенному укорочению времени формирования циклов возбуждения в нейронных структурах зрительного анализатора и формированию позитивных функциональных адаптационно-компенсаторных перестроек в системах зрительного анализатора больных с невротическими расстройствами.
Выявленное нейровегетотропное действие деанола аце глумата, вероятно, в значительной степени предопределяет его позитивное воздействие не только на сложнейшую морфофункциональную систему зрительного анализатора, но и на функциональное состояние ЦНС в целом.
Изучено также влияние Нооклерина на зрительные функции и антиоксидантную активность слезы больных первичной открытоугольной глаукомой - ПОУГ (С.А.Бо рисова и соавт., 2006). Показано улучшение зрительных функций после курса лечения Нооклерином в виде достоверного снижения дефицита площади в центральном поле зрения и повышения уровня световой чувствительности, что свидетельствует о возрастании функциональной активности сетчатки и зрительного нерва у больных ПОУГ.
Кроме того, было выявлено положительное и достоверное влияние Нооклерина на гидродинамические показатели у больных ПОУГ: истинное внутриглазное давление, коэффициент легкости оттока, секрецию внутриглазной жидкости.
Благодаря нейрометаболическому, ноотропному и ней ропротекторному действию Нооклерина с нормализующим действием на местную антиокислительную систему глаза авторы рекомендуют препарат в комплексной терапии глаукоматозной оптической нейропатии, заболеваний, связанных с нарушением церебральной гемодинамики, и лицам, работающим с компьютерами.
Безопасность и переносимость Нооклерина
В подавляющем количестве публикаций подчеркивается хорошая переносимость Нооклерина и отсутствие нежелательных явлений (НЯ) на фоне его приема. Наряду с высокой терапевтической эффективностью эти свойства препарата определяют высокую приверженность терапии, в том числе у детей, подростков и пожилых людей.
Незначительные побочные эффекты (головная боль, раздражительность, инсомния, повышение аппетита), спектр которых подтверждал наличие у препарата стимулирующего действия, наблюдались преимущественно у больных с гиперстеническим вариантом астенического синдрома и ни в одном случае не приводили к его преждевременной отмене. Изменение режима приема Нооклери на (только в утреннее и дневное время) позволяло значительно уменьшить число НЯ. Особо следует отметить отсутствие у препарата свойственного психостимуляторам эйфоризирующего эффекта (А.С.Аведисова, 2005).
В сравнении с ноотропилом действие Нооклерина отличается лучшей переносимостью (П.В.Морозов, 2003), что особенно важно для больных шизофренией, у которых Нооклерин, значительно улучшая состояние, не вызывает в отличие от ноотропила появления взбудораженности, раздражительности, обострения психопатологической симптоматики (П.В.Морозов, 2003).
Среди НЯ, регистрировавшихся на фоне приема Ноокле рина, описываются единичные случаи легких проявлений инсомнии, нормализовавшейся без медикаментозного вмешательства (Ю.В.Попов, 2004) и тревоги (М.П.Андру сенко, Г.П.Пантелеева, 1992). В связи с этим при наличии в структуре психопатологических состояний выраженной тревоги, аффективных нарушений, нарушений сна рекомендуется назначение Нооклерина в сочетании с анксио литиками (Ю.А.Александровский и соавт., 2003).
Заключение
Результаты клинических исследований позволили сформулировать широкий круг показаний к применению Но оклерина в психиатрической, неврологической и общесоматической практике. Основными среди них являются астенические состояния различного генеза, в том числе развивающиеся в результате черепно-мозговых травм и сосудистых заболеваний головного мозга.
Клинические исследования Нооклерина свидетельствуют о том, что препарат обладает отчетливой ноотроп ной и церебропротективной активностью, эффективен при лечении астенических и астенодепрессивных расстройств (соматические заболевания, реакции на острый стресс, инфекции, пограничные состояния, алкоголизм, психоорганические нарушения, эндогенные заболевания) у пациентов разных возрастных групп (старше 10 лет). Препарат рекомендуется для улучшения интеллектуально-мнестических функций, коррекции проявлений нейролептического синдрома, купирования алкогольного абстинентного синдрома (ААС) с преобладанием соматове гетативных и астенических расстройств, в педиатрии -для улучшения качества обучения.
Перспективным представляется использование Ноокле рина в целях профилактики и коррекции нарушений функционального состояния зрительного анализатора у лиц, профессиональная деятельность которых сопряжена с постоянным воздействием непрерывного потока зрительной информации.
В спортивной медицине Нооклерин может использоваться в качестве средства, корригирующего работоспособность спортсменов и способствующего развитию выносливости.
Наличие выраженных гепатопротекторных свойств у Нооклерина позволяет рассматривать возможность его применения при лечении алкоголизма с поражением печени.
Таким образом, Нооклерин является высокоэффективным и безопасным средством, показанным для терапии широкого круга состояний, включающих явления астении. К ним относятся, как правило, сопровождающиеся повышенной утомляемостью и слабостью хронические, часто прогрессирующие неврологические, психические (например, шизофрения) и соматические заболевания (прежде всего инфекционные, эндокринные, гематологические, неопластические и гепатологические), злоупотребление психоактивными веществами и др.
Кроме того, в круг показаний для назначения Нооклери на можно отнести астенические явления, возникающие как реакция на острый стресс или значительные перегрузки на работе, в спорте и т.д. или развивающиеся вслед за родами (послеродовая астения), инфекциями (постин фекционная астения), или в структуре синдрома отмены, кахексии и др., а также астению, коморбидную другим пограничным психическим расстройствам (тревога, депрессия, инсомния и пр.). Вызывая у большинства пациентов быструю редукцию астенических нарушений, Нооклерин лишен отрицательных свойств психостимуляторов и обладает позитивным влиянием на психофизиологические показатели когнитивной деятельности пациентов, свойственным ноотропным препаратам.
ЛИТЕРАТУРА
1. Абдуллаев ТЮ. Роль патологии печени в клинике алкоголизма. Автореф. дис.... канд.мед. наук, 2001.
2. Аведисова А.С. Новый отечественный ноотроп Нооклерин в терапии астении и других заболеваний. Фарматека. 2005; 6: 51-4.
3. Александровский Ю.А., Аведисова Р.С., Князева НА. и др. Отчет НИИОСП им. В.П.Сербского, 1992.
4. Александровский Ю.А., Аведисова А.С., Ястребов Д.В. и др. Применение препарата Нооклерин в качестве антиастеническо го средства у больных с функциональной астенией. Психиатр. и психофармакотер. 2003; 4:164-6.
5. Альтшулер ВБ, Абдуллаев Т.Ю. Гепатопротектор Глютаби анц - эффективное средство лечения хронической и острой алкогольной интоксикации. XII Съезд психиатров России, 10-13 октября 2000 г. Материалы съезда. М, 2000; с. 223.
6. Альтшулер В.Б., Абдуллаев Г.Ю. Отчет НИИ наркологии Минздрава РФ, 1999.
7. Андрусенко М.П., Пантелеева Г.П. Отчет НЦПЗ РАМН, 1992.
8. Борисова С.А., Абдулкадырова М.Ж., Кузнецова Т.П., Давыдова Н.Г. Влияние ноотропов на зрительные функции и антиоксидантную активность слезы больных первичной открытоугольной глаукомой. Вестн. офтальмологии. 2006; 6:42-5.
9. Воронин К.Э. О новых препаратах для лечения наркоманий и токсикоманий, прошедших клинические испытания в ВНЦ наркологии Минздрава СССР. Вопр. наркологии. 1991; 1:42-3.
10. Гершанович ИИ. Отчет ВНЦ БАВ, 1999.
11. Горчакова Л.Н. Вялотекущая шизофрения с преобладанием астенических расстройств. Автореф. дис. . канд. мед. наук. М., 1989.
12. Альтшулер ВБ, Корольков А.И., Кравченко С.Л., Козырева А.В. Отчет отделения клинических исследований алкоголизма ФГБУ «ННЦ наркологии» МЗ РФ. 2013.
13. Гусев В.В., Львова О.А. Современные подходы к терапии астенического синдрома. Cons. Med. 2013; 1.
14. Дикая В.И., Владимирова Т.В., Никифорова М.Д., Пантелеева Г.П. Отчет НЦПЗ РАМН, 1992.
15. Жариков Н.М., Иваницкая ТИ, Телюк Л.И., Воробьева И.Д. Отчет Клиники психиатрии им. С.С.Корсакова ММА им. ИМ.Сече нова, 1991.
16. Жариков Н.М., Иваницкая Т.И., Телюк Л.И. Отчет Клиники психиатрии им. С.С.Корсакова ММА им. И.М.Сеченова, 1993.
17. Лохов М.И., Скоромец А.А., Фесенко Ю.А. Задержка развития функционального взаимодействия структур коры головного мозга как основа патогенеза речевых расстройств детского возраста (диагностика и терапия). Обозрение психиатрии и мед. психологии им. В.М.Бехтерева. 2005; 4.
18. Макарова Т.И. Экспериментальное изучение нейропротекторной активности Нооклерина. Автореф. дис. ... канд. мед. наук. Купавна, 2007.
19. Манько ОМ. Нейрометаболические стимуляторы (пикамилон и нооклер) и функциональное состояние зрительного анализатора у больных с невротическими расстройствами. Автореф. дис.... канд.мед. наук, 1997.
20. Медведев В.Э., Албантова К.А. Пантогам-актив при лечении невротических, связанных со стрессом и соматоформных расстройств у больных кардиологического стационара. Психич. расстройства в общей медицине. 2009; 2:40-3.
21. Медведев В.Э. Мексидол в психиатрической практике. Психиатр. и психофармакотер. 2010; 4:18-21.
22. Морозов П.В. Новый отечественный ноотропный препарат Нооклерин (обзор). Психиатр. и психофармакол. 2003; 5 (6): 262-7.
23. Морозова МА, Михеев М.Ю. Отчет РГЦ экспертизы лекарств, 1999.
24. Нооклерин - новый отечественный ноотроп (научный обзор). М., 2002.
25. Попов Ю.В. Применение Нооклерина у подростков в качестве антиастенического средства. Психиатр. и психофармакотер. 2004; 4.
26. Сейфулла Р.Д., Кондратьева И.М. Отчет ТОО Бифарм, СВАО г. Москва, 1999.
27. Скачилова С.Я., Желтухин Н.К., Сернов Л.Н. и др. Твердая дозированная лекарственная форма, повышающая физическую и умственную работоспособность. Патент на изобретение. М., 2006.
28. Соколовская Л.В. Астения - типология, динамика (пограничные состояния и эндогенные заболевания). Автореф. дис.... канд. мед. наук. М., 1991.
29. Сухотина Н.К., Крыжановская И.Л., Коновалова В.В. и др. Опыт применения ноотропов при пограничных психических расстройствах у детей. Психиатр. и психофармакотер. 2004; 6.
30. Шакирова И.Н., Дюкова Г.М. Астения - междисциплинарная проблема. Трудный пациент. 2012; 5.
31. Danysz A, Smieta ski J, Panek W. The influence of 2-dimethylami nethanol (DMAE) on the mental and physical efficiency in man Act Nerv Super Praha 1967; 9 (4): 417.
32. Dimpfel W, Wedekind W, Keplinger I. Efficacy of dimethylaminoet hanol (DMAE) containing vitamin-mineral drug combination on EEG patterns in the presence of different emotional states. Eur J Med Res 2003; 30; 8 (5): 183-91.
33. Dormard Y, Levron JC, Benakis A. Pharmacokinetic study of maleate acid of 2-(N,N-dimethylaminoethanol-14C1)-cyclohexylpro pionate (cyprodenate) and of N,N-dimethylaminoethanol-14C1 in animals. Arzneimittelforschung 1975; 25 (2): 194-201.
34. Lemere F, Lasater JH. Deanol (deaner) a new cerebral stimulant for the treatment of neurasthenia and mild depression: a preliminary report. Am J Psychiat 1958; 114 (7): 655-6.
35. Levin ED, Rose J.E., Abood L. Effects of nicotinic dimethylaminoethyl esters on working memoryperformance of rats in the radial-arm maze. Pharmacol Biochem Behav 1995; 51 (2-3): 369-73.
36. Levine LJ. 2-dimethylaminoethanol bitartrate in depressive illnesses and chronic schizophrenia. Lancet 1960; 17:653.
37. Lohr J,Acara M. Effect of dimethylaminoethanol, an inhibitor of betaine production, on the disposition of choline in the rat kidney. J Pharmacol Exp Ther 1990; 252 (1): 154-8.
38. Malanga G, Aguiar MB, Martinez HD, Puntarulo S. New insights on dimethylaminoethanol (DMAE) features as a free radical scavenger. Drug Metab Lett 2012; 6 (1): 54-9.
39. Miller E. Dimethylanminoethanol in the treatment of blepharospasm. New England J Med 1973; 289 (13): 697.
40. Moriarty J.D., Mebane J.C. Clinical uses of deanol (Deaner): a new type of psychotropic drug. Am J Psychiat 1959; 115 (10): 941 -2.
41. Pennington VM. Clinical results with the use of deanol (Deaner) in schizophrenia. Am J Psychiat 1959; 116:165-6.
| Июнь 2014 г. |