Опубликовано в: "Circulation" 2001г.;№103; С.919-925.Эффективность рамиприла и витамина Ε при атеросклерозе.
Исследование SECURE.
Effects of Ramipril and Vitamin E on Atherosclerosis
The Study to Evaluate Carotid Ultrasound Changes in Patients Treated With
Ramipril and Vitamin E (SECURE)
Lonn E.M., Yusuf S., Dzavik V., Doris C.I., Yi Q., Smith S.,
Moore-Cox A., Bosch J., Riley W.A., Teo K.K. от исследователей SECURE
Введение. Активация ренин-ангиотензин-альдостероновой системы и окислительная модификация липопротеидов низкой плотности (ЛПНП) играют важную роль в развитии атеросклероза. В проспективном двойном слепом исследовании SECURE с факториальным дизайном 3х2 (проводилось в рамках HOPE) изучались эффекты длительной терапии ингибитором ангиотензинпревращающего фермента рамиприлом и витамином Ε на прогрессирование атеросклероза у больных высокого риска.
Методы и результаты. Были рандомизированы 732 больных в возрасте ≥55 лет, у которых имелись сосудистые заболевания или сахарный диабет в сочетании с еще по крайней мере одним фактором риска, но отсутствовали сердечная недостаточность или низкая фракция выброса левого желудочка. Им назначали рамиприл в дозах 2,5 или 10 мг/сут или витамин Ε (RRR-α-токоферола ацетат) или соответствующее плацебо. Средняя длительность наблюдения составила 4,5 года. Прогрессирование атеросклероза оценивали с помощью ультразвукового исследования сонной артерии. Средняя скорость увеличения максимальной толщины интимы-медии сонной артерии составила 0,0217 мм в год в группе плацебо, 0,0180 мм в год в группе рамиприла 2,5 мг/сут и 0,0137 мм в год в группе рамиприла 10 мг/сут (р=0,033). Скорость прогрессирования атеросклероза при применении витамина Ε не отличалась от таковой при приеме плацебо.
Заключение. Длительная терапия рамиприлом оказывает благоприятное влияние на прогрессирование атеросклероза, в то время как витамин Ε не оказывает на него действие.
Circulation 2001;103:919-925.
Экспериментальные и эпидемиологические данные свидетельствуют о том, что активация ренин-ангиотензин-альдос-тероновой системы и окислительная модификация холестерина липопротеидов низкой плотности (ЛПНП) играют важную роль в ате-рогенезе, а длительная терапия ингибитором АПФ или антиоксидантом витамином Ε может оказаться полезной [1,2]. Влияние этих препаратов на развитие атеросклероза у человека изучалось в ограниченном числе рандомизированных исследований. В связи с этим мы провели проспективное рандомизированное клиническое исследование с целью оценки эффектов рамиприла и витамина на развитие атеросклероза. Исследование SECURE проводилось в рамках исследования HOPE, в котором изучалась эффективность этих препаратов в профилактике сердечно-сосудистых осложнений у 9541 больного [3,4].
Методы
Дизайн и характеристики исследования были подробно описаны ранее [5]. Приводится краткое резюме.
Больные
В исследование HOPE и его субисследование SECURE включали пациентов с высоким риском развития сердечно-сосудистых осложнений [3-5]. Набор больных проходил с декабря 1993 г по август 1995 г в 6 канадских центрах. Два из них имели опыт в области двухмерной эхографии сонной артерии. В исследования включали больных в возрасте ≥55 лет, у которых имелись сосудистые заболевания или сахарный диабет в сочетании с еще по крайней мере одним сердечно-сосудистым фактором риска и были зарегистрированы адекватные изображения при исходной эхографии сонных артерий. Критерием адекватности служила возможность точного измерения толщины интимы-медии сонной артерии минимум в 4 заранее выбранных участках. Критериями исключения были сердечная недостаточность, снижение фракции выброса левого желудочка менее 40%, инфаркт миокарда, нестабильная стенокардия или инсульт в течение предыдущего месяца, терапия ингибитором АПФ или витамином Е, неконтролируемая гипертония (>160/100 мм рт. ст.), явная нефропатия или серьезные заболевания, которые могли помешать участию в исследовании. Все пациенты дали письменное информированное согласие, а протокол исследования был утвержден этическими комитетами всех центров.
Дизайн исследования, рандомизация, терапия и наблюдение
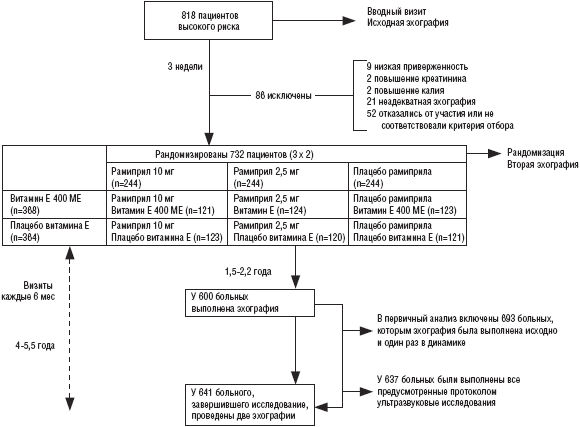
SECURE было рандомизированным двойным слепым параллельным исследованием с факториальным дизайном 3х2. При вводном визите оценивали критерии отбора и проводили исходную эхографию (рис.). Пациентов, отвечавших критериям отбора, включали в вводную фазу, во время которой они принимали ра-миприл в дозе 2,5 мг/сут (простым слепым методом) в течение 7-10 дней. Затем измеряли сывороточные уровни креатинина и калия и назначали плацебо рамиприла на 10-14 дней. Из 818 больных, включенных в вводную фазу, 86 были исключены из исследования в течение 3 недель, а оставшиеся 732 пациента были рандо-мизированы. Им назначали рамиприл в дозах 10 или 2,5 мг/сут, витамин Ε (RRR-α-токоферо-ла ацетат) или плацебо рамиприла и витамина Ε и проводили второе исходное ультразвуковое исследование. В группе рамиприла 10 мг/сут проводили форсированное титрование дозы до целевой или максимальной переносимой в течение 1 мес.
Пациентов обследовали через 1 месяц после рандомизации, а затем каждые 6 месяцев. Все визиты и ультразвуковые исследования были завершены к 1 июля 1999 г. Систолическое и ди-астолическое АД измерялось опытными медицинскими сестрами во время рандомизации, через 1 месяц, 2 года и в конце исследования с помощью стандартного сфигмоманометра по стандартному протоколу (измерение проводили в утренние часы, в то время как препарат пациенты принимали вечером, использовали манжету адекватного размера, пациенты находились в положении лежа ≥5 минут, после чего АД регистрировали дважды на каждой руке; определяли среднее значение минимальных показателей на правой и левой руке).
Секторальная эхография
Исходно и в конце исследования (через 4-5 лет после рандомизации; медиана 4,5 года) дважды проводили эхографию сонных артерий (с интервалом максимум 3 недели), а через 1,5-2,2 года после рандомизации выполняли однократное ультразвуковое исследование. Методика исследования подробно описана ранее [5]. Высокочастотную эхографию проводили 3 опытных и сертифицированных специалиста. Использовали стандартизованный протокол исследования и интерпретации изображений [6,7]. В продольной проекции регистрировали максимальную толщину интимы-медии (ТИМ) в каждом из 12 сегментов сонной артерии длиной 1 см (внутренняя сонная артерия, бифуркация, общая сонная артерия). Анализ изображений проводился двумя сертифицированными специалистами слепым методом. Для каждого больного рассчитывали среднюю максимальную ТИМ на основании значений в 12 сегментах. Разница средней максимальной ТИМ между 732 парными исходными измерениями составила 0,014±0,17 мм, средняя абсолютная разница - 0,12±0,11 мм, коэффициент корреляции Пирсона — 0,87. В конце исследования средняя разница средней максимальной ТИМ между 641 парным измерением составила 0,004±0,09 мм, средняя абсолютная разница -0,06±0,06 мм, коэффициент корреляции - 0,97. При детальном анализе меж- и интраиндивиду-альной вариабельности была продемонстрирована высокая воспроизводимость результатов и отсутствие ее изменений со временем.
Конечные точки
Первичной конечной точкой исследования была ежегодная скорость увеличения средней максимальной ТИМ. Вторичной конечной точкой служила ежегодная скорость увеличения максимальной ТИМ в отдельных сегментах сонной артерии. В рамках исследования HOPE регистрировали и анализировали также клинические исходы. Это исследование обладало достаточной силой для изучения влияния двух препаратов на риск сердечно-сосудистых осложнений.
Статистический анализ
Анализ проводили в выборке больных, начавших лечение, с помощью программы SAS 6.12. При анализе первичной и вторичной конечной точки не было выявлено взаимодействия между двумя препаратами (р=0,90 ир=0,61 соответственно; метод ANOVA). В связи с этим оценивали разницу между рамиприлом в целом и в разных дозах и плацебо, а также между витамином Ε и соответствующим плацебо. Исходные характеристики сравнивали с помощью метода ANOVA и критерия хи-квадрат. Скорость увеличения средней максимальной ТИМ и максимальной ТИМ в отдельном сегменте для каждого больного рассчитывали на основании результатов серии исследований с помощью метода регрессии (после подтверждения отсутствия значимого отклонения от линейности). Общий эффект рамиприла, эффекты каждой дозы ра-миприла (2,5 и 10 мг) и витамина Ε анализировали с помощью метода ANOVA. Скорость увеличения средней максимальной ТИМ служила зависимой переменной, а проводимая терапия — независимой. С помощью метода ANCOVA проводили анализ с поправкой на изменения систолического и диастолического АД и поправкой на множественные факторы, которые оказывали влияние на скорость увеличения ТИМ по данным однофакторного анализа. С целью поправки на использование одного контроля для сравнения двух доз рамиприла использовали метод Даннета [8]. В первичный анализ включали всех больных, у которых можно было оценить динамику ТИМ, т.е. при наличии двух исходных ультразвуковых исследований и по крайней мере одного исследования в динамике.
Результаты
Исходные характеристики, наблюдение и приверженность
Исходные характеристики не отличались между группами сравнения, за исключением частоты курения, которая была выше в группе больных, получавших витамин Ε (табл. 1). Исходные характеристики 693 больных, которые были включены в первичный анализ в конце исследования, были сходными.
ТАБЛИЦА 1. Исходные характеристики (М±о)
* р<0.05.
Рамиприл Витамин E Показатель плацебо (n=244) 2,5 м г/сут (n=244) 10 м г/сут (n=244) плацебо (n=364) витамин Ε (n=368) Возраст, лет 65.6±6.8 65.6±6.865 65.2±6.2 65.7±6.6 65.0±6.4 Женщины, % 21 27 24 24 23 АД, мм рт. ст. 132±17/75±9 132±17/76±10 132±15/76±9 132±17/76±9 132±17/76±9 Частота сердечных сокращений в минуту 66±11 66±11 66±11 66±11 66±11 Индекс массы тела, кг/м2 28±4 28±4 28±4 28±5 28±5 Анамнез, % Коронарная болезнь сердца 85 87 81 85 84 Инфаркт миокарда 55 58 57 58 55 Стабильная стенокардия 64 65 54 62 60 Нестабильная стенокардия 34 34 30 34 32 Инсульт или транзиторная ишемическая атака 10 7 12 10 10 Периферический атеросклероз 42 39 38 37 41 Гипертония 34 35 40 35 37 Диабет 35 32 35 32 36 Курение в настоящее время 9 10 10 9 11 в настоящее время или в прошлом 74 75 76 70 80* Повышение общего холестерина 48 46 47 46 48 Снижение холестерина ЛПВП 18 16 19 18 17 Сопутствующая терапия, % Бета-блокаторы 43 40 44 43 42 Аспирин/другие антиагреганты 86 85 82 85 83 Гиполипидемические средства 35 39 29 37 32 Диуретики 8 11 9 10 8 Антагонисты кальция 44 43 40 40 45 Витамин С 8 10 11 9 11 Бета-каротин 1 1 2 1 2 Поливитамины 11 12 6 10 9 Гормональная заместительная терапия у женщин 2 3 3 3 3 Лабораторные показатели, ммоль/л Общий холестерин 5.3±1.2 5.3±1.0 5.3±1.0 5.3±1.0 5.3±1.25.3±1 Триглицериды 2.2±1.3 2.2±1.3 2.2±1.3 2.2±1.4 2.2±1.32 Холестерин ЛПВП 1.0±0.3 1.0±0.3 0.9±0.3 0.9±0.3 1.0±0.3 Холестерин ЛПНП 3.5±1.1 3.5±1.1 3.4±0.8 3.4±0.8 3.5±1.13.4±0 ТИМ сонной артерии, мм средняя максимальная 1.1462±0.34 1.1477±0.34 1.1603±0.32 1.1477±0.341.1603 1.1564±0.33 максимальная 2.2653±0.92 2.2559±0.84 2.2±7860.79 2.2883±0.89 2.2379±0.81 Наблюдение было завершено у всех больных. Через 1,5-2,2 года после рандомизации адекватные эхограммы были зарегистрированы у 690 больных. 17 из 732 больных, включенных в исследование, умерли, 15 пропустили эхографию из-за болезни, а 10 пациентов отказались от исследования или у них не удалось зарегистрировать качественное изображение. У 3 больных эхография не была проведена через 1,5-2,2 года, однако была выполнена в конце исследования. Таким образом, в первичный анализ были включены 693 больных (95% из всех рандомизированных пациентов и 97% из всех рандомизированных пациентов, которые были живы через 1,5-2,2 года после рандомизации). У 637 пациентов были выполнены все 5 запланированных ультразвуковых исследования (87% из всех рандомизированных больных и 95% больных, которые были живы к концу исследования; см. схему).
Сведения о приверженности к проводимой терапии приведены в табл. 2. Только кашель был более частой причиной отмены рамиприла по сравнению с плацебо (1,6% в группе плацебо рамиприла, 9,0% в группе рамиприла 2,5 мг и 9,8% в группе рамиприла 10 мг). Витамин Ε не вызывал выраженных побочных реакций.
ТАБЛИЦА 2. Приверженность больных лечению
Указан процент больных, принявших >80% доз исследуемых препаратов. * Частота применения ингибитора АПФ открытым методом во время исследования составила 15,7% в группе больных, получавших плацебо рамиприла, 13,5% в группе рамиприла 2,5 мг/сут и 13,3% в группе рамиприла 10 мг/сут. ** Частота применения витамина Ε открытым методом составила 6,2% в группе плацебо витамина Ε и 5,5% в основной группе.
Рамиприл* Витамин E** Год плацебо 2,5 мг/сут 10 мг/сут плацебо витамин Ε 1 93 88 85 94 95 2 85 80 79 91 95 3 81 76 74 90 90 4 76 73 69 89 88 Конец исследования 72 71 67 86 90 Изменения АД
Во всех группах АД исходно составляло в среднем 132/76 мм рт. ст. При лечении рами-прилом в обеих дозах было отмечено снижение систолического и диастолического АД по сравнению с плацебо, в то время как динамика АД достоверно не отличалась между группами рамиприла 2,5 и 10 мг/сут (табл. 3). Витамин Ε не оказывал существенного влияния на АД.
ТАБЛИЦА 3. Систолическое и диастолическое АД (мм рт. ст.) до и после лечения рамиприломм (Μ±σ)
* p<0.001; f p<0.01; ** p<0.05 по сравнению с динамикой АД в группе плацебо. Динамика АД у больных, получавших рамиприл в двух разных дозах, достоверно не отличалась.
Исходно
1 мес
2 года
Конец исследования
Средняя динамика
Систолическое
Плацебо
131.6±17.1
130.4±17.9
130.0±15.8
134.1±16.9
0.1 ± 12.2
Рамиприл 2,5 мг/сут
131.7±17.0
12±.1 ± 17.0*
125.2±15.6*
130.8±16.7**
-4.6±13.5*
Рамиприл 10 мг/сут
131.9±15.3
127.1±14.8f
125.9±17.8f
130.5±16.6**
-4.1 ± 12.4*
Диастолическое
Плацебо
75.4±8.7
76.4±9.6
74.8±9.8
73.4±8.7
-0.4±7.3
Рамиприл 2,5 мг/сут
76.4±9.3
74.4±9.3*
73.0±9.6f
72.7±9.0
-2.9±7.9*
Рамиприл 10 мг/сут
76.2±9.2
74.8±8.7f
72.6±9.1*
72.6±8.9
-2.8±7.6*
Прогрессирование каротидного атеросклероза
По данным однофакторного анализа, на скорость увеличения средней максимальной ТИМ оказывали влияние следующие характеристики: исходная средняя максимальная ТИМ (р=0,0002), высокий уровень холестерина в анамнезе (р=0,0002) или низкий уровень холестерина липопротеидов высокой плотности (ЛПВП) (р=0,0008), концентрации общего холестерина и холестерина ЛПНП (р=0,03 и р=0,01 соответственно) и распределение в группу рамиприла 10 мг/сут (р=0,028). По данным многофакторного анализа, только исходная средняя максимальная ТИМ (р<0,001), дисли-пидемия в анамнезе (р=0,0005) и лечение рами-прилом 10 мг/сут (р=0,046) были независимыми предикторами скорости увеличения средней максимальной ТИМ.
Основные результаты исследования обобщены в табл. 4. Число сегментов сонной артерии, в которых не удалось измерить ТИМ, было низким (в среднем 5%), поэтому первичный анализ проводили без коррекции на отсутствующие данные. Рамиприл в целом снижал ежегодную скорость увеличения средней максимальной ТИМ по сравнению с плацебо (р=0,033). Рамиприл в дозе 10 мг/сут также превосходил плацебо (р=0,028; при коррекции Даннетар=0,027).
ТАБЛИЦА 4. Скорость прогрессирования первичной и вторичной эхографической конечной точки (мм в год) у 693 больных (М±m)*
* Скорость увеличения средней максимальной ТИМ (мм в год) в 6 рандомизационных "клетках" была следующей: двойное плацебо 0.0205±0.0039; плацебо витамина Е/рамиприл 2,5 мг/сут 1.0184±0.0035; плацебо витамина Е/рамиприл 10 мг/сут 0.0135±0.0030; витамин Е/плацебо рамиприла 0.0229±0.0038; витамин Е/рамиприл 2,5 мг/сут 0.0175±0.0039; витамин Е/рамиприл 10 мг/сут 0.01385±0.0038. p=0.18 для витамина Е/рамиприла 10 мг/сут (n=115) по сравнению с двойным плацебо (n=114).
Показатель Рамиприл! Витамин E плацебо (n=227) 2.5 мг/сут (n=232) 10 мг/сут (n=234) плацебо (n=344) витамин Ε (n=349) Средняя максимальная ТИМ Максимальная ТИМ 0.0217±0.0027 0.0277 ±0.0075 0.0180±0.0026 0.0280±0.0096 0.0180±0.0022 0.00760.0277 0.0174±0.0020 0.0141±0.0076 0.0180±0.00260.0137±0.002 0.0277±0.0075
t Рамиприл вызывал снижение скорости увеличения средней максимальной ТИМ; р=0,033 (p=0.043 после поправки на изменения систолического и диастолического АД и р=0.046 после поправки на множественные факторы [возраст, пол, исходный ИМТ, высокий общий холестерин и низкий холестерин ЛПВП, курение, терапия гиполипидемическими средствами, гипертония, изменения АД и исходные концентрации общего холестерина и холестерина ЛПНП]).
φ p=0.028 рамиприл 10 мг/сут в сравнении с плацебо (р=0.037 после поправки на изменения АД и р=0.046 после поправки на множественные факторы)Мы проверили надежность наших результатов с помощью дополнительных тестов. При анализе 711 больных, в том числе включенных в первичный анализ, и 18 больных, которые умерли во время исследования или перенесли инфаркт миокарда или инсульт (у этих пациентов не проводили ультразвуковое исследование в период наблюдения; у них предполагали наличие быстрого прогрессирования атеросклероза, критерием которого служил верхний 10-й перцентиль средней максимальной ТИМ для всей выборки SECURE), выявлено снижение скорости прогрессирования атеросклероза при лечении рамиприлом по сравнению с плацебо (р=0,019; р=0,027 при внесении поправки на изменения АД и р=0,027 при внесенные поправки на множественные факторы) и рамиприлом в дозе 10 мг/сут по сравнению с плацебо (р=0, 015, р=0,022 при внесении поправки на изменения АД ир=0,031 при внесении поправки на множественные факторы). Сходная тенденция была отмечена при анализе 637 больных, которым были выполнены все 5 ультразвуковых исследований (р=0,068 для рамиприла во всех дозах в сравнении с плацебо ир=0,055 для рамиприла 10 мг/сут в сравнении с плацебо). Похожие результаты были получены при анализе вторичной конечной точки (скорость увеличения максимальной ТИМ в одном сегменте). Абсолютная разница этой конечной точки между группами рамиприла 10 мг/сут и плацебо превышала разницу скорости увеличения средней максимальной ТИМ, однако она не достигла статистической значимости из-за более высокой вариабельности этого показателя. По данным анализа 637 больных, которым были выполнены все 5 ультразвуковых исследований, рамиприл значительно снижал скорость увеличения максимальной ТИМ в одном сегменте (р=0,003 для рамиприла во всех дозах в сравнении с плацебо и р=0,008 для рамиприла 10 мг по сравнению с плацебо).
Витамин Ε не оказывал влияния на первичную и вторичную конечные точки.
Клинические исходы
Как и ожидалось, в этом относительно небольшом исследовании частота первичной клинической конечной точки (комбинация сердечно-сосудистой смерти, инфаркта миокарда и инсульта) достоверно не отличалась между группами. Ее зарегистрировали у 41 (16,8%) больного группы плацебо, 34 (13,9%) больных группы рамиприла 2,5 мг, 31 (12,7%) больного группы рамиприла 10 мг/сут, 55 (15,1%) больных группы плацебо витамина Ε и 51 (13,9%) больного группы витамина Е. Влияние лечения на клинические конечные точки было продемонстрировано в исследовании HOPE, которое обладало достаточной статистической силой [3,4].
Обсуждение
Исследование SECURE показало, что длительная терапия ингибитором АПФ задерживает прогрессирование атеросклероза, в то время как витамин Ε не оказывает на него действие.
В клинических исследованиях все чаще применяют секторальную эхографию сонных артерий для оценки эффектов различных средств на атеросклероз. Метод характеризуется высокой воспроизводимостью, а его результаты коррелируют с факторами риска и развитием коронарной болезни сердца и инсульта [9]. В предыдущих исследованиях применялись различные оборудование и протоколы сканирования и интерпретации изображений, а также выбирались разные конечные точки. В качестве первичной конечной точки мы измеряли среднюю максимальную ТИМ на основании изучения 12 сегментов сонной артерии, так как этот показатель лучше всего коррелирует с результатами корона-роангиографии у больных коронарным атеросклерозом [10]. Кроме того, он достаточно чувствителен и позволяет выявить изменения, возникающие под влиянием лечения [11]. Мы измеряли максимальную, а не среднюю ТИМ в сегменте, так как такой подход позволяет свести к минимуму пропуски данных, оценить наиболее измененные участки и получить очень стабильные результаты при расчете средних показателей в 12 сегментах артерий [7,11]. Процедура сканирования и интерпретации изображений тщательно валидирована [6,7], а нам удалось добиться высокой воспроизводимости измерений.
Лечение рамиприлом привело к уменьшению скорости прогрессирования атеросклероза. Этот эффект наблюдался у больных высокого риска, большинство из которых уже получали эффективные лекарственные средства, в том числе аспирин (84%), гиполипидемические препараты (34%), бета-блокаторы (43%), диуретики (9%), нитраты (32%) и антагонисты кальция (43%). Хотя абсолютная разница скорости прогрессирования атеросклероза между группами рамиприла и плацебо была небольшой, тем не менее относительное снижение средней максимальной ТИМ при лечении рамиприлом 10 мг/сут составило 37%, что сопоставимо со снижением относительного риска инсульта (на 32%) в исследовании HOPE. Сходные результаты были получены при изучении эффективности ги-похолестеринемических средств, которые оказывали впечатляющее влияние на риск сердечно-сосудистых осложнений, что свидетельствовало о стабилизации атеросклеротического процесса. Наше исследование не обладало статистической силой, необходимой для сравнения двух доз рамиприла. Однако была отмечена тенденция к зависимости эффекта препарата от дозы. Максимальную пользу приносила терапия рамиприлом в дозе 10 мг/сут. В этой же дозе рамиприл применялся в крупном исследовании HOPE, которое подтвердило благоприятный эффект препарата на риск различных сердечно-сосудистых осложнений [3].
Рамиприл оказывал небольшое гипотензивное действие в нашем исследовании, так как у большинства больных отсутствовала артериальная гипертония или она хорошо контролировалась; другие антигипертензивные и антианги-нальные средства применялись более чем у 75% больных. Благоприятный эффект рамиприла на атеросклероз оставался статистически значимым после поправки на наличие артериальной гипертонии и изменения АД. Это свидетельствовало о том, что результаты лечения нельзя полностью объяснить снижением АД, а они могут отражать прямое протективное действие рамиприла на сосуды.
В атеросклеротических поражениях коронарных артерий продемонстрирована повышенная тканевая активность АПФ [12], а длительное применение ингибиторов АПФ вызывало уменьшение площади атеросклеротических изменений аорты, сонных и коронарных артерий у нормо-тензивных животных [13,14]. Эти антиатероген-ные свойства могут быть связаны с ингибирова-нием образования ангиотензина II в тканях и циркуляции и увеличением уровней брадикини-на, вызывающим снижение пролиферации и миграции гладкомышечных клеток, накопления и активации воспалительных клеток, окислительного стреса и повышением образования оксида азота, улучшающего функцию эндотелия [1].
Ранее влияние ингибиторов АПФ на атеросклероз изучались в клинических исследованиях QUIET, SCAT и PART-2 [15-17]. В двух из них (QUIET и SCAT) с помощью коронарной ангиографии не был продемонстрирован благоприятный эффект квинаприла и эналаприла, хотя в исследовании QUIET было отмечено замедление прогрессирования коронарного атеросклероза при лечении квинаприлом в подгруппе больных с повышенным уровнем холестерина ЛПНП. Разница результатов SECURE и этих исследований может быть следствием выбора определенного ингибитора АПФ, дозы препарата, дизайна исследования и методов оценки прогрессирования атеросклероза. Эхография, которая использовалась в SECURE, позволяет изучить состояние стенки артерий и может быть более чувствительным методом, чем коронароан-гиография. В PART-2 рамиприл в дозах 5-10 мг/сут не оказывал влияния на ТИМ, которую измеряли с помощью ультразвукового исследования. Однако в этом исследовании оценивали только толщину общей сонной артерии. В исследовании SECURE рассчитывали средний показатель на основании изучения сегментов общей и внутренней сонной артерии и бифуркации.
Этот показатель может быть более чувствительным к изменениям [11], что позволяет объяснить разницу результатов двух исследований.
Витамин Ε в дозе 400 МЕ/сут не оказывал влияния на прогрессирование атеросклероза. Приверженность к лечению этим препаратом была высокой, другие антиоксидантные витамины использовались редко, а исследование обладало адекватной статистической силой, достаточной для выявления умеренного эффекта лечения (оно позволяло выявить снижение первичной конечной точки на 48% со статистической силой 80% и на 33% со статистической силой 50%). При рассчете размера выборки мы ориентировались на более высокую скорость увеличения ТИМ с учетом имевшихся на тот момент данных. В связи с этим исследование не позволяет полностью исключить небольшой эффект витамина Е.
Мы не измеряли уровни витамина Ε или его влияние на окисление ЛПНП. Однако в предыдущих исследованиях было показано, что применение витамина Е, полученного из естественных источников, в дозе 400 МЕ/сут приводит к значительному повышению содержания а-токо-ферола в плазме и тканях. В сходных или более низких дозах витамин Ε повышает устойчивость ЛПНП к окислению [18,19]. Сходные данные были получены в субисследовании HOPE (R.Hoeschen, 2000). Кроме того, целью нашего исследования было изучение эффектов витамина Е, который принимают миллионы людей в мире без оценки окислительного статуса.
Экспериментальные данные свидетельствуют о важной роли окислительной модификации ЛПНП в атерогенезе, а витамин Ε является эффективным антиоксидантом, который вызывал уменьшение атеросклероза в опытах на животных [2,20], хотя и не постоянно [21]. В эпидемиологическом исследовании было отмечено замедление прогрессирования коронарного атеросклероза у людей, принимающих витамин Ε [22]. Крупные эпидемиологические исследования продемонстрировали кардиопротективные свойства этого витамина. В исследовании Cambridge Heart Antioxidant Study было выявлено снижение числа несмертельных осложнений у больных, получавших витамин Ε после инфаркта миокарда [23], однако наблюдалась тенденция к увеличению смертности. В нескольких более крупных и длительных рандомизированных клинических исследованиях не подтверждена польза применения витамина Ε [4,24]. До настоящего времени влияние витамина Ε на атеросклероз изучалось в небольшом числе рандомизированных исследований. У15 больных с гомозиготной семейной гиперхолестеринемией наблюдалось быстрое увеличение ТИМ сонных артерий при лечении витамином Ε и ее уменьшение при применении статинов [25]. Предварительные результаты Antioxidant Supplementation in Atherosclerosis Prevention (ASAP) свидетельствуют об отсутствии благоприятного влияния на ТИМ сонных артерий витамина Ε по отдельности или в комбинации с витамином С у женщин, хотя отмечен эффект комбинированной терапии у курящих мужчин с гиперхолестеринемией [26].
Результаты исследования SECURE согласуются с результатами HOPE. В целом эти исследования свидетельствуют о том, что рамиприл замедляет прогрессирование атеросклероза и предупреждает развитие сердечно-сосудистых осложнений. Напротив, терапия витамином Ε в течение от 4 до 6 лет не оказывала существенного влияния на развитие атеросклероза или сердечно-сосудистых осложнений. Роль витамина Ε по отдельности или в комбинации с другими анти-оксидантами в различных группах пациентов нуждается в дополнительном изучении.
Литература
1. Lonn EM, Yusuf S, Jha P, et al. Emerging role of angiotensin-converting enzyme inhibitors in cardiac and vascular protection. Circulation. 1994; 90:2056 -2069.
2. Steinberg D, Parthasarathy S, Carew TE, et al. Beyond cholesterol: modifications of low-density lipoprotein that increase its atherogenicity. N Engl J Med. 1989;320:915-924.
3. The Heart Outcomes Prevention Evaluation Study Investigators. Effects of an angiotensin-converting enzyme inhibitor, ramipril, on death from cardiovascular causes, myocardial infarction, and stroke in high-risk patients. N Engl J Med. 2000;342:145-153.
4. The Heart Outcomes Prevention Evaluation Study Investigators. Effects of long-term vitamin E supplementation on cardiovascular events in 9541 high-risk persons. N Engl J Med. 2000;342:154-202.
5. Lonn EM, Yusuf S, Doris CI, et al. Study design and baseline characteristics of the Study to Evaluate carotid Ultrasound changes in patients treated with Ramipril and vitamin E (SECURE). Am J Cardiol. 1996;78: 914-919.
6. Riley WA, Barnes RW, Applegate WB, e al. Reproducibility of noninvasive ultrasonic measurement of carotid atherosclerosis: the Asymptomatic Carotid Artery Plaque Study. Stroke. 1992;23:1062-1068.
7. Pitt B, Byington RP, Furberg CD, et al. Effect of amlodipine on the progression of atherosclerosis and the occurrence of clinical events. Circulation. 2000;102:1503-1510.
8. Dunnett CW. A multiple comparisons procedure for comparing several treatments with a control. J Am Stat Assoc. 1955;50:1096-1121.
9. O'Leary DH, Polak JF, Kronmal RA, et al. Carotid-artery inti-ma and media thickness as a risk factor for myocardial infarction and stroke in older adults. N Engl J Med. 1999;340: 14-22.
10. Crouse JR, Craven TE, Hagaman AP, et al. Association of coronary artery disease with segment-specific intimal-medial thickening of the extracranial carotid artery. Circulation. 1995;92:1141-1147.
11. Espeland MA, Craven TE, Riley WA, et al. Reliability of longitudinal ultrasonographic measurements of carotid intimal-medial thickness. Stroke. 1996;27:480-485.
12. Diet F, Pratt RE, Berry GJ, et al. Increased accumulation of tissue ACE in human atherosclerotic coronary artery disease. Circulation. 1996;94: 2756-2767.
13. Chobanian AV, Haudenshild CC, Nickerson C, et al. Antiatherogenic effect of captopril in the Watanabe heritable hyperlipidemic rabbit. Hypertension. 1990;15:327-331.
14. Aberg G, Ferrer P. Effects of captopril on atherosclerosis in cynomolgus monkeys. J Cardiovasc Pharmacol. 1990; 15: S65-S72.
15. Cashin-Hemphill L, Holmvang G, Chan RC, et al. Angiotensinconverting enzyme inhibition as antiatheroscle-rotic therapy: no answer yet: Quinapril Ischemic Event Trial. Am J Cardiol. 1999;83:43- 47.
16. Teo KK, Burton JR, Buller CE, et al. Long term effects of cholesterol lowering and angiotensin-converting enzyme inhibition on coronary atherosclerosis: the Simvastatin/Enalapril Coronary Atherosclerosis Trial (SCAT). Circulation. 2000;102:1748 -1754.
17. MacMahon S, Sharpe N, Gamble G, et al. Randomized, placebocontrolled trial of the angiotensin converting enzyme inhibitor, ramipril, in patients with coronary or occlusive arterial disease. J Am Coll Cardiol. 2000;36:438-443.
18. Burton GW, Traber MG, Acuff RV, et al. Human plasma and tissue α-tocopherol concentrations in response to supplementation with deuterated natural and synthetic vitamin E. Am J Clin Nutr. 1998;67: 669-684.
19. Devaraj S, Adams-Huet B, Fuller CJ, Jialal I. Dose-response comparison of RRR-α-tocopherol and all-racemic a-toco-pherol on LDL oxidation. Arterioscler Thromb Vasc Biol. 1997;17:2273-2279.
20. Verlangieri AJ, Busch MJ. Effects of d-alpha-tocopherol supplementation on experimentally induced primate atherosclerosis. J Am Coll Nutr. 1992; 11:131-138.
21. Godfried SL, Combs GF, Saroka JM, et al. Potentiation of atherosclerotic lesions in rabbits by a high dietary level of vitamin E. Br J Nutr. 1989;61:607- 617.
22. Hodis HN, MackWJ, LaBree L, et al. Serial coronary angiographic evidence that antioxidant vitamin intake reduces progression of coronary atherosclerosis. JAMA. 1995;85: 1483-1492.
23. Stephens NG, Parsons A, Schofield PM, et al. Randomized controlled trial of vitamin E in patients with coronary disease: Cambridge Heart Antioxidant Study (CHAOS). Lancet. 1996;347:781-776.
24. GISSI-Prevenzione trial. Dietary supplementation with n-3 polyunsaturated fatty acids and vitamin E after myocardial infarction: results of the GISSI-Prevenzione trial. Lancet. 1999;354:447- 445.
25. Raal FJ, Pilcher GJ, Veller MG, et al. Efficacy of vitamin E compared with either simvastatin or atorvastatin in preventing the progression of atherosclerosis in homozygous familial hypercholesterolemia. Am J Cardiol. 1999;84:1344 -1346. 26. Salonen JT, NyyssЪnen K, Salonen R, et al. Antioxidant Supplementation in Atherosclerosis Prevention (ASAP) study: a randomized study of the effects of vitamins E and C on 3-year progression of carotid atherosclerosis. J Intern Med. 2000;248:377-386.
| Октябрь 2007 г. |