Опубликовано в журнале:
Clinical Surgery and Neurosurgery »» 105 (2003):241-244.Клинические критерии для смены тактики лечения болезни Паркинсона
Schoenfeld MAa*, Pantelie CM.б, Schwartz B
а – II неврологическое отделение, Магдебургский университет, Магдебург;
б – неврологическая клиническая практика, Дуйсбург, ГерманияПо прошествии многих лет применения препаратов леводопы для лечения болезни Паркинсона оказалось, что через 5-10 лет терапии, как правило, появляются побочные эффекты. Это привело к разработке современных критериев терапии впервые выявленных пациентов, которые учитывают, главным образом, возраст, а также на общей стратегии как можно дольше откладывать терапию леводопой. Однако этот практический подход недостаточно научно обоснован. В ретроспективном исследовании были проанализированы данные по 155 пациентам с болезнью Паркинсона, с целью поиска клинического маркера той критической временной точки, когда необходимо назначать препарат леводопы. Клинические стадии заболевания определяли по Hoehn и Yahr, а тяжесть симптомов – по баллу шкалы UPDRS. Полученные результаты показывают, что возраст пациентов и терапия леводопой (назначена или нет) не коррелируют с клиническими исходами. Однако была обнаружена достоверная связь между клинической стадией по Hoehn и Yahr и терапией. Дальнейший анализ этой связи показал, что при 1 – 2.5 стадиях по Hoehn и Yahr баллы UPDRS были ниже у больных, не получавших лечение леводопой. Примечательно, что на стадиях 3 и более по Hoehn и Yahr баллы шкалы UPDRS были ниже, напротив, на фоне приема леводопы. Эти результаты позволяют предполагать, что клиническая стадия заболевания по Hoehn и Yahr может быть лучшим критерием для назначения леводопы впервые выявленным больным, чем возраст.
Ключевые слова: Parkinson syndrome, L-dopa, Dopamine agonists, Treatment strategy.
1. Введение
Синдром Паркинсона часто встречается в клинической практике невролога. Хотя его диагноз обычно не представляет проблемы для опытного врача, выбор реальной терапевтической тактики сопряжен с большими ошибками и затруднениями. В последние два десятилетия мы узнали, что применение «золотого стандарта» – терапии леводопой – сопровождается важными побочными эффектами, такими как дискинезии, феномен «включения-выключения» и т.д. Эти побочные эффекты возникают, как правило, через 5-10 лет после начала лечения леводопой и могут отмечаться почти у 80% пациентов. Подобные проблемы особенно выражены у молодых больных, которым лечение леводопой требуется на протяжении десятилетий.
Было очевидно, что длительная терапия препаратами леводопы приводит к описанным выше феноменам и по прошествии лет снижает свою эффективность. Этот факт, а также создание агонистов дофамина потребовали разработки новых подходов к лечению. Одним из первых возник вопрос – каких больных нужно лечить только агонистами. Rinne (1-3) изучали эффективность монотерапией препаратами, которые существовали в то время (бромкриптин, лизурид, перголид), и обнаружили, что эффективность длительной терапии впервые выявленных пациентов этими препаратами была ограниченной. Кроме того, частота побочных эффектов была выше, а клинические результаты - хуже, чем при лечении препаратами леводопы. В других исследованиях (4-7) было установлено, что раннее назначение комбинированной терапии леводопой и агонистами дофамина уменьшало частоту возникновения дискинезий и флуктуаций в отдаленном периоде. Из-за побочных эффектов длительной монотерапии препаратами леводопы и недостаточной эффективности монотерапии агонистами дофамина стало ясно, что лечение следует проводить обоими типами препаратов одновременно. Тогда ключевым вопросом стал следующий: как именно это нужно делать?
Общая гипотеза заключалась в том, что лечение надо начинать только с агонистов дофамина, а несколько позже добавлять препараты леводопы. Вот почему во многих исследованиях (8-15) было предложено назначать лечение в зависимости от возраста больных. В соответствии с этой тактикой, молодым пациентам следовало вначале назначать агонисты, а пациентам более старшего возраста (старше 65 лет) – комбинированную терапию или монотерапию леводопой. Преимущество такого подхода заключается в том, что его легко применять в клинической практике. Однако эта «повозрастная» тактика лечения ставит важные проблемы. Она не принимает во внимание многие важные факторы заболевания, такие как коморбидность, степень тяжести клинической симптоматики и когнитивного дефицита.
Самым важным фактором для выбора любого лечения какого-либо заболевания является клинический результат. В настоящем исследовании мы изучали клинический параметр – стадию заболевания по Hoehn и Yahr (в сравнении с возрастом) - как критерий для выбора терапевтической тактики у впервые выявленных пациентов. Поскольку этот параметр оценивается по стандарту, его будет легко применять в клинической практике, так же, как и возраст.
2. Методы
В ретроспективном исследовании мы проанализировали данные 155 больных, обратившихся в неврологическую клиническую практику. Все пациенты в исследовании были обследованы одним и тем же исследователем. Мы сравнили клинические исходы, которые оценивались с помощью стандартного балла шкалы UPDRS после монотерапии агонистами дофамина и после монотерапии леводопой / комбинированной терапии леводопой и агонистами дофамина. Диагноз синдрома Паркинсона ставился по наличию двух основных симптомов (гипертонус мышц, тремор, брадикинезия, постуральные нарушения). Экстрапирамидные симптомы, вызванные другими заболеваниями центральной нервной системы, исключали с помощью клинического обследования и нейрорентгенологических методов (КТ, МРТ). Возраст пациентов колебался от 40 до 80 лет, большинство больных, однако, попадали в возрастной диапазон 60-69 лет. Около 60% больных были женского пола, продолжительность заболевания колебалась от 1 до 20 лет. Больных разделили на две группы, в зависимости от вида терапии (леводопа/комбинированная терапия леводопой и агонистом дофамина или только агонисты дофамина). 77 пациентов вошли в группу без леводопы, 78 – в группу с леводопой. Каждую группу разделили на 6 подгрупп, в зависимости от стадии по Hoehn и Yahr (стадии 1, 1.5, 2, 2.5, 3 и 4). Больных со стадией 5 исключали, так как таких больных, не принимавших леводопу, было мало. Таким образом, были составлены 12 различных групп (таблица 1). Статистический анализ проводили с помощью программы SPSS 7.5. Группы сравнивали методом вариантного анализа (ANOVA). Для факторов с более чем тремя уровнями применяли поправку Бонферрони.
3. Результаты
Баллы шкалы UPDRS проанализировали с помощью трехфакторного метода ANOVA, где факторами служили вид терапии (леводопа в сравнении с отсутствием леводопы), клиническая стадия по Hoehn и Yahr (стадии 1, 1.5, 2, 2.5, 3 и 4) и возрастная группа (шесть групп от 30 до 90 лет). Вид терапии существенно не влиял на исход (F(1.5) = 0.435, p > 0.05). Был установлен достоверный эффект возраста (F(1.5) = 2.433, p =0.02), отражавший более высокие баллы шкалы UPDRS у пациентов старшего возраста. Главный эффект клинической стадии был высоко достоверным (F(1.5) = 166.31, p < 0.001). Достоверных взаимодействий между фактором возрастной группы и видом терапии найдено не было (F(1,6) = 1.406; р > 0.05), отсутствовали они также между возрастной группой и клинической стадией (F(1,6) = 1.342; р > 0.05). Однако, между факторами «вид терапии» и «клиническая стадия» была выявлена высоко достоверная связь (F(1,5) = 4.943; р < 0.001).
У пациентов со стадиями 1, 1.5, 2 и 2.5, не получавших леводопу, баллы шкалы UPDRS были ниже, чем у получавших леводопу. У больных со стадиями 3 и 4 эта зависимость принимала обратный характер: баллы шкалы UPDRS на фоне лечения леводопой были ниже, чем в отсутствие такой терапии (см. рисунок 1). По-видимому, выше описанная связь является причиной достоверного взаимодействия между факторами «вид терапии» и «клиническая стадия». Для дальнейшего изучения этого аспекта для каждой стадии заболевания в этих группах больных был проведен однофакторный ANOVA, в котором фактором являлся «вид терапии» (сравнение лечения леводопой с отсутствием такого лечения). На стадии 1 достоверных различий между терапевтическими группами не было (F(1,28) = 1.04; р > 0.05). Однако на стадии 1.5 достоверные различия между терапевтическими группами появлялись (F(1,19) = 5.02; р = 0.03), а на стадии 2 была обнаружена тенденция к статистически достоверной разнице (F(1,49) = 3.2; р = 0.08). На стадии 2.5 достоверных различий между терапевтическими группами не было (F(1,22) = 0.54; р > 0.05). На стадии 3 баллы шкалы UPDRS у пациентов, принимавших леводопу, становились ниже, чем у не принимавших, при высоко достоверной разнице (F(1,19) = 10.25; р = 0.003), несмотря на малое число больных в этих группах. На стадии 4 разница теряла статистическую значимость (F(1,14) = 2.05; р > 0.05), вероятно, из-за относительно малого числа пациентов.
Таблица 1.
В таблице представлены средние показатели шкалы UPDRS у больных с различными стадиями заболевания по Hoehn и Yahr, а также значения F и P, полученные в однофактором анализе ANOVA в двух терапевтических группах. N означает число пациентов в каждой подгруппе по стадиям по Hoehn и Yahr.
Стадия 1
Стадия 1.5
Стадия 2
Стадия 2.5
Стадия 3
Стадия 4
Группа агонистов
13.17
15.03
24.13
36.28
60
88.35
Группа леводопы
15.17
22.95
28.59
38.65
45.83
79.82
F
1.04
5.02
3.2
0.54
10.25
2.05
P
0.31
0.03
0.08
0.38
0.003
0.16
N
29
20
50
23
19
14
4. Обсуждение
В настоящем исследовании изучали результаты лечения, оцененные по шкале UPDRS, на фоне двух видов терапии болезни Паркинсона: монотерапии агонистами дофамина в сравнении с комбинированной терапией леводопой и агонистами дофамина. Полученные нами результаты показывают, что результаты лечения изменяются в зависимости от клинической стадии заболевания. На ранних стадиях (1 – 2.5) баллы по шкале UPDRS у пациентов, получающих монотерапию агонистами дофамина, были ниже, чем у тех, кто получал леводопу или леводопу в комбинации с агонистами дофамина. Начиная с 3 стадии, баллы по шкале UPDRS в группе пациентов, получавших леводопу или леводопу в комбинации с агонистами дофамина, были ниже, чем при монотерапии агонистами леводопы (см. рисунок 1).
Рисунок 1.
На рисунке показаны баллы по шкале UPDRS у пациентов двух изученных групп, в зависимости от стадии болезни по Hoehn и Yahr. Обращает внимание, что на ранних стадиях (1 – 2.5) баллы по шкале UPDRS выше у пациентов, получающих леводопу (черная линия). На более поздних стадиях (3-4) баллы по шкале UPDRS выше в группе пациентов, не получавших леводопу.
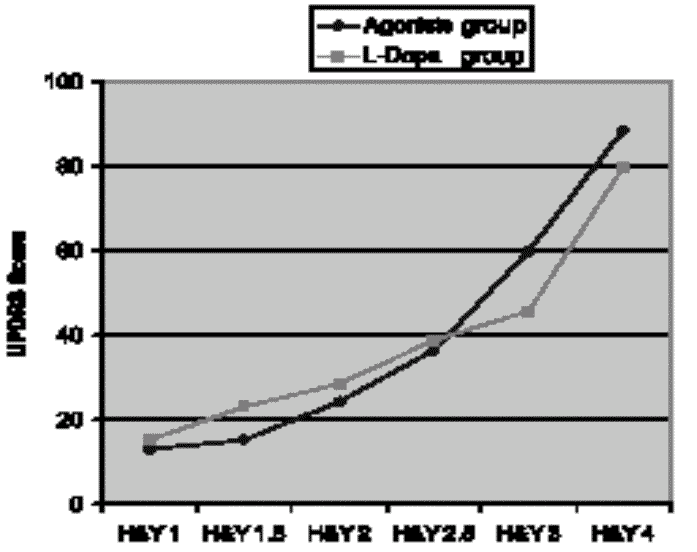
Ось у: Баллы по шкале UPDRS
Ось х: стадия 1 стадия 1.5 стадия 2 стадия 2.5 стадия 3 стадия 4
Надписи на рисунках: группа агонистов группа леводопыПри использовании большинства терапевтических подходов предполагается, что решение о выборе терапии (монотерапия агонистами дофамина или комбинированная терапия леводопой и агонистами дофамина) при болезни Паркинсона должно основываться на возрасте пациентов. Хотя этот подход легко и просто использовать, по-видимому, он не является наилучшим. В настоящем исследовании нам не удалось найти какую-либо связь между возрастом и типом терапии, которая бы повлияла на клинический результат лечения. Более того, было обнаружено, что намного лучшим критерием для принятия терапевтического решения, по-видимому, может служить стадия заболевания по Hoehn и Yahr.
Однако при интерпретации этих результатов необходимо помнить о возможных источниках ошибок. Во-первых, исследование проводилось на относительно небольшой группе пациентов с болезнью Паркинсона и делать из него выводы о лечении всех больных следует очень осторожно. Во-вторых, общепризнано, что возраст – не самый лучший критерий для выбора вида терапии. Этот показатель был предложен только потому, что в клинической практике его с легкостью могут использовать врачи, не являющиеся неврологами, в то время как неврологи так или иначе будут определять точную клиническую стадию заболевания. В-третьих, из-за ограниченного числа пациентов, в исследование вошли самые разные агонисты. Rascol et al. (16) показали, что, например, агонист дофамина ропиринол обладает такой же эффективностью, как леводопа, при монотерапии первых двух стадий заболевания по Hoehn и Yahr, - результат, совпадающий с нашим. В настоящее время неясно, однако, будет ли это распространяться и на другие агонисты дофамина, если сравнивать их с леводопой. Помимо этого, при лечении больных с минимально выраженными нарушениями можно склониться, скорее, к назначению монотерапии агонистами, чем леводопой, а при лечении пациентов с резко выраженными нарушениями, независимо от клинической стадии, поступать наоборот. Это может объяснять также, почему у пациентов, получавших монотерапию агонистами дофамина, баллы по шкале UPDRS на ранних стадиях заболевания были ниже. Однако наиболее подходящим объяснением будет то, что пациенты с 1 – 2.5 стадиями заболевания по Hoehn и Yarh, лечившиеся комбинацией леводопы с агонистами, имели несколько более выраженные нарушения, чем больные, получавшие монотерапию агонистами дофамина.
С учетом всего этого, какой вывод следует сделать из настоящего исследования? Общепризнано, что на очень ранних стадиях заболевания следует начинать лечение с агонистов дофамина, и наши результаты хорошо согласуются с таким подходом. Стадия 2.5 по Hoehn и Yahr, по-видимому, представляет переходную фазу, когда монотерапия агонистами дофамина становится недостаточной. Начиная с этой стадии, тактика лечения должна основываться на применении комбинации леводопы с агонистом дофамина, что позволяет достичь наилучшего результата. Полученные нами данные подтверждают, что для определения временной точки, когда пора менять тактику лечения, следует опираться на клиническую стадию заболевания, которая будет намного лучшим критерием, чем возраст больного.
Библиография
[1] Rinne UK. Problems associated with long-term levodopa treatment of Parkinson’s disease. Acta Neurol Scand 1983;68(Suppl. 95):19 -26.
[2] Rinne UK. Dopamine agonists as primary treatment in Parkinson’s disease. In: Yahr MD, Bergmann KJ, editors. Advances in neurology, vol. 45. New York: Raven Press, 1986:519-23.
[3] Rinne UK. Early dopamin agonist treatment in Parkinson’s disease. In: Lieberman A, Lataste X, editors. Parkinson’s disease the role of dopamine agonists. UK: The Partheon Publishing Group, 1989:29-33.
[4] Rinne UK. Combined bromocriptine-levodopa therapy early in Parkinson’s disease. Neurology 1985;35:1196-8.
[5] European Multicenter Trial Group, Olsson JE. Bromcriptine and levodopa in early combination in Parkinson’s disease: first results of the collaborative European Multicenter Trial. In: Lieberman A, Lataste X, editors. Parkinson’s disease the role of dopamine agonists. UK: The Partheon Publishing Group, 1989:77-82.
[6] Olanow CW. Dopamin agonists: a rewiew. In: Lieberman A, Lataste X, editors. Parkinson’s disease the role of dopamine agonists. UK: The Partheon Publishing Group, 1989:69-75.
[7] Olanow CW, Alberts M, Stajich J, Burch G. Prospective randomized blinded study of sinimet versus parlodel in untreated Parkinson’s patients. Neurology 1987;37(Suppl.):341-7.
[8] Koller WC, Silver DE, Lieberman A. An algorithm for the management of Parkinson’s disease. Neurology 1995;45(12):2301-2.
[9] Stocchi F. The influence of age on the use of dopamine agonists as primary symptomatic therapy. In: Olanow CW, Obeso JA, editors. Beyond the decade of the brain, vol. 2. Wells Medicals Limited, 1997:187-93.
[10] Playfer JR. Parkinson’s disease. Postgrad Med J 1997;73:257-64.
[11] Contin M, Riva R, Martinelli P, Albani F, Baruzzi A. Effect of age on the pharmacokinetics of oral levodopa in patients with Parkinson’s disease. Eur J Clin Pharmacol 1991;41:463-6.
[12] Steiger MJ, Quinn NP. Levodopa-based therapy. In: Koller WC, editor. Handbook of Parkinson’s disease, 2nd ed. New York: Marcel Dekker, 1992:391-410.
[13] Olanow CW, Watts RL, Koller WC. An algorithm (decision tree) for the management of Parkinson’s disease (2001): treatment guidelines. Neurology 2001;56(Suppl. 5):1-88.
[14] Braune HJ, Moller JC, Oertel WH. Erkrankungen der Basalganglien. In: Kunze K, editor. Praxis der Neurologie. Stuttgart: Georg Thieme Verlag, 1999:453-60.
[15] Moller JC, Wachter T, Oertel WH. Parkinson-Krankheit Moderne Therapie gezielt einsetzen. MMW-Fortschr Med 2001;Sonderheft 2:45-9.
[16] Rascol O, Brooks DJ, Brunt ER, Korczyn AD, Poewe WH, Stocchi F. Ropirinole in the treatment of early Parkinson’s disease: a 6-month interim report of a 5-year levodopa controlled study. Mov Disord 1998;13:39-45.
| Январь 2006 г. |