Опубликовано в журнале
"Врач", 3 -2011Тактика антиагрегантной терапии у курящих пациентов с ХОБЛ
Е. Привалова,
Н. Кузубова, доктор медицинских наук,
О. Титова, доктор медицинских наук
СПбГМУ им. акад. И.П. ПавловаОценивали агрегацию тромбоцитов у курильщиков с хронической обструктивной болезнью легких методом импедансной агрегатометрии образцов цельной крови.
Определяли изменение степени одышки и вентиляционных параметров при приеме препарата ацетилсалициловой кислоты.Ключевые слова: хроническая обструктивная болезнь легких, агрегатометрия, ацетилсалициловая кислота.
Antiaggregant Therapy Tactics In Smoking Patients With Chronic Obstructive Pulmonary Disease
E. Privalova; N. Kuzubova, MD; O. Titova, MD
Acad. I.P. Pavlov Saint Petersburg State Medical UniversityPlatelet aggregation was assessed in smokers with chronic obstructive pulmonary disease by impedance aggregatometry of whole blood samples.
A change in the degree of dyspnea and ventilation parameters was determined when an acetylsalicylic acid preparation was taken.Key words: chronic obstructive pulmonary disease, aggregatometry, acetylsalicylic acid.
Табакокурение - ведущий фактор формирования не только хронической обструктивной болезни легких (ХОБЛ), но и атеросклероза [11]. Процессы образования и разрыва атеросклеротической бляшки, сопровождающиеся внутрисосудистым тромбозом и лежащие в основе многих кардиоваскулярных заболеваний, являются причиной таких грозных осложнений, как инфаркт миокарда и инсульт. Тромбоциты с присущей им способностью к адгезии и агрегации в местах повреждения сосудистой стенки участвуют в процессах как поддержания нормального гемостаза, так и патологического тромбообразования [4]. Неконтролируемое прогрессирование последнего приводит к формированию тромба внутри сосуда с его окклюзией и развитием транзиторной ишемии или инфаркта органа [9].
Сочетание ХОБЛ и кардиоваскулярной патологии достаточно часто встречается в клинической практике. Так, артериальная гипертензия (АГ) наблюдается в 35% случаев ХОБЛ [1], а ишемическая болезнь сердца (ИБС) разной степени тяжести- у каждого 2-го больного [12]. Наличие ХОБЛ, в свою очередь, способствует более тяжелому течению сердечно-сосудистых заболеваний (ССЗ), повышая риск смертельного исхода у больных ИБС на 50%. При тяжелой и крайне тяжелой стадии ХОБЛ формируется легочное сердце, что провоцирует развитие желудочковых форм нарушения ритма [12]. Сочетание обострения ХОБЛ с АГ усиливает ишемию миокарда, повышая постнагрузку на правый желудочек. Снижение общей сократимости миокарда при ИБС в свою очередь ухудшает легочную гемодинамику при ХОБЛ [11]. Лекарственные препараты, используемые для лечения ХОБЛ, также способны негативно влиять на сердечно-сосудистую систему. Прием препаратов теофиллина и агонистов β-рецепторов может провоцировать у больных ХОБЛ эпизоды аритмии, среди которых преобладают суправентрикулярная тахикардия и желудочковые формы аритмии [12].
Профилактика ССЗ и снижение риска развития осложнений- одно из приоритетных направлений совре менной медицины. Тесная взаимосвязь процессов атерогенеза и тромбообразования патогенетически обосновывает долговременную антитромботическую терапию [8]. Назначение антиагрегантных препаратов признано обязательным звеном профилактики и терапии большинства ССЗ [6]. Ацетилсалициловая кислота (АСК) на сегодня рассматривается как главный компонент профилактической терапии у кардиологических больных [5].
Наиболее широкое применение АСК началось с 1980-х годов после подтверждения результатов исследований, свидетельствующих о снижении риска развития острого инфаркта миокарда и острой коронарной смерти примерно на 25% на фоне применения препарата [14]. В настоящее время ХОБЛ не является противопоказанием для применения АСК, однако отсутствуют исследования, посвященные влиянию препаратов этой группы на течение заболевания. Нет и четкого представления об определяющих тактику антиагрегантной терапии исходных изменениях активности тромбоцитов у больных ХОБЛ.
Антиагрегантную терапию назначают, как правило, на длительный срок, при этом требуется мониторинг агрегации тромбоцитов [6]. Активность тромбоцитов в кардиологической практике оценивают преимущественно с использованием оптико-механических коагулометров. До недавнего времени индуцированную агрегацию тромбоцитов чаще измеряли оптическим методом Борна, имеющим ряд особенностей и недостатков. Так, оптическая агрегатометрия проводится в образцах обогащенной тромбоцитами плазмы, которая является искусственной системой, исключающей влияние на активацию тромбоцитов других клеток крови. Существующие в настоящее время медицинские технологии позволяют детально исследовать процессы агрегации тромбоцитов и расширяют возможности мониторинга антиагрегантной терапии. В частности, все более широкое применение находит метод импедансной агрегатометрии, основанный на регистрации изменений электрического сопротивления в образцах цельной цитратной крови (разведение 1:1). Данный метод широко используется за рубежом и в России для скрининга активности тромбоцитов, а также для мониторинга терапии антиагрегантами в кардиологической и неврологической практике [15, 16]. Моделируя комплексный ответ тромбоцитов в присутствии всех клеточных и плазменных элементов крови в реальном времени, методика позволяет оценить активность тромбоцитов в условиях, приближенных к физиологическим, что особенно важно при обследовании больных с таким патогенетически сложным заболеванием, как ХОБЛ [2].
Таким образом, изучение агрегационной активности тромбоцитов и возможностей ее коррекции с оценкой влияния препаратов АСК на клинические и лабораторные показатели больных ХОБЛ представляется весьма актуальным.
Нами агрегационная активность тромбоцитов у больных ХОБЛ исследована методом импедансной агрегатометрии с последующей оценкой влияния препарата АСК на клиническое течение заболевания, вентиляционные показатели и агрегационную активность тромбоцитов. В исследование было включено 108 пациентов, составивших 3 группы (табл. 1).
Таблица 1
Распределение больных по полу, возрасту и индексу курения (М±m)
Группа Характеристика группы Средний возраст, годы Индекс курения, пачка/лет Мужчины/ женщины 1-я (n=64) Курильщики с ХОБЛ 61,2±1,01 37,3±2,01 62/2 2-я (n=24) Курильщики без нарушения бронхиальной проходимости 53,4±2,2 28,7±2,8 19/5 3-я (n=20) Некурящие без бронхолегочной патологии 54,0±3,0 0 17/3 Степень тяжести ХОБЛ оценивали в соответствии с классификацией GOLD 2008 г. [13] на основании результатов клинического и функционального обследований.
В группе курильщиков с ХОБЛ преобладали пациенты с тяжелой и очень тяжелой степенью одышки по шкале MRC.
В исследование не включали больных с кардиоваскулярной патологией, а также с любой клинически значимой хронической патологией или с профессиональной вредностью в анамнезе.
Дизайн исследования предполагал 3 этапа. На 1-м этапе проводилось сравнительное исследование функциональных характеристик тромбоцитов у больных ХОБЛ, курильщиков без нарушения бронхиальной проходимости и некурящих без бронхолегочной патологии. Второй этап предполагал исследование 34 пациентов с ХОБЛ, получавших базисную терапию в соответствии с рекомендациями GOLD 2008 в течение года. Пациенты с легкой степенью тяжести ХОБЛ получали фенотерол/ипратропия бромид в дозе 50/20 мкг по требованию до 4 раз в сутки, со среднетяжелой- тиотропия бромид в дозе 18 мкг/сут; фенотерол/ипратропия бромид в дозе 50/20 мкг по требованию 1-2 раза в сутки, с тяжелой и крайне тяжелой стадией заболевания- тиотропия бромид в дозе 18 мкг/сут; формотерол в дозе 24 мкг/сут, беклометазон дипропионат в дозе 1000 мкг/сут.
На 3-м этапе из группы повторно обследованных пациентов с ХОБЛ было отобрано 10 курильщиков (средний объем форсированного выдоха за 1-ю секунду (ОФВ1)- 38,4±5,7% от должного) с более высокими показателями агрегации тромбоцитов для продолжения базисной терапии в сочетании с приемом АСК в дозе 150 мг в течение месяца. Вентиляционные показатели определяли на спирографе Pneumoscreen-2 фирмы E. Jaeger (Германия), функциональную активность тромбоцитов- на импедансном агрегометре Chrono-log (Chrono-log Corporation, США). В качестве индукторов применяли аденозиндифосфат (АДФ) и коллаген производства Chrono-log Corporation в дозе 10 мкМ и 2 мкг соответственно. В ходе агрегатометрии оценивали ряд параметров (табл. 2).
Таблица 2
Параметры агрегации тромбоцитов при исследовании методом импедансной агрегатометрии (индукция АДФ и коллагеном)
Показатель агрегации Значение для оценки функции тромбоцитов Амплитуда Сопротивление при прохождении тока через образующиеся на электродах агрегаты тромбоцитов после добавления индуктора в кювету с кровью Наклон кривой агрегации Отражает интенсивность ответа тромбоцитов на активацию индуктором Время задержки агрегации (Lag-фаза) Время от формирования монослоя тромбоцитов на электроде до начала процесса агрегации после добавления индуктора Площадь под кривой агрегации Интегральная характеристика функционального состояния тромбоцитов за 6 мин наблюдения При статистической обработке результатов использовали критерий Манна-Уитни, коэффициент ранговой корреляции Спирмана и парный критерий Вилкоксона. Альтернативная статистическая гипотеза принималась при значении р<0,05.
В ходе исследования было отмечено, что у курильщиков 1-й и 2-й групп параметры агрегации были достоверно ниже, чем у некурящих, что отражает замедление ранних этапов формирования тромбоцитарного тромба и связано либо с нарушением реакции высвобождения, либо с меньшим содержанием гранул в тромбоците (табл. 3).
Таблица 3
Агрегационная активность тромбоцитов исследуемых групп (M±m)
Показатель Группа 1-я (n=64) 2-я (n=24) 3-я (n=20) Амплитуда с АДФ, Ом 14,3±0,5* 14,4±0,6* 18,5±0,6 Амплитуда с коллагеном, Ом 19,4±0,5* 19,8±0,7* 22,4±0,6 Наклон с АДФ 8,7±0,4* 8,4±0,5* 13,3±0,6 Наклон с коллагеном 9,2±0,5* 9,0±0,4* 13,7±0,7 Время задержки с АДФ, с 32,0±1,9* 31,0±2,0* 18,5±0,9 Время задержки с коллагеном, с 52,6±1,9 49,9±3,5 45,9±2,9 Площадь с АДФ 58,2±2,4* 57,6±2,8* 81,6±2,8 Площадь с коллагеном 67,9±2,3* 69,3±2,8* 84,2±3,0 Примечание. Достоверность различий с показателями лиц 3-й группы: * p<0,0001 (тест Манна-Уитни).Увеличение времени задержки агрегации отражает истощение систем вторичных посредников активации тромбоцитов (АДФ; тромбоксан А2). В исследованиях последних лет, посвященных использованию агрегатометрии у больных с кардиоваскулярной патологией, отсутствуют сведения об изменении этого показателя, его референтные значения в настоящее время не определены.
По мере нарастания клинической симптоматики и вентиляционных нарушений у пациентов с ХОБЛ отмечалось усиление агрегационной активности, что указывает на участие тромбоцитов в прогрессировании патологического процесса. На фоне достоверного снижения ОФВ1 (p<0,0001) и жизненной емкости легких (p<0,001) происходило повышение интенсивности агрегации при индукции с АДФ, коррелировавшее со степенью выраженности одышки (p<0,05). Снижению ОФВ1 сопутствовали уменьшение времени задержки агрегации тромбоцитов с АДФ (p<0,005), а также увеличение площади под кривой агрегации с АДФ (p<0,05). Увеличение площади агрегации и укорочение времени ее задержки при индукции АДФ сочетались со снижением минутного объема сердца (МОС) 25, МОС 50 и МОС 75 (p<0,05). По мере нарастания степени тяжести ХОБЛ происходило уменьшение времени задержки с АДФ (p<0,005) и увеличение площади под кривой при индукции АДФ (p<0,05). Выявленные изменения свидетельствуют о повышении интенсивности агрегации тромбоцитов на ранних этапах формирования тромбоцитарного тромба по мере утяжеления ХОБЛ.
Достоверных изменений вентиляционных, эритроцитарных и тромбоцитарных показателей при повторном исследовании курильщиков с ХОБЛ, получавших базисную терапию в течение года, не отмечено. Прием препарата АСК вызвал адекватное снижение всех средних показателей агрегационной активности тромбоцитов, достигшее достоверных значений при индукции с коллагеном (р<0,05). На фоне приема антиагреганта у больных нарастала одышка (p<0,01) и ухудшались вентиляционные показатели с достоверным снижением индекса Тиффно (р<0,05).
Антиагрегантное действие АСК обусловлено необратимым блоком циклооксигеназы I (ЦОГ I) с подавлением синтеза и высвобождения тромбоксана А2 (ТХА2) [7]. В результате тромбоциты на весь период своей жизни теряют способность к секреции гранул [10], в том числе и ɑ-гранул, содержащих тромбоцитарный фактор роста, без которого репарация эндотелия невозможна (рис. 1).
Рис. 1. Влияние АСК на репарацию эндотелия у больных ХОБЛУхудшение клинических и вентиляционных показателей у больных ХОБЛ является, вероятно, следствием резкого снижения репарации эндотелия сосудов легких под воздействием АСК. Ситуация усугубляется замедлением ранних этапов формирования тромбоцитарного тромба, что свидетельствует об исходном дефиците пула хранения тромбоцитов и особенно ɑ-гранул, играющих важную роль в развитии эндотелиальной дисфункции при этом заболевании. В настоящее время препараты АСК - наиболее распространенные антиагреганты, используемые при кардиоваскулярной патологии [10], но ими перечень антиагрегантов не ограничивается. В него входят: препараты АСК; тиенопиридины (тиклопидин, клопидогрел); бокаторы рецепторов IIb/IIIa тромбоцитов. Подавляет агрегацию тромбоцитов также дипиридамол, который значительно уступает по эффективности препаратам других групп [2]. Действие блокаторов гликопротеиновых рецепторов IIb/IIIa обратимо, они используются для кратковременного блокирования тромбоцитарной активности у больных, подвергающихся эндоваскулярным вмешательствам [2]. С препаратами АСК по эффективности сравнима группа тиенопиридинов, имеющая 2 подгруппы: препараты тиклопидина и клопидогрела. Являясь мощными ингибиторами агрегации, препараты этой группы не оказывают ульцерогенного и диспепсического действия [3]. Применение тиклопидина ограничено длительностью развития антиагрегантного эффекта за 24-48 ч. Клопидогрел в отличие от тиклопидина развивает свое действие за 2 ч, для достижения терапевтического эффекта требуются меньшие дозы [3, 20]. Механизм действия клопидогрела связан с селективным блоком АДФ рецепторов тромбоцитов; преимущественно он подавляет поздние этапы агрегации тромбоцитов и образование фибриновых мостиков (рис. 2).
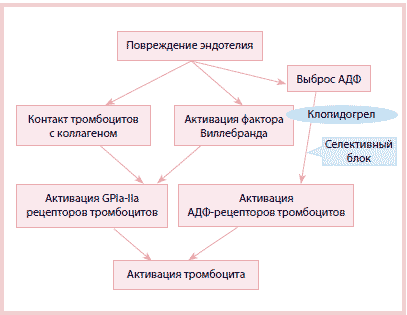 Рис. 2. Механизм действия клопидогрела
Рис. 2. Механизм действия клопидогрелаИмпедансная агрегатометрия в настоящее время считается информативным методом мониторинга терапии клопидогрелем [20].
Таким образом, современные антиагреганты различаются по направленности действия. Это позволяет подобрать препарат, снижающий эндогенную индукцию тромбоцитов, но не блокирующий высвобождение тромбоцитарного фактора роста на ранних этапах формирования тромбоцитарного тромба, что предотвращает резкое снижение репарации эндотелия и отрицательное влияние на течение ХОБЛ.
Вышеизложенное позволяет заключить, что: o нарастание одышки и ухудшение вентиляционных показателей у пациентов с ХОБЛ сопровождается повышением агрегационной активности томбоцитов;
назначение препаратов АСК больным с сочетанной кардиоваскулярной патологией требует дополнительного контроля клинических и вентиляционных показателей через месяц терапии; при ХОБЛ предпочтительнее назначать клопидогрел; в случае нарастания одышки и снижения показателей функции внешнего дыхания на фоне приема АСК рекомендована замена антиагреганта препаратом группы клопидогрела. Литература
1. Адашева Т.В., Задионченко В.С., Мациевич М.В. и др. Артериальная гипертония и ХОБЛ - рациональный выбор терапии // Русск. мед. журн. -2010; 14 (10): 795-801.
2. Вавилова Т.В. Антитромботическая терапия в клинической практике. Принципы проведения и лабораторный контроль: пособие для врачей. -СПб.: СПбГМА им И.И. Мечникова, 2008. - 82 с.
3. Добровольский А.В. Клопидогрел в лечении заболеваний сердечно-сосудистой системы // Русск. мед. журн. - 2009; 17 (8): 558-570.
4. Долгов В.В., Свирин П.В. Лабораторная диагностика нарушений гемостаза. - М.: Триада, 2005. - 223 с.
5. Карпов Ю.А. Ацетилсалициловая кислота - ключевая позиция в первичной и вторичной профилактике сердечно-сосудистых заболеваний и их осложнений // Русск. мед. журн. - 2008; 16 (11): 1554-1558.
6. Косарев В.В., Бабанов С.А. Антиагреганты: клинико-фармакологические подходы к применению при ишемической болезни сердца // Русск. мед. журн. - 2009; 17 (18): 1172-1177.
7. Колобов С.В., Верткин А.Л., Зайратьянц О.В. и др. Эффективная и безопасная антиагрегантная терапия в общемедицинской практике: метод. рекоменд. - М.: ММА им И.М. Сеченова, 2006. - 31 с.
8. Лупанов В.П. Роль ацетилсалициловой кислоты при вторичной профилактике атеросклероза и его сердечно-сосудистых осложнений // Русск. мед. журн. - 2009; 17 (14): 898-903.
9. Танашян М.М., Домашенко М.А. Антиагреганты во вторичной профилактике ишемического инсульта у пациентов с мультифокальным атеросклерозом // Русск. мед. журн. - 2010; 18 (26): 1549-1552.
10. Санодзе И.Д., Святов И.С., Шилов А.М. Антиагреганты - современное состояние вопроса // Русск. мед. журн. - 2003; 11 (9): 552-556.
11. Цветкова О.А. Лечение легочного сердца у больных ХОБЛ в сочетании с ИБС // Русск. мед. журн. - 2005; 13 (7): 425-428.
12. Чучалин А.Г. Хроническая обструктивная болезнь легких и сопутствующие заболевания. Ч. I. ХОБЛ и поражения сердечно-сосудистой системы // Русск. мед. журн. - 2008; 16 (2): 58-65.
13. Глобальная инициатива по хронической обструктивной болезни легких: пер. с англ. / под ред. А.Г. Чучалина. - М., 2008. - 99 с.
14. Malinin A., Atar D., Callahan K., Marcus E. ет. al. Effect of single dose aspirin on humans with multiple risk factors for coronary artery disease // European J. Pharmacology. - 2003; 462: 139-143.
15. Hochholzer W., Trenk D., Frundi D. Whole blood aggregometry for evaluation of the antiplatelet effects of clopidogrel // Thrombos. Research. J. -2007; 119: 285-291.
16. Svenstrup T., Kristensen S., Korsholm L. Variation and importance of aspirin resistance in patient with know cardiovascular disease // Thrombos. reseach. J. - 2006; 10: 22-29.
| Ноябрь 2011 г. |