3. Результаты современных международных научных исследований бенфотиамина
К наиболее важным и часто развивающимся сопутствующим заболеваниям при сахарном диабете относятся диабетическая ретинопатия и диабетическая нефропатия. В результате их развития качество жизни пациентов серьезно ухудшается, и их эффективное лечение связано с огромными финансовыми затратами. Стоит задуматься об одних только издержках на лазерную терапию и проведение диализа (Brownlee, 2004).
Международным исследовательским группам в настоящее время удалось экспериментально подтвердить терапевтическое значение бенфотиамина для лечения соответствующих заболеваний. В основе обоих заболеваний лежит общий патогенетический механизм, который был исследован международной рабочей группой Хаммеса (Hammes, 2003).
В процессе метаболизма глюкозы образуются радикалы кислорода. У больных сахарным диабетом их число увеличивается, что приводит к блокаде расщепления глюкозы. Происходит повышение концентрации промежуточных продуктов, таких как фруктозо-6-фосфат и глицеральдегид-3-фосфат. Последние превращаются далее в другие, но по неблагоприятному механизму распада. К ним относятся: гексозаминовый путь, диацилглицероловый путь, путь с участием протеинкиназы С, образование AGE-продуктов и соединений NF-кВ.
Последствиями являются возникновение:
микроангиопатий: ретинопатия и нефропатия; макроангиопатий: артериосклероз/инфаркт миокарда/кровоизлияние в мозг. 3.1. Бенфотиамин при диабетической ретинопатии
Бенфотиамин препятствует активации патогенетических механизмов изменения направления промежуточных продуктов распада глюкозы - фруктозо-6-фосфата и глицеральдеги-д3-фосфата - в пентозо-фосфатный цикл. Это осуществляется путем активации фермента транскетолазы, который зависит от присутствия витамина В1 и активность которого у больного сахарным диабетом снижена.
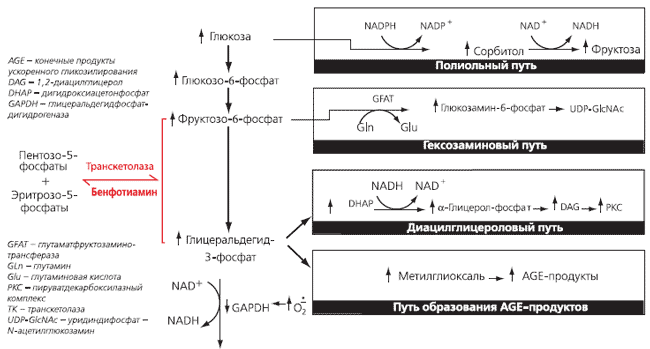
Активность транскетолазы под влиянием бенфотиамина увеличивается на 400% и, таким образом, устраняется "задержка утилизации" (Brownlee, 2001). В результате происходит нормализация метаболизма глюкозы (Рис. 20).
Рис. 20. С помощью транскетолазы бенфотиамин индуцирует обходной метаболический путь, который приводит к беспроблемному выделению вредных полупродуктов метаболизма (изменено в сравнении с Brownlee, 2004).
Hammes и соавт. продемонстрировали это на модели у крыс. В процессе исследования крысы одинаковой массы и возраста были разделены на 3 группы. Одна группа использовалась в качестве контрольной и оставалась здоровой. У животных двух других групп введением стрептозотоцина индуцировался сахарный диабет. Обе эти группы имели отличие только в том, что животные одной из них дополнительно получали бенфотиамин. Через 36 недель число патологических ацеллюлярных капиллярных сегментов в сетчатке у крыс с сахарным диабетом втрое превысило этот показатель у здоровых животных. Напротив, у крыс с сахарным диабетом (одинаковыми по степени тяжести), получавших терапию бенфотиамином, изменений числа ацеллюлярных капиллярных сегментов и, следовательно, повышен -ного риска развития ретинопатии выявлено не было (фото. 3 и рис. 21).
Фото 3. Микрофотографии состояния сосудов сетчатки у крыс без сахарного диабета (левый снимок), у крыс с сахарным диабетом, которые получали терапию бенфотиамином (правый снимок), и не получавших ее (средний снимок). Применение бенфотиамина полностью предотвращало экспериментально индуцированное капиллярное повреждение или развитие ретинопатии (изменено в сравнении с Hammes, 2003)

Рис. 21. Чисдо патологических ацеллюлярных капиллярных сегментов в сетчатке при терапии бенфотиамином могло сохраняться на таком же уровне, как у животных без сахарного диабета, а у животных с сахарным диабетом, не получавших бенфотиамин, оно увеличивалось втрое (изменено в сравнении с Hammes, 2003)

Бенфотиамин:
активизирует транскетолазу в клетках эндотелия; активизирует транскетолазу в сетчатке у пораженных сахарным диабетом; предотвращает гипергликемические расстройства in vitro; препятствует действию неблагоприятных механизмов в сетчатке при сахарном диабете. 3.2. Бенфотиамин при диабетической нефропатии
Нефропатия у больных сахарным диабетом 1 и 2 типа приводит не только к почечной недостаточности с такими последствиями, как диализ или пересадка почки, но и к повышению риска сердечно-сосудистых заболеваний и летального исхода. Первыми признаками этого являются длительная микроальбуминурия и гиперфильтрация. Адекватный контроль и нормализация глюкозы в крови может снижать этот риск, однако полностью устранить его не удается. Вследствие повышения концентрации глюкозы в клетках почечного эндотелия и перицитах происходит активация вышеописанных неблагоприятных механизмов (Beltramo, 2002 и 2004). Для проверки того, способно ли переключение обмена веществ на пентозо-фосфатный путь привести к улучшению функции почек, рабочая группа Торнелли (Thornalley) провела исследование влияния тиамина и бенфотиамина на возникновение диабетической нефропатии (Babaei-Jadidi, 2004). Так же, как и при исследовании Хаммеса (Hammes) в качестве экспериментальной модели были выбраны крысы с сахарным диабетом, индуцированным введением стрептозотоцина. При этом формировалось несколько подгрупп:
здоровые контрольные животные, получавшие высокие дозы тиамина или бенфотиамина; контрольные животные с сахарным диабетом; контрольные животные с сахарным диабетом, получавшие низкие дозы тиамина (7 мг/кг в сутки или 70 мг/кг в сутки) или бенфотиамина (7 мг/кг в сутки или 70 мг/кг в сутки). Были получены следующие результаты:
применение тиамина и бенфотиамина не оказывало влияния на уровень глюкозы в крови; развитие микроальбуминурии уменьшалось на 70-80% независимо от дозы; относительно протеинурии были достигнуты подобные результаты. Также была обнаружена зависимость действия от дозы; только бенфотиамин был способен предотвратить гиперфильтрацию, которая является ранним признаком нефропатии; изначально гломерулярная активность транскетолазы у животных с сахарным диабетом была снижена и могла нормализоваться в результате заместительной терапии; экспрессия транскетолазы у животных с сахарным диабетом также была снижена и далее могла нормализоваться до прежней степени; гломерулярная PKC-активность была повышена в диабетической группе на 38% по сравнению с контрольной группой. Она могла возвращаться к исходному уровню под влиянием лечения в дозозависимом режиме; у крыс с сахарным диабетом также был повышен уровень AGE-продуктов, и степень его нормализации зависела от дозы препарата; в качестве индикатора выраженности окислительного стресса определялась концентрация тиолов в белках плазмы. У животных с сахарным диабетом она была понижена на 30% по сравнению c нормальными показателями. И только бенфотиамин был способен возвращать ее к норме. Таким образом, было показано, что бенфотиамин представляет собой эффективное средство, способное предотвращать развитие диабетической нефропатии на самых ранних стадиях и, возможно, препятствовать прогрессированию заболевания.
3.3. Бенфотиамин как средство защиты сосудов и органов от вредных AGE-продуктов
Вышеописанные патогенетические механизмы касаются не только сетчатки и почек, но также нервных волокон и функции сосудистого эндотелия. Группа шотландских специалистов под руководством Кэмерона в экспериментах на животных в течение 24 недель исследовала у крыс с сахарным диабетом влияние бенфотиамина на нервные волокна и функцию сосудистого эндотелия (Cameron, 2004).
Установлено, что бенфотиамин был способен сделать обратимым нейрональный и сосудистый дефицит с помощью процессов, проходящих при участии NO, которые могли бы иметь терапевтическое значение при диабетической ангиопатии и диабетической невропатии. Большой интерес в этой связи вызывают результаты проведенного недавно исследования Нью-Йоркской рабочей группы под руководством Vlassara, которая в кооперации с сотрудниками Немецкого научно-исследовательского института диабета в Дюссельдорфе и Диабетического центра в Бад-Ойнхаузене установила следующее. С помощью лазерной допплеровской флуометрии подтверждено, что через час после приема пищи, содержащей вредные конечные продукты ускоренного гликозилирования (AGEs), микрососудистая функция у больных сахарным диабетом 2 типа ухудшается. При заблаговременном приеме бенфотиамина можно было бы полностью избежать индуцированной AGE-продуктами сосудистой дисфункции, выражавшейся в сужении просвета и ухудшении кровоснабжения, что могло бы иметь большое значение в плане профилактики и терапии последствий и осложнений сахарного диабета (Stirban, 2005).
| Март 2009 г. |