Опубликовано в журнале:
«Терапия психических расстройств» 2007, № 2, С. 48-52Опыт применения венлафаксина (Велафакса) у пациентов с депрессией в амбулаторной и клинической практике
Б.А. Волель, Д.В. Романов
Научный центр психического здоровья РАМН, МоскваРЕЗЮМЕ
В статье приводятся данные исследования по оценке терапевтической эффективности и безопасности препарата венлафаксина (Велафакса) у пациентов с депрессивными состояниями различной степени тяжести и психопатологической структуры (всего 30 больных). Обосновывается вывод, что венлафаксин является эффективным антидепрессантом для терапии депрессивных расстройств лёгкой и средней степени тяжести, в т.ч. с выраженным тревожным компонентом. Менее эффективен препарат при тяжёлых тоскливых депрессиях. Обосновывается целесообразность применения венлафаксина как при госпитальной, так и при продолжительной терапии депрессивных расстройств.
ВВЕДЕНИЕ
Родоначальником одной из современных групп тимоаналептических средств, характеризующихся двойным механизмом действия (СИОЗСиН -селективные ингибиторы обратного захвата серотонина и норадреналина) и влияющих как на серотонинергическую, так и на норадреналинергическую нейротрансмиттерные системы, является Велафакс (венлафаксина гидрохлорид - [2-диметиламино-1-(4-метоксифенил)-этил]циклогексан-1-ол), относимый к антидепрессантам III поколения [1]. Поиски таких антидепрессантов и последующее появление группы препаратов1, фактически промежуточных между классами селективных ингибиторов обратного захвата монаминов (норадреналина/серотонина) и традиционных антидепрессантов - ТЦА, блокирующих широкий спектр рецепторов, обусловлены рядом следующих факторов.
Несмотря на высокую эффективность, применение традиционных тимоаналептиков (ТЦА) ассоциировано с высокой частотой нежелательных лекарственных реакций, связанных с воздействием не только на норадреналин/серотонинергические, но и на холинергические, гистаминовые и адренергические рецепторы [2], что ограничивает возможности их назначения в амбулаторной практике и длительного применения в качестве средств поддерживающей терапии [3]. В свою очередь препараты последних генераций, в особенности СИОЗС (наиболее часто назначаемые в мире антидепрессанты [4]), лишённые многих недостатков ТЦА, хотя и отличаются лучшей переносимостью [10], но проигрывают им, по данным некоторых авторов, в эффективности [5, 8].
Венлафаксин, формально относимый к препаратам двойного действия, влияет на метаболизм не только серотонина и норадреналина, но и дофамина, причём соответствующие эффекты последовательно проявляются при наращивании дозировок в его широком терапевтическом диапазоне [1]. Таким образом, венлафаксин, селективно влияя на метаболизм основных нейротрансмиттеров, участвующих в патогенезе депрессии, не только перекрывает спектр обусловленных их дисметаболизмом ведущих клинических проявлений аффективного расстройства, но и сочетает в себе зависящие от дозы свойства комбинированного тимоаналептика. Это позволяет использовать венлафаксин при лечении различных клинических вариантов депрессии, чем и определяется синдромальное разнообразие аффективных нарушений, активность препарата в отношении которых исследовалась в настоящей работе.
Целью настоящего исследования является оценка терапевтической эффективности и безопасности венлафаксина (Велафакса) у пациентов с депрессивными состояниями различной степени тяжести и психопатологической структуры.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Исследование проводилось на базе клиники отдела по изучению пограничной психической патологии и психосоматических расстройств (руководитель - академик РАМН, профессор А.Б. Смулевич) Научного центра психического здоровья РАМН (директор - академик РАМН, профессор А.С. Тиганов). Процедура клинического обследования состояла из стандартных процедур анализа психического состояния, сбора субъективных и объективных анамнестических сведений и оформления медицинской документации.
Для оценки состояния больных и действия препарата использовались следующие формализованные психометрические инструменты:
- Шкала общего клинического впечатления (CGI) для оценки тяжести заболевания (CGI-S) и улучшения (CGI-I);
- Шкала Гамильтона для оценки депрессии (HAMD21);
- Шкала Гамильтона для оценки тревоги (HAMA);
- Шкала депрессии Монтгомери-Асберг (MADRS).
В целях оценки безопасности регистрировались жалобы пациентов на неблагоприятные изменения в самочувствии.
В исследование включались пациенты старше 18 лет, состояние которых определялось клинически выраженным депрессивным синдромом (CGI-S > 4, HAMD21 > 20, HAMA > 20) в рамках депрессивного эпизода (F32), рекуррентного депрессивного расстройства (F33) и смешанного депрессивно-тревожного расстройства (F41.2)2 по критериям МКБ-10. Критериями исключения являлись период беременности и лактации, коморбидные депрессивному эпизоду острые психотические состояния, хронический алкоголизм, наркомания, общее тяжёлое соматическое состояние в фазе декомпенсации (почечная, печёночная, сердечная недостаточность, неконтролируемая гипергликемия), а также указания на гиперчувствительность к исследуемому препарату и приём МАО-И в течение двух недель, предшествующих включению в исследование.
В рамках исследования венлафаксин назначался курсами длительностью 84 дня (12 недель -3 месяца). Рекомендовался приём препарата вместе с пищей.
Начальная доза венлафаксина составляла 75 мг/сут (двукратный приём по 37,5 мг). В дальнейшем доза повышалась до 150 мг (двукратный приём по 75 мг). При необходимости назначения более высокой стартовой дозы (тяжёлая депрессия или госпитализация пациента) титрация начиналась с дозы 150 мг/сут, также разделённой на два приёма (по 75 мг). При неудовлетворительном терапевтическом эффекте суточная доза венлафаксина повышалась на 75 мг каждые два-три дня до достижения эффективной. Максимальная суточная доза составляла 375 мг. В качестве сопутствующей терапии нарушений сна применялись гипнотики (золпидем, зопиклон).
Оценка эффективности лечения по сравнению с исходным состоянием (визит 0) проводилась на 3-й (визит 1), 6-й (визит 2) и 12-й (визит 3) неделях терапии. Её критерием наряду с клинически регистрируемым улучшением состояния были уменьшение суммы балов по шкалам HAMD > 50 %, MADRS > 50 % и HAMA > 35 %3, в качестве дополнительных использовались показатели по шкале CGI-I «существенное», «выраженное» или «умеренное улучшение», а также по CGI-S («нет симптомов» или «пограничное расстройство»).
Для статистической обработки данных использовалась программа Statistica 6.0 (компаниf StatSoft, США).
Выборка исследования включала 30 больных, 11 мужчин и 19 женщин, в возрасте от 27 до 50 лет (средний возраст - 35,3 ± 5,3 года), госпитализированных в клинику ГУ НЦПЗ РАМН (9 наблюдаемых) или обратившихся за помощью амбулаторно (21 наблюдаемый). Социодемографические характеристики пациентов изученной выборки представлены в табл. 1.
Таблица 1. Социодемографические характеристики пациентов исследованной выборки, n = 30
Показатель Число пациентов абсолютное, n относительное,
%Пол Мужчины 11 36,7 Женщины 19 63,3 Профессиональный статус Работают/ учатся 17 56,7 Безработные/инвалиды 13 43,3 Семейный статус В браке 21 70 Одинокие/ разведены 9 30 В соответствии с критериями МКБ-10 клиническая картина психических нарушений у 25 больных определялась наличием признаков депрессивного состояния (F32, F33) или смешанного депрессивного и тревожного расстройства (F41.2) - у 5 пациентов.
На момент включения в исследование в статусе всех пациентов присутствовали стойкие депрессивные и тревожные расстройства разной степени выраженности, средний стартовый балл по шкале Гамильтона для оценки депрессии составил 22,2 ± 6, по шкале депрессии Монтгомери-Асберг - 28,9 ± 6, по шкале Гамильтона для оценки тревоги - 26,5 ± 5,6 баллов.
Распределение пациентов в соответствии с диагностическими категориями и выраженностью депрессивных расстройств представлено на рис. 1.
Рис. 1. Распределение по диагностическим рубрикам МКБ-10, n = 30
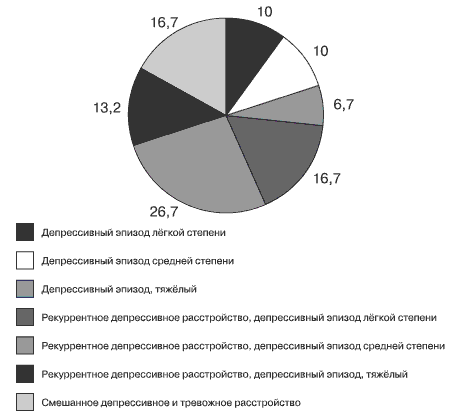
В 26,7 % случаев у пациентов был диагностирован первый эпизод депрессии (F32) или впервые возникшее смешанное депрессивное и тревожное расстройство (F41.2 - 16,7 %), тогда как более чем в половине наблюдений депрессивная симптоматика регистрировалась в рамках рекуррентной депрессии (F33 - 56,6 %).
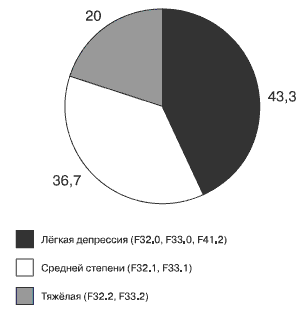
Как видно из диаграммы (рис. 2), в выборке преобладали больные с депрессией лёгкой и средней степени тяжести (80 %), и лишь в 20 % случаев выраженность депрессивного синдрома соответствовала тяжёлой депрессии.
Рис 2. Распределение больных в зависимости от тяжести депрессивного синдрома
Переходя к психопатологической характеристике депрессивных расстройств, наблюдавшихся в исследуемой выборке, отметим, что в неё вошли пациенты с тревожными (гипотимия с преобладанием беспредметного беспокойства, внутреннего напряжения, предчувствия несчастья), апатическими (сниженное настроение сопровождается дефицитом побуждений с утратой жизненного тонуса, вялостью, безразличием ко всему окружающему), тревожно-апатическими (смешанный вариант) и тоскливыми депрессиями (подавленность с явлениями витальной тоски в виде диффузного, протопатического ощущения гнета, тяжести в груди). Наиболее частыми синдромальными вариантами были депрессии с преобладанием тревоги - у 12 наблюдаемых (40 %) и смешанные (тревожно-аптические) - у 8 наблюдаемых (26,6 %) (см. табл. 2).
Таблица 2. Распределение больных в зависимости от синдромального варианта депрессии
Вариант депрессии Число пациентов абсолютное, n относительное, % Тревожная 12 40 Апатическая 6 20 Тревожно-апатическая 8 26,6 Тоскливая 4 13,4 РЕЗУЛЬТАТЫ
Из 30 больных, включённых в исследование, полностью завершили курс терапии 25 (83,3 %) пациентов, что является высоким показателем тимоаналептической активности и толерантности к препарату. Средняя эффективная доза венлафаксина составила 200 мг/сут (от 75 до 375 мг). Доля пациентов, получавших максимальные терапевтические дозировки препарата (300-375 мг/сут), была равна 36 % (9 из 25 пациентов, закончивших исследование), что также характеризует переносимость препарата.
Причинами исключения из исследования были неэффективность терапии по оценке состояния на третьей неделе терапии (двое наблюдаемых - в обоих случаях тяжёлая тоскливая витальная депрессия -F32.2 по МКБ-10) и выраженные побочные эффекты, не поддающиеся коррекции симптоматическими средствами или снижением дозы препарата (трое наблюдаемых - тошнота, выраженная дневная сонливость при амбулаторном применении препарата).
Эффективность терапии венлафаксином (процент респондёров по шкалам HAMD > 50 %, MADRS > 50 % и HAMA > 35 %) при промежуточной оценке на 6-й неделе лечения была отмечена в 80 % случаев (20 наблюдаемых). При завершении курса лечения (3 месяца) в связи с его значительной продолжительностью проводилась шкальная оценка достижения уровня ремиссии (HAMD < 7 баллов, MADRS < 15 баллов) в зависимости от синдромального варианта депрессии (табл. 3): этот показатель составил в среднем 64 % (16 наблюдаемых), что сопоставимо с результатами большинства исследований эффективности венлафаксина [10].
Таблица 3. Процент достижения ремиссий на 12-й неделе терапии в зависимости от синдромального варианта депрессии, n = 16
Вариант депрессии Число пациентов абсолютное, n относительное, % Тревожная 10 83,3 Апатическая 3 60 Тревожно-апатическая 2 33,3 Тоскливая 1 50 На 1-й неделе терапии средний балл среди пациентов, достигших ремиссии, по шкале Гамильтона для оценки депрессии составил 5,3 ± 5,2, по шкале депрессии Монтгомери–Асберг - 4,3 ± 4,3, по шкале Гамильтона для оценки тревоги - 4,5 ± 1,9. Динамика показателей представлена на рис. 3.
Рис. 3. Редукция депрессивных и тревожных расстройств по шкалам депрессии Гамильтона (HDRS-21), шкале Монтгомери-Асберг (MADRS) и шкале тревоги Гамильтона (HAMA)
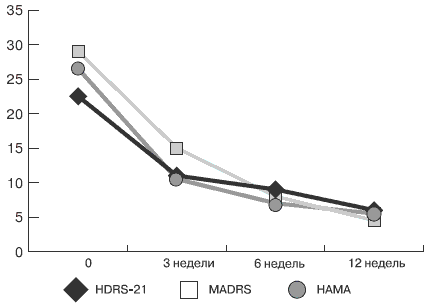
Высокая общая эффективность терапии отражается в результатах оценки по шкалам общего клинического впечатления - CGI-тяжесть и CGI-улучшение. Стартовый средний суммарный балл CGI-тяжесть, составивший 4,7 (интервал между 4 - «умеренно болен» и 5 - «явно болен»), снизился через 12 недель терапии до 1,4 (интервал между 1 - «здоров, отсутствие психических нарушений» и 2 - «пограничное состояние»). Средний суммарный балл шкалы CGI-улучшение на финальном визите (12-я неделя) составил 1,5 (интервал между 1 - «очень хорошее улучшение» и 2 - «хорошее улучшение»).
Клинический эффект венлафаксина характеризовался отчётливым антидепрессивным действием с редукцией как уровня аффективных, так и анксиозных расстройств. Проявления антидепрессивного действия выражались в субъективном улучшении настроения, снижении амплитуды колебаний аффективных расстройств, редукции признаков эмоциональной лабильности и проявлений синдрома раздражительной слабости, улучшении сна, повышении уровня продуктивности в повседневных делах. Наблюдалось проявление анксиолитического действия венлафаксина: редукция признаков тревоги, беспокойства, появление чувства «контроля над ситуацией», что в первую очередь относилось к проявлениям психической тревоги. При этом характерно было быстрое наступление тимоаналептического эффекта: в 80 % случаев отмечалась 50 % редукция суммы баллов по шкалам HDRS-21 и MADRS уже на третьей неделе терапии. Имела место гармоничная редукция гипотимии и тревожных нарушений в структуре депрессивных расстройств (см. рис. 4). Следует отметить, что, несмотря на длительное (12 недель) применение венлафаксина в нашем исследовании, случаев инверсии аффекта с переходом в гипоманиакальное состояние не зафиксировано.
Рис. 4. Редукция депрессивных и тревожных расстройств по шкалам у пациентов в структуре депрессии без выраженных тревожных расстройств, n = 13
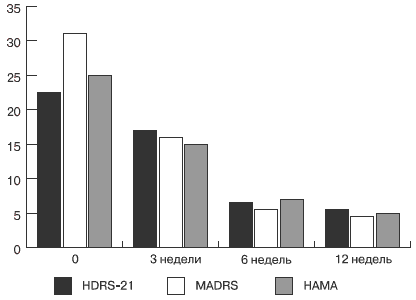
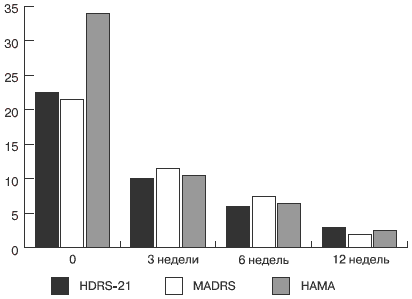
В то же время при терапии состояний, сопровождающихся наряду с депрессивной симптоматикой выраженными проявлениями тревоги (12 наблюдаемых с исходным средним баллом по шкале тревоги НАМА - 34), была выявлена наряду с тимоаналептическим эффектом выраженная анксиолитическая активность препарата (рис. 5), зарегистрированная при применении в высоких дозах (200 мг/сут и выше) уже на третей неделе терапии.
Рис. 5. Анксиолитический эффект венлафаксина у пациентов с тревогой в рамках депрессии, ассоциированной с тревожными проявлениями, n = 12
Венлафаксин хорошо переносился пациентами. В связи с побочными эффектами из исследования выбыли трое больных (двое - выраженная тошнота, один - дневная сонливость). Среди завершивших исследование неблагоприятные лекарственные эффекты зафиксированы в 7 случаях (28 %) и распределяются следующим образом (см. табл. 4).
Таблица 4. Зарегистрированные побочные эффекты
Побочные эффекты Число пациентов абсолютное, n относительное, % Тошнота 4 57 Сухость во рту 2 28,6 Дневная сонливость 1 14,4 Упомянутые нежелательные реакции возникали на начальном этапе терапии (первая неделя), были кратковременными, корригировались симптоматическими средствами или снижением дозы венлафаксинакса.
Применение венлафаксинакса не было связано с какими-либо проблемами в аспекте безопасности лечения. Токсических эффектов или аллергических реакций, связанных с приёмом венлафаксинакса, не зафиксировано, каких-либо признаков взаимодействия с препаратами сопутствующей терапии не отмечалось.
Таким образом, венлафаксин (Велафакс) является эффективным антидепрессантом для терапии депрессивных расстройств лёгкой и средней степени тяжести, в т. ч. с выраженным тревожным компонентом, что согласуется с результатами, полученными другими авторами [6, 7, 8, 9]. Менее эффективен препарат при тяжёлых тоскливых депрессиях.
Наряду с доказанной клинической эффективностью венлафаксину свойственен благоприятный профиль переносимости и высокий уровень безопасности, что, учитывая высокую распространённость аффективной патологии, в т. ч. сочетанной с проявлениями тревоги, обуславливает целесообразность применения венлафаксина как при госпитальной, так и при продолжительной амбулаторной терапии указанных расстройств.
1Исследования в этой области привели к разработке вслед за венлафаксином аналогичных по механизму действия тимоаналептиков - милнаципрана и дулоксетина.
2Удовлетворяя критериям смешанного тревожно-депрессивного расстройства (персистирующее или периодически возникающее расстройство настроения длительностью не менее одного месяца и выявлением 4 или более из следующих 10 симптомов, таких как беспокойство; плаксивость; склонность к чрезмерным опасениям; ожидание худшего; нарушения сна; чувство слабости или утраты энергии; затруднения концентрации внимания; раздражительность; безнадёжность; низкая самооценка или чувство собственной малоценности; а также значительный клинический дистресс и/или нарушения в социальной, профессиональной или в других важных областях активности), в исследованной выборке состояние клинически соответствовало тревожной депрессии умеренной степени.
3Критерий эффективности по шкале HAMA был установлен равным 35 %, поскольку показатель по этой шкале в предыдущих более длительных исследованиях достигал редукции от 50 % и более к 6-му месяцу терапии.
ЛИТЕРАТУРА
1. Аведисова А.С. Венлафаксин (Велаксин): результаты международных исследований антидепрессанта III поколения // Психиатрия и психофармакотерапия. 2006. Т. 11. № 2.
2. Мосолов С.Н. Клиническое применение антидепрессантов. СПб., 1995.
3. Anderson I., Mortimore C. Discontinuation rates of SSRI's and tricyclic antidepressants // Br J Psychiatry. 1997 Jul;171:87.
4. Bauer M., Whybrow P.C, Angst J., Verciani M., Moller H. World Federation of Societies of Biological Psychiatry (WFSBP) guidelines for biological treatment of unipolar depressive disorders, part 1: acute and continuation treatment of major depressive disorder // The World Journal of Biological Psychiatry 3: 5-43, 2002.
5. Vestergaard P., Gram L.F., Kragh-Sorensen P., Bech P., Reisby N., BolwigT.G. Therapeutic potentials of recently introduced antidepressants. Danish University Antidepressant Group // Psychopharmacol Ser. 1993;10:190-8.
6. Gorman J., Laszlo A. Efficacy of Fenlafaxine in mixed Depression-Anxiety States // Depression and Anxiety, 2000; 12 (1): 77-80.
7. Judge R., Wagner B. Once-daily venlafaxine XR compared with fluoxetine in outpatientwith depression and anxiety // J Clin Psychiatry 1999; 60: 795-6.
8. Roose S.P, Glassman A.H., Attia E., Woodring S. Comparative efficacy of selective serotonin reuptake inhibitors and tricyclics in the treatment of melancholia // Am J Psychiatry. 1994 Dec;151(12):1735-9
9. Rudolph R.L., Entsuah R., Chitra R. A meta-analysis of the effects of venlafaxine on anxiety associated with depression // J Clin Psychopharmacol Apr;18(2):136-44. 1998.
10. Williams J.W., Mulrow C.D., Chiquette E., Noel P.H., Aguilar C, Cornell J. A systematic review of newer pharmacotherapies for depression in adults: evi dence report summary // Ann Intern Med 2000;132:743-756.
| Май 2008 г. |