|
Опубликовано в журнале:
«Современные проблемы дерматовенерологии, иммунологии и врачебной косметологии», 3, 2010Сравнительный анализ эффективности и безопасности фторированных и хлорированных топических глюкокортикостероидов
Свирщевская Е. В.1, Матушевская Е. В.2
1 Институт повышения квалификации ФМБА, Москва
2 Институт биоорганической химии РАН
Свирщевская Елена Викторовна 117997, Москва, ул. Миклухо-Маклая, 16/10Топические глюкокортикостероиды и механизм их действия
Топические глюкокортикостероиды (ГКС) являются основными и практически безальтернативными препаратами при наружном лечении многих дерматозов. В последнее время дерматологи определили целый ряд заболеваний кожи, основой лечения которых являются ГКС. Эта группа получила название стероидочувствительные дерматозы [1]. В нее входят заболевания, которые отличаются по патогенезу и клиническим проявлениям, но их объединяет необходимость супрессивного воздействия на клетки иммунной системы, ассоциированные с кожей. Это атопический дерматит (АД), аллергические дерматиты, экзема, себорейное воспаление кожи, псориаз и многие другие. В соответствии с Европейской классификацией активности местных ГКС выделено 4 класса топических препаратов, разделенных по степени вазоконстрикторного эффекта (табл. 1).
При применении топических кортикостероидов отмечается локальное повышение концентрации ГКС в зоне воспалительного процесса, за счет чего ГКС-препараты не оказывают супрессорного действия как на центральную иммунную систему, так и на другие системы организма, что позволяет избежать тяжелых побочных эффектов. Топические кортикостероиды обладают выраженным противовоспалительным, противоаллергическим, антиэкссудативным и противозудным действиями. Они тормозят накопление лейкоцитов, высвобождение лизосомальных ферментов и провоспалительных медиаторов в очаге воспаления, угнетают фагоцитоз, уменьшают сосудисто-тканевую проницаемость, препятствуют образованию воспалительного отека. Таким образом, становится понятным, что применение топических ГКС является целесообразным за счет их локального действия на активированные клетки в коже. Современные синтетические ГКС имеют большее сродство с глюкокортикостероидным рецептором (ГКР), в связи с чем действие развивается значительно быстрее и сохраняется дольше.
Топические аналоги глюкокортикостероидов
В настоящее время синтезирован целый ряд высокоэффективных ГКС-препаратов, применяемых в виде мазей, кремов, лосьонов, аэрозолей и, реже, - в виде растворов и суспензий. Структура основных производных приведена на рисунке. Самыми эффективными на настоящий момент считаются фторированные и хлорированные производные кортизола (табл. 2). Среди фторированных препаратов наибольшей активностью обладают бетаметазона дипропионат (БДП), содержащий один атом фтора, и флютиказона пропионат (ФП), содержащий три атома фтора. Среди хлорированных производных наиболее эффективным считаются мометазона фуроат (МФ), содержащий 2 атома хлора, и беклометазона дипропионат (БКДП), содержащий один атом хлора [2 - 4].
Сравнение фторированных и хлорированных производных кортизола проведено по многим показателям. Наиболее важные параметры действия, такие как связывание стероидов с ГКР, подавление транскрипции белков, снижение в результате этого синтеза различных цитокинов и вазоактивных факторов и др., приведены в табл. 3 для наиболее изученного хлорированного производного МФ и фторированного препарата ФП по сравнению с дексаметазоном (ДМ). В тестах in vitro активность МФ и ФП практически не различается и значительно превосходит ДМ [5].
Рис. 1. Структура кортизола и синтетических ГКС производных. Кольцо D является основой всех производных ГКС (по материалам статьи S. P. Umland)
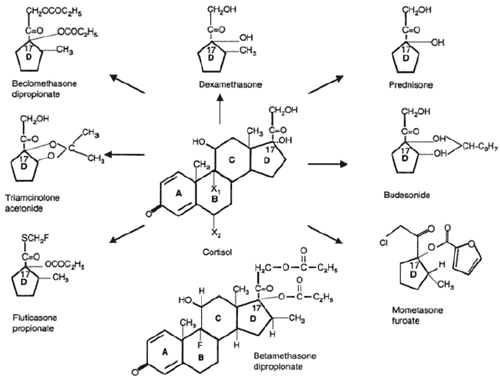
Фторированные кортикостероиды являются высокоэффективными ингибиторами активации клеток не только in vitro, но и при использовании in vivo. Однако при длительном применении они могут вызывать у больных атрофию кожи и повышение уровня кортизона в крови, утяжелять течение остеопороза [1; 6]. Имеющиеся на настоящий момент данные свидетельствуют о большей безопасности применения хлорированных производных при длительном терапии, например, сезонных ринитов и атопического дерматита. Так, использование МФ у 68 больных АД в течение 6 месяцев привело к поддержанию ремиссии у 61 больного; при этом незначительные осложнения наблюдали только у одного больного [7]. Эффективность и безопасность МФ (крем Унидерм) были подтверждены также в отечественных исследованиях детей и взрослых с атопическим дерматитом и псориазом [8; 9].
Таблица 1. Классификация топических ГКС
Группа Международное непатентованное название Очень сильные Клобетазола пропионат 0,5%
Хальцинонид 0,1%Сильные Бетаметазона валерат 0,1%
Бетаметазона дипропионат 0,05%
Будезонид 0,0375%
Мометазона фуроат 0,1%
Гидрокортизона 17-бутират 0,1%
Дексаметазон 0,025%
Триамцинолона ацетонид 0,1%
Метилпреднизолона ацепонат 0,1%
Флуметазона пивалат 0,02%
Флуоцинолона ацетонид 0,025%
Флутиказона пропионат 0,05%Средней силы Преднизолон 0,25%
Предникарбат 0,25%
Флуокортолон 0,025%
Алклометазона дипропионат 0,05%Слабые Гидрокортизона ацетат 0,1%, 0,5% Таблица 2. Классификация хлорированных и фторированных ГКС
Исходные производные Кортизол, преднизолон, будезонид Один атом хлора Беклометазона дипропионат, алклометазона дипропионат Два атома хлора Мометазона фуроат Один атом фтора Дексаметазон, бетаметазона дипропионат, триамцинолона ацетонид Два атома фтора Флуметазона пивалат Три атома фтора Флутиказона пропионат, флуоцинолона ацетонид Атом хлора и фтора Клобетазола пропионат Таблица 3. Сравнительная активность фторированных и хлорированных производных ГКС в различных тестах, % от активности мометазона фуората (по данным Umland, 2002)
Примечания:
Действие МФ ФП ДМ Связывание с ГКС рецептором 100 65-79 5-10 Подавление активации транскрипции 100 25 5 Подавление синтеза ИЛ-4 и ИЛ-5 100 90-100 20 Подавление конститутивной экспресии молекул адгезии 100 90-100 15 Подавление экспресии молекул адгезии VCAM-1 и ICAM-1, индуцированной ФНО-α 0 0 0 Подавление экспресии молекул адгезии VCAM-1 и ICAM-1, индуцированной риновирусом 100 100 18 Подавление функции эозинофилов 100 90-100 20 Подавление продукции лейкотриенов 100 90-100 15 Подавление миграции лейкоцитов в ткань 100 100
МФ - мометазон фуроат
ФП - флутиказона пропионат
ДМ - дексаметазон
ИЛ - интерлейкин
ФНО-α - фактор некроза опухоли альфаСравнительное исследование БДП и МФ показало, что использование больными АД мометазона фуроата раз в день давало более быстрое разрешение симптомов заболевания при меньших побочных эффектах, чем использование БДП два раза в день [10]. Однако при краткосрочном применении (от 2 до 4 недель) фторированных препаратов побочных явлений практически не наблюдали [11 - 14].
Анализ стоимости препаратов в Англии показал, что МФ примерно в 2,5 - 3 раза дороже, чем БДП [7]. При этом применение МФ раз в день позволяет снизить стоимость лечения. При необходимости длительного использования топических стероидов, особенно на больших поверхностях кожных покровов, при нанесении их на лицо, шею, складки имеет смысл применять МФ, а при необходимости короткого курса вполне адекватным является использование более дешевых и равно эффективных фторированных препаратов (табл. 4).
Таблица 4. Сравнительная характеристика эффективности действия и особенностей применения фторированных и хлорированных топических ГКС III класса
Бетаметазона дипропионат Мометазона фуроат Содержит 1 атом фтора Содержит 2 атома хлора Быстрота наступления лечебного эффекта (в первые 4 - 5 дней) Быстрота наступления лечебного эффекта (в первые 2 - 3 дня) Наносить на лицо, шею, складки не более 5 дней Наносить на лицо, шею, складки не более 14 дней Преимущественно на небольшие поверхности Преимущественно на большие поверхности Лекарственная форма - мазь, крем Лекарственная форма - крем Высокая местная безопасность Высокая местная безопасность Применять 2 раза в день Применять 1 раз в день «Линия» с комбинациями действующих веществ (Акридерм) Монопрепарат(Унидерм) Безрецептурный препарат Рецептурный препарат Разрешено применение у детей с 1 года Разрешено применение у детей с 6 месяцев Учитывая длительный характер течения многих кожных заболеваний, в настоящее время все более актуальной становится интермиттирующая схема применения топических ГКС - два дня в неделю или через день в течение нескольких месяцев. Эффективность и безопасность этой схемы доказана зарубежными и российскими исследованиями [15 - 17].
Одним из возможных вариантов топической кортикостероидной терапии является комбинирование с антимикотическими или антибактериальными препаратами [18 - 20]. Так, при наличии сопутствующих инфекций эффективно применение таких препаратов, как Акридерм СК, Акридерм ГК и Акридерм Гента, в состав которых входит бетаметазона дипропионат в качестве действующего кортикостероида, а также салициловая кислота (СК), антибиотик гентамицин (Гента) или гентамицин и противогрибковое средство клотримазол (ГК) соответственно [21]. Однако следует отметить: проведенные рандомизированные исследования показали, что использование только стероидов для терапии бактериальных и микотических инфекций было столь же эффективно, как и использование комбинированных топических препаратов [22 - 24].
В настоящее время «сильные» топические ГКС (бетаметазона дипропионат и мометазона фуроат) рекомендованы ведущими специалистами в России и за рубежом в качестве препаратов выбора при лечении многих дерматозов.
Список использованной литературы
- Weston W. L. The use and abuse of topical steroids // Contemp. Pediatr. - 1988. - Vol. 5. - P. 57 - 66.
- Medansky R. S., Brody N. I., Kanof N. B. Clinical investigations of momethasone furoate - a novel, non-fluorinated, topical corticosteroid // Semin. Dermatol. - 1987. - Vol. 6. - P. 94 - 100.
- Viglioglia P., Jones M. L., Peers E. A. Once daily 0.1% momethasone furoate cream versus twice daily 0.1% betamethasone valerate cream in the treatment of a variety of dermatoses // J. Int. Med. Res. - 1990. - Vol. 18. - P. 460 - 467.
- Roumestan C., Henriquet C., Bousquet J. et al. Fluticasone propionate and mometasone furoate have equivalent transcriptional potencies // Clin. Exp. Allergy. - 2003. - Vol. 33. - P. 895 - 901.
- Umland S.P., Schleimer R.P., Johnston S.L. Review of the molecular and cellular mechanisms of action of glucocorticoids for use in asthma // Pulmonary Pharmacol. & Therapeutics. - 2002. - Vol. 15. - P. 35 - 50.
- Stoppoloni G., Prisco F., Santinelli R. Potential hazards of topical steroid therapy // Am. J. Dis. Child. - 1983. - Vol. 137. - P. 1130 - 1331.
- Faergemann J., Christensen O., Sjovall P. et al. An open study of efficacy and safety of long-term treatment with mometasone furoate fatty cream in the treatment of adult patients with atopic dermatitis // J. Eur. Acad. Dermatol. Venereol. -2000. - Vol. 14, № 5. - P. 393 - 396.
- Потекаев Н. Н., Жукова О. В., Лекашева Н. Н. и др. Неинвазивные методы диагностики в оценке эффективности наружной терапии хронических воспалительных дерматозов // Клин. дерматол. и венерол. - 2010. - № 2. - P. 32 - 37.
- Короткий Н. Г., Гамаюнов Б. Н., Тихомиров А. А. Практика применения новых наружных средств в лечении атопического дерматита у детей // Клин. дерматол. и венерол. - 2010. - № 1. - P. 2 - 6.
- Green С., Colquitt J. L., Kirby J. et al. Clinical and cost-effectiveness of once-daily versus more frequent use of same potency topical corticosteroids for atopic eczema: a systematic review and economic evaluation // Health Technol. Assessment. - 2004. - Vol. 8. - P. 47.
- Tayab Z. R., Fardon T. C., Lee D. K. C. et al. Pharmacokinetic/pharmacodynamic evaluation of urinary cortisol suppression after inhalation of fluticasone propionate and mometasone furoate // Br. J. Clin. Pharmacol. - 2007. - Vol. 64, № 5. - P. 698 - 705
- Bruni F. M., De Luca G., Venturoli V. et al. Intranasal corticosteroids and adrenal suppression // Neuroimmunomodulation. - 2009. - Vol. 16, № 5. - P. 353 - 362.
- Lebrun-Vignes B., Legrain V., AmoricJ. et al. Comparative study of efficacy and effect on plasma cortisol levels of micronised desonide cream 0.1 p. 100 versus betamethasone dipropionate cream 0.05 p. 100 In the treatment of childhood atopic dermatitis // Ann. Dermatol. Venereol. - 2000. - Vol. 127, № 6 - 7. - P. 590 - 595.
- Delescluse J., van der EndtJ. D. A comparison of the safety, tolerability, and efficacy of fluticasone propionate ointment, 0.005%, and betamethasone-17,21-dipropionate ointment, 0.05%, in the treatment of eczema // Cutis. - 1996. - Vol. 57, № 2, Suppl. - P. 32 - 38.
- Hanifin J., Gupta A. K., Rajagopalan R. Intermittent dosing of fluticasone propionate cream for reducing the risk of relapse in atopic dermatitis patients // J. Dermatol. - 2002. - Vol. 147, № 3. - P. 528 - 537.
- Veien N. K., Olholm Larsen P., Thestrup-Pedersen K. et al. Long-term, intermittent treatment of chronic hand eczema with mometasone furoate // Br. J. Dermatol. - 1999. - Vol. 140, № 5. - P. 882 - 886.
- Соколовский Е. В., Монахов К. Н., Холодилова Н. А. и др. Интермиттирующая терапия бетаметазоном атопического дерматита и экземы кистей // Рос. журн. кожн. и венер. болезней. - 2009. - № 3. - С. 16 - 21.
- Larsen F. S., Simonsen L., Melgaard A. et al. An efficient new formulation of fusidic acid and betamethasone 17-valerate (fucicort lipid cream) for treatment of clinically infected atopic dermatitis // Acta Derm. Venereol. - 2007. - Vol. 87, № 1. - P. 62 - 68.
- Khobragade K.J. Efficacy and safety of combination ointment «fluticasone propionate 0.005% plus mupirocin 2.0%" for the treatment of atopic dermatitis with clinical suspicion of secondary bacterial infection: an open label uncontrolled study // Indian J. Dermatol. Venereol. Leprol. - 2005. - Vol. 71, № 2. - P. 91 - 95.
- Hjorth N., Schmidt H., Thomsen K. Fusidic acid plus betamethasone in infected or potentially infected eczema // Pharmatherapeutica. - 1985. - Vol. 4, № 2. - P. 126 - 131.
- Матушевская Е. В., Шакуров И. Г., Хисматулина З. Р. Эффективность и переносимость препаратов «линии» Акридерм® в практике дерматовенеролога // Клин. дерматол. и венерол. - 2008. - № 2. - С. 2 - 4.
- Mosges R., Domrose C. M., Loffler J. Topical treatment of acute otitis externa: clinical comparison of an antibiotics ointment alone or in combination with hydrocortisone acetate // Eur. Arch. Otorhinolaryngol. - 2007. - Vol. 264, № 9. - P. 1087 - 1094.
- Gong J. Q., Lin L., Lin T. et al. Skin colonization by Staphylococcus aureus in patients with eczema and atopic dermatitis and relevant combined topical therapy: a double-blind multicentre randomized controlled trial // Br. J. Dermatol. - 2006. - Vol. 155, № 4. - P. 680 - 687.
- Birnie A.J., Bath-Hextall F.J., Ravenscroft J. C. et al. Interventions to reduce Staphylococcus aureus in the management of atopic eczema // Cochrane Database Syst. Rev. - 2008. - Vol. 16, № 3. - CD003871.
| Сентябрь 2013 г. |