Опубликовано в журнале:
CONSILIUM MEDICUM »» ТОМ 5 №11Различия фармакологических свойств бета-адреноблокаторов и их клиническое значение
А.Я.Ивлева
Поликлиника №1 Медицинского центра Управления делами Президента РФ, МоскваВ первые в клиническую практику бета-адреноблокаторы были внедрены 40 лет назад в качестве антиаритмических средств и для лечения стенокардии. В настоящее время они являются наиболее эффективными средствами для вторичной профилактики после перенесенного острого инфаркт миокарда (ОИМ). Доказана их эффективность в качестве средств для первичной профилактики сердечно-сосудистых осложнений при лечении гипертонии. В 1988 г. создателям бета-адреноблокаторов была присуждена Нобелевская премия. Нобелевский комитет оценил значение препаратов этой группы для кардиологии как сопоставимое с дигиталисом. Интерес к клиническому изучению бета-адреноблокаторов оказался оправданным. Блокада бета-адренорецепторов стала терапевтической стратегией при ОИМ, направленной на снижение летальности и уменьшение зоны инфаркта. За последнее десятилетие было установлено, что бета-адреноблокаторы уменьшают летальность при хронической сердечной недостаточности (ХСН) и предупреждают кардиальные осложнения при внекардиальных хирургических операциях. В контролируемых клинических исследованиях была подтверждена высокая эффективность бета-адреноблокаторов в особых группах пациентов, в частности у страдающих сахарным диабетом и пожилых.
Однако последние широкомасштабные эпидемиологические исследования (IMPROVEMENT, EUROASPIRE II и Euro Heart Failure survey) показали, что бета-адреноблокаторы применяются реже, чем следовало бы в ситуациях, где они могли бы принести пользу [1,2], поэтому для внедрения в медицинскую практику современной стратегии превентивной медицины требуются усилия со стороны ведущих клиницистов и ученых для разъяснения фармакодинамических преимуществ отдельных представителей группы бета-адреноблокаторов и обоснования новых подходов к решению сложных клинических проблем с учетом различий в фармакологических свойствах препаратов.
Бета-адреноблокаторы являются конкурентными ингибиторами связывания медиатора симпатической нервной системы с бета-адренорецепторами. Норадреналин играет важнейшую роль в генезе гипертонии, инсулинорезистентности, сахарного диабета и атеросклероза. Уровень норадренали-на в крови повышается при стабильной и нестабильной стенокардии, ОИМ и в период ремоделирования сердца. При ХСН уровень норадреналина варьирует в широком диапазоне и повышается по мере нарастания функционального класса по NYHA. При патологическом повышении симпатической активности инициируется цепь прогрессирующих патофизиологических изменений, завершением которых является сердечно-сосудистая летальность. Повышенный симпатический тонус может провоцировать аритмии и внезапную смерть. В присутствии бета-адреноблокатора необходима более высокая концентрация агониста норадреналина для реакции специфического рецептора.
Для врача клинически наиболее доступным маркером повышенной симпатической активности является высокая частота сердечных сокращений (ЧСС) в покое [У]. В 20 больших эпидемиологических исследованиях с включением более 288 000 человек, завершившихся за последние 20 лет, получены данные о том, что частый ритм работы сердца является самостоятельным фактором риска сердечно-сосудистой летальности в популяции в целом и прогностическим маркером развития ИБС, гипертонии, сахарного диабета [4]. Обобщенный анализ эпидемиологических наблюдений позволил установить, что в когорте с ЧСС в диапазоне 90—99 уд/мин частота летальности от осложнений ИБС и внезапной смерти выше в 3 раза по сравнению с группой популяции, имеющей ЧСС менее 60 уд/мин [5]. Установлено, что высокий ритм сердечной деятельности достоверно чаще регистрируется при артериальной гипертонии (АГ) и ИБС. После перенесенного ОИМ ЧСС приобретает значение независимого прогностического критерия летальности как в раннем постинфарктном периоде, так и летальности за 6 мес после ОИМ. Многие эксперты считают оптимальной ЧСС до 80 уд/мин в покое и наличие тахикардии констатируют при ЧСС выше 85 уд/мин [6].
Исследования уровня норадреналина в крови, его обмена и тонуса симпатической нервной системы в норме и при патологических состояниях с использованием высоких экспериментальных технологий с применением радиоактивных веществ, микронейрографии, спектрального анализа позволили установить, что бета-адреноблокаторы устраняют многие токсические эффекты, характерные для кате-холаминов [7]:
- перенасыщение цитозола кальцием и защищают миоциты от некроза,
- стимулирующее влияние на клеточный рост и апоптоз кардиомиоцитов,
- прогрессирование фиброза миокарда и гипертрофии миокарда левого желудочка (ГМЛЖ),
- повышенный автоматизм миоцитов и фибрилляторное действие,
- гипокалиемию и проаритмическое действие,
- повышенное потребление кислорода миокардом при гипертонии и ГМЛЖ,
- гиперренинемию,
- тахикардию.
Существует ошибочное мнение, что при правильном дозировании любой бета-адреноблокатор может быть эффективен при стенокардии, АГ и аритмии. Однако между препаратами этой группы имеются клинически важные фармакологические различия, такие как селективность по отношению к Бета-адренорецепторам, различия по липофильности, присутствию свойств частичного агониста бета-адренорецеп-торов, а также различия по фармакокинетическим свойствам, определяющим стабильность и продолжительность действия в клинических условиях. Фармакологические свойства бета-адреноблокаторов, представленные в табл. 1, могут иметь клиническое значение как при выборе препарата на начальном этапе применения, так и при переходе с одного бета-адреноблокатора на другой.
Сила связывания со специфическим рецептором, или прочность связи лекарственного средства с рецептором, определяет концентрацию медиатора норадреналина, которая требуется для преодоления конкурентной связи на уровне рецептора. Как следствие терапевтические дозы би-сопролола и карведилола ниже, чем у атенолола, метопро-лола и пропранолола, у которых связь с бета-адренорецепто-ром менее прочная.
Селективность блокаторов к Бета-адренорецепторам отражает способность препаратов в разной степени блокировать влияние адреномиметиков на специфические бета-адре-норецепторы в разных тканях. К селективным Бета-адреноб-локаторам относятся бисопролол, бетаксолол, небиволол, метопролол, атенолол, а также редко применяемые в настоящее время талинолол, окспренолол и ацебутолол. При использовании в низких дозах Бета-адреноблокаторы проявляют эффекты блокады адренорецепторов, которые относятся к подгруппе "Pj", поэтому их действие проявляется в отношении органов, в тканевых структурах которых представлены преимущественно Бета-адренорецепторы, в частности в миокарде, и мало влияют на бета2-адренорецепторы в бронхах и сосудах. Однако в более высоких дозах они блокируют также и бета-адренорецепторы. У некоторых пациентов даже селективные Бета-адреноблокаторы способны спровоцировать бронхоспазм, поэтому при бронхиальной астме применение бета-адреноблокаторов не рекомендовано. Коррекция тахикардии у пациентов с бронхиальной астмой, получающих бета-адреномиметики, является клинически одной из наиболее актуальных и одновременно трудно решаемых проблем, особенно при сопутствующей ишемической болезни сердца (ИБС), поэтому повышение селективности Бета-адреноблокаторов является особенно важным клинически свойством для этой группы пациентов. Имеются данные, что у метопролола сукцината CR/XL селективность к Бета-адренорецепторам выше, чем у атенолола. В кли-нико-экспериментальном исследовании он достоверно меньше влиял на объем форсированного выдоха у больных бронхиальной астмой, а при применении форматерола обеспечивал более полное восстановление бронхиальной проходимости, чем атенолол [8].
Таблица 1.
Клинически важные фармакологические свойства бета-адреноблокаторов
Препарат
Сила связывания с бета-адренорецептором (пропранолол=1 ,0)
Относительная селективность к бета-рецептору
Внутренняя симпатомиметическая активность
Мембрано-стабилизирующая активность
Атенолол
1,0
++
0
0
Бетаксолол
1,0
++
0
+
Бисопролол
10,0
++
0
0
Буциндолол
1,0
0
+
+
Карведилол*
10,0
0
0
++
Эсмолол
0,02
++
0
0
Лабетолол**
0,3
0
+
0
Метопролол
1,0
++
0
0
Небиволол
Нет данных
+++
0
0
Пенбутолол
1,0
0
+
0
Пиндолол
6,0
0
++
+
Пропранолол
1,0
0
0
++
Соталол****
0,3
0
0
0
Тимолол
6,0
0
0
0
Примечание. Относительная селективность (по Wellstern и соавт., 1987, цит. по [7]); * - карведилол обладает дополнительно свойством бета-адреноблокатора; ** - лабетолол обладает дополнительно свойством а-адреноблокатора и внутренним свойством агониста бета-адрено-рецепторов; *** - соталол обладает дополнительными антиаритмическими свойствами
Селективность по отношению к Бета-адренорецепторам имеет важное клиническое значение не только при бронхообструктивных заболеваниях, но и при использовании у пациентов с АГ, при заболеваниях периферических сосудов, в частности при болезни Рейно и перемежающейся хромоте. При использовании селективных Бета-адреноблокаторов бета2-адренорецепторы, оставаясь активными, реагируют на эндогенные катехоламины и экзогенные адрено-миметики, что сопровождается вазодилатацией. В специальных клинических исследованиях установлено, что высокоселективные Бета-адреноблокаторы не повышают сопротивления сосудов предплечья, системы бедренной артерии, а также сосудов области каротид и не влияют на переносимость шаговой пробы при перемежающейся хромоте.
Метаболические эффекты бета-адреноблокаторов
При длительном (от 6 мес до 2 лет) применении неселективных бета-адреноблокаторов повышаются триглицериды в крови в широком диапазоне (от 5 до 2 5%) и снижается холестерин фракции липопротеинов высокой плотности (ХСЛПВП) в среднем на 13%. Влияние неселективных р-ад-реноблокаторов на липидный профиль связывают с инги-бированием липопротеинлипазы, так как бета-адренорецеп-торы, снижающие активность липопротеинлипазы, оказываются без контррегуляции со стороны бета2-адренорецепто-ров, являющихся их антагонистами в отношении этой ферментативной системы. При этом наблюдается замедление катаболизма липопротеинов очень низкой плотности (ЛПОНП) и триглицеридов. Количество ХСЛПВП уменьшается, поскольку эта фракция холестерина является продуктом катаболизма ЛПОНП. Убедительной информации о клиническом значении влияния неселективных бета-адреноб-локаторов на липидный профиль до сего времени не получено, несмотря на огромное количество наблюдений разной продолжительности, представленных в специальной литературе. Повышение триглицеридов и снижение ХСЛПВП не характерно для высокоселективных Бета-адре-ноблокаторов, более того, имеются данные, что метопро-лол замедляет процесс атерогенеза [9].
Влияние на обмен углеводов опосредуется через бета2-адренорецепторы, так как через эти рецепторы регулируются секреция инсулина и глюкагона, гликогенолиз в мускулатуре и синтез глюкозы в печени. Применение неселективных бета-адреноблокаторов при сахарном диабете типа 2 сопровождается повышением гипергликемии, а при переходе на селективные Бета-адреноблокаторы эта реакция устраняется полностью. В отличие от неселективных бета-адреноблокаторов селективные Бета-адреноблокаторы не удлиняют гипогликемию, индуцированную инсулином, так как гликогенолиз и секреция глюкагона опосредуются через бета2-адренорецепторы. В клиническом исследовании было установлено, что метопролол и бисопролол по влиянию на углеводный обмен при сахарном диабете типа 2 не отличаются от плацебо и коррекции гипогликемических средств не требуется [10]. Тем не менее чувствительность к инсулину снижается при использовании всех бета-адреноблокаторов, причем под влиянием неселективных бета-адреноблокаторов более существенно.
Мембраностабилизирующая активность бета-адреноблокаторов обусловлена блокадой натриевых каналов. Она свойственна лишь некоторым бета-адреноблокаторам (в частности, имеется у пропранолола и некоторых других, не имеющих клинического значения в настоящее время). При применении терапевтических доз мембраностабилизиру-ющее действие бета-адреноблокаторов не имеет клинического значения. Оно проявляется нарушениями ритма при интоксикации вследствие передозировки.
Наличие свойств частичного агониста бета-адреноре-цепторов лишает препарат способности снижать ЧСС при тахикардии. По мере того как накапливались доказательства снижения летальности у пациентов, перенесших ОИМ, при терапии бета-адреноблокаторами, становилась все более достоверной корреляционная связь их эффективности с уменьшением тахикардии [11]. Было установлено, что препараты со свойствами частичных агонистов бета-адреноре-цепторов (окспренолол, практолол, пиндолол) мало влияли на ЧСС и летальность в отличие от метопролола, тимолола, пропранолола и атенолола. В дальнейшем, в процессе исследования эффективности бета-адреноблокаторов при ХСН было установлено, что буциндолол, обладающий свойствами частичного агониста, не изменял ЧСС и не оказывал существенного влияния на летальность в отличие от метопролола, карведилола и бисопролола [12].
Вазодилатирующее действие присутствует лишь у некоторых бета-адреноблокаторов (карведилол, небиволол, лабетолол) и может иметь важное клиническое значение. Для лабеталола этот фармакодинамический эффект определил показания и ограничения для его применения. Однако клиническая значимость сосудорасширяющего действия других бета-адреноблокаторов (в частности, карведилола и неби-валола) пока не получила полной клинической оценки.
Таблица 2.
Фармакокинетические показатели наиболее часто применяемых бета-адреноблокаторов [7]
Препарат
Биодоступность, %
Липофильность
Период полувыведения, ч
Атенолол
40-60
6-9
Бетаксолол
80-90
++
16-22
Бисопролол
90
+
10-12
Метопролол
40-50
+
3-6
Надолол
30-50
-
14-24
Пропранолол
20-30
+++
3-5
П индол ол
90
+
3-4
Карведилол
25
+
7
Небиволол
12-96
+++
10-11
Липофильность и гидрофильность бета-адреноблока-торов определяет их фармакокинетические характеристики и способность влиять на тонус вагуса. Водорастворимые бета-адреноблокаторы (атенолол, соталол и нодалол) из организма элиминируются преимущественно через почки и мало метаболизируются в печени. Умеренно липофильные (бисопролол, бетаксолол, тимолол) имеют смешанный путь элиминации и частично метаболизируются в печени. Высо-колипофильный пропранолол метаболизируется в печени более чем на 60%, метопролол подвергается метаболизму в печени на 95%. Фармакокинетические характеристики наиболее часто используемых бета-адреноблокаторов представлены в табл. 2. Специфические фармакокинетические свойства препаратов могут быть клинически важными. Так, у препаратов с очень быстрым метаболизмом в печени в системный кровоток попадает лишь небольшая часть всосавшегося в кишечнике препарата, поэтому при приеме внутрь дозы таких препаратов намного выше, чем применяемые парентерально внутривенно. У жирорастворимых бета-адре-ноблокаторов, таких как пропранолол, метопролол, тимолол и карведилол, существует генетически предопределенная вариабельность фармакокинетики, что требует более тщательного подбора терапевтической дозы.
Липофильность повышает проникновение бета-адренобло-катора через гематоэнцефалический барьер. Эксперимен-дально доказано, что при блокаде центральных Бета-адрено-рецепторов повышается тонус вагуса, и это имеет важное значение в механизме антифибрилляторного действия. Имеются клинические данные о том, что применение препаратов, обладающих липофильностью (клинически доказано для пропранолола, тимолола и метопролола) сопровождается более существенным снижением частоты внезапной смерти у пациентов высокого риска. Клиническое значение липофильности и способности препарата проникать через гематоэнцефалический барьер нельзя считать полностью установленным в отношении таких эффектов центрального действия, как сонливость, депрессии, галлюцинации, так как не доказано, что водорастворимые бета1ад-реноблокаторы, такие как атенолол, вызывают меньше подобных нежелательных эффектов.
Клинически важно, что:
- при нарушении функции печени, в частности вследствне сердечной недостаточности, а также при совместном применении с лекарственными средствами, конкурирующими в процессе метаболической биотрансформации в печени слипофилъными бета-адреноблокаторами, дозы или частоту приемов липофилъных fS-адреноблокаторов следует уменьшать.
- при серьезных нарушениях функции почек требуется снижение доз или коррекция частоты приема гидрофильных бета-адреноблокаторов.
Стабильность действия препарата, отсутствие выраженных колебаний концентрации в крови являются важной фармакокинетической характеристикой. Совершенствование лекарственной формы метопролола привело к созданию препарата с контролируемым медленным высвобождением. Метопролола сукцинат CR/XL обеспечивает стабильную концентрацию в крови на протяжении 24 ч без резких повышений содержания. При этом изменяются и фармакодинамические свойства метопролола: у метопролола CR/XL клинически установлено повышение селективности к Бета-адренорецепторам, поскольку при отсутствии пиковых колебаний концентрации менее чувствительные бета2-адренорецепторы остаются полностью интактными [13, 14].
Клиническая ценность бета-адреноблокаторов при ОИМ
Самая частая причина летальных исходов при ОИМ — нарушения ритма. Однако риск остается повышенным, и в постинфарктном периоде большинство летальных исходов наступает внезапно. Впервые в рандомизированном клиническом исследовании MIAMI (1985 г.) было установлено, что применение бета-адреноблокатора метопролола при ОИМ снижает летальность. Метопролол вводили внутривенно на фоне ОИМ с последующим применением этого препарата внутрь. Тромболизис при этом не производили. Отмечено снижение летальности за 2 нед на 13% по сравнению с группой пациентов, получавших плацебо [15]. Позднее в контролируемом исследовании TIMI П-В применяли метопролол внутривенно на фоне тромболизиса и добились снижения повторных инфарктов за первые 6 дней с 4,5 до 2,3% [16].
При применении бета-адреноблокаторов при ОИМ достоверно снижается частота угрожающих жизни желудочковых аритмий и фибрилляции желудочков, реже развивается синдром удлинения интервала Q—T, предшествующий фибрилляции. Как показали результаты рандомизированных клинических исследований - ВНАТ (пропранолол), Норвежское исследование (тимолол) и Гетеборгское исследование (метопролол) - применение бета-адреноблокатора позволяет снизить летальность от повторного ОИМ и частоту повторных нелетальных инфарктов миокарда (ИМ) за первые 2 нед в среднем на 20-25%.
На основании клинических наблюдений были разработаны рекомендации по внутривенному применению бета-адреноблокаторов в остром периоде ИМ в первые 24 ч. Метопролол, наиболее изученный клинически при ОИМ, рекомендуется использовать внутривенно по 5 мг за 2 мин с перерывом в 5 мин, всего 3 дозы. Затем препарат назначают внутрь по 50 мг каждые 6 ч в течение 2 сут, а в последующем — по 100 мг 2 раза в день. При отсутствии противопоказаний (ЧСС менее 50 уд/мин, САП менее 100 мм рт. ст., наличие блокады, отека легких, бронхоспазма или в случае, если пациент получал верапамил до развития ОИМ) лечение продолжают длительно.
Было установлено, что применение препаратов, обладающих липофильностью (доказано для тимолола, метопролола и пропранолола), сопровождается существенным снижением частоты внезапной смерти при ОИМ у пациентов высокого риска. В табл. 3 представлены данные контролируемых клинических исследований с оценкой клинической эффективности липофильных бета-адреноблокаторов при ИБС по снижению частоты внезапной смерти при ОИМ и в раннем постинфарктном периоде.
Клиническая ценность бета-адреноблокаторов в качестве средств для вторичной профилактики при ИБС
В постинфарктном периоде применение бета-адреноблокаторов обеспечивает достоверное, в среднем на 30%, снижение сердечно-сосудистой летальности в целом. По данным Гетеборгского исследования и метанализа, применение метопролола обеспечивает снижение летальности в постинфарктном периоде на 36—48% в зависимости от уровня риска [19]. бета-адреноблокаторы являются единственной группой лекарственных средств для медикаментозной профилактики внезапной смерти у пациентов, перенесших ОИМ [10, 21]. Однако не все бета-адреноблокаторы одинаковы.
Таблица 3.
Контролируемые клинические исследования, в которых установлено снижение внезапной смерти при применении липофильных бета-адреноблокаторов при ОИМ
Исследование
Число пациентов
Эфективность, %
Норвежское исследование (тимолол) [17]
Более 1 800
-51
ВНАТ(пропранолол) [18]
Более 3800
-28
Метанализ (метопролол) [19]
Более 5400
-41
На рис. 1 представлены обобщенные данные по снижению летальности в постинфарктном периоде, зарегистрированные в рандомизированных клинических исследованиях при использовании бета-адреноблокаторов с группировкой в зависимости от наличия дополнительных фармакологических свойств [22].
Метанализ данных плацебо-контролируемых клинических исследований показал достоверное снижение летальности в среднем на 22% при длительном применении бета-адреноблокаторов у пациентов, ранее перенесших ОИМ, частоты реинфаркта на 27%, снижение частоты внезапной смерти, особенно в ранние утренние часы, в среднем на 30% [23]. Летальность после перенесенного ОИМ у пациентов, получавших метопролол в Гетеборгском исследовании, у которых имелись симптомы сердечной недостаточности, снизилась на 50% по сравнению с группой, получавших плацебо [19].
Клиническая эффективность бета-адреноблокаторов была установлена как после трансмурального ИМ, так и у лиц, перенесших ОИМ без Q на ЭКГ Особенно высока эффективность у пациентов из группы высокого риска: курящих, лиц пожилого возраста, при ХСН, сахарном диабете.
Различия антифибрилляторных свойств бета-адреноблокаторов более убедительны при сравнительной оценке результатов клинических исследований с использованием липофильных и гидрофильных препаратов, в частности результатов, зарегистрированных при применении водорастворимого соталола [25]. Клинические данные свидетельствуют о том, что липофильность является важным свойством препарата, которое по крайней мере отчасти объясняет клиническую ценность бета-адреноблокаторов в профилактике внезапной аритмической смерти при ОИМ и в постинфарктный период, так как их ваготропное антифибрилля-торное действие имеет центральное происхождение [25-27].
При длительном применении липофильных бета-адреноблокаторов особенно важным свойством представляется ослабление стресс-индуцированного подавления тонуса вагу-са и усиление ваготропного влияния на сердце. Превентивное кардиопротективное действие, в частности снижение внезапной смерти в отдаленном постинфарктном периоде, в значительной мере обусловлено этим эффектом бета-адреноблокаторов. В табл. 4 представлены данные о липофиль-ности и кардиопротективных свойствах, установленных в контролируемых клинических исследованиях при ИБС.
Эффективность бета-адреноблокаторов при ИБС объясняется как их антифибрилляторным, антиаритмическим, так и антиишемическим действиями. бета-адреноблокаторы оказывают благоприятное воздействие на многие механизмы развития ишемии миокарда. Полагают также, что бета-адреноблокаторы способны уменьшать вероятность разрыва атероматозных образований с последующим тромбозом.
В клинической практике врачу следует ориентироваться на изменение ЧСС при терапии бета-адреноблокаторами, клиническая ценность которых в значительной мере обусловлена их способностью уменьшать ЧСС при тахикардии [2 5]. В современных международных экспертных рекомендациях по лечению ИБС с применением бета-адреноблокаторов целевой ЧСС является от 55 до 60 уд/мин, а в соответствии с рекомендациями Американской ассоциации сердца в тяжелых случаях ЧСС можно снизить до 50 уд/мин и менее.
В работе Hjalmarson и соавт. представлены результаты изучения прогностического значения ЧСС у 1807 пациентов, поступивших с ОИМ. В анализ включили как пациентов с развившейся впоследствии ХСН, так и без нарушения гемодинамики. Оценивали летальность за период со второго дня госпитализации до 1 года. Было установлено, что частый ритм работы сердца прогностически неблагоприятен [29]. При этом были зарегистрированы следующие показатели смертности в течение года в зависимости от ЧСС при поступлении:
- при ЧСС 50-60 уд/мин - 15%;
- при ЧСС выше 90 уд/мин - 41%;
- при ЧСС выше 100 уд/мин - 48%.
В широкомасштабном исследовании GISSI-2 с контингентом пациентов 8915 за период наблюдения в течение 6 мес было зарегистрировано 0,8% смертей в группе с ЧСС менее 60 уд/мин в период тромболизиса и 14% в группе с ЧСС выше 100 уд/мин [30]. Результаты исследования GISSI-2 подтверждают наблюдения 80-х годов XX в. о прогностическом значении ЧСС при ОИМ, лечение которого производилось без тромболизиса. Координаторы проекта предложили включить в клиническую характеристику в качестве прогностического критерия ЧСС и считать бета-адреноблока-торы препаратами первого выбора для превентивной терапии пациентов с ИБС и высокой ЧСС.
На рис. 2 представлена зависимость частоты развития повторного ИМ при применении бета-адреноблокаторов с разными фармакологическими свойствами для вторичной профилактики осложнений ИБС, по данным рандомизированных контролируемых исследований [31].
Клиническая ценность бета-адреноблокаторов при лечении гипертонии
В ряде широкомасштабных рандомизированных клинических исследований (SHEP Cooperative Research Group, 1991; MRC Working Party, 1992; IPPPSH, 1987; HAPPHY, 1987; MAPHY,1988; STOP Hypertension, 1991) было установлено, что применение бета-адреноблокаторов в качестве антигипер-тензивных средств сопровождается снижением частоты сердечно-сосудистой летальности как у молодых, так и у пациентов старших возрастных групп. В международных экспертных рекомендациях бета-адреноблокаторы отнесены к препаратам первой линии для лечения АГ [32].
Выявлены этнические различия в эффективности бета-адреноблокаторов как антигипертензивных средств. В целом они более эффективно корригируют АД у молодых пациентов белой расы и при высокой ЧСС.
Рис. 1.
Уменьшение летальности при использовании бета-адреноблокаторов после инфаркта миокарда в зависимости от дополнительных фармакологических свойств.
Независимо от свойств
ХХХХХХ - 20%
Без свойств агониста
ХХХХХХХХХ- 30%
Со свойством частичного агониста
XXX- 10%
Неселективный
ХХХХХХХХ - 27%
Селективный f^-блокатор
ХХХХХХХХХХХХ - 36%
Таблица 4.
Липофильность и кардиопротективное действие бета-адреноблокаторов по снижению летальности при длительном применении с целью вторичной профилактики кардиальных осложнений при ИБС
Вторичная профилактика, исследование
Препарат
Кардиопротективное действие
Липофильность
ВНАТ[18]
Пропранолол
Установлено
Высокая
Hjalmarson и соавт. [28]
Метопролол
Установлено
Умеренная
Norwegian Study Group [17]
Тимолол
Установлено для всех возрастных групп
Умеренная
Olsson и соавт. [19] (метанализ)
Метопролол
Установлено
Умеренная
Julian [24]
Соталол
Нет
Низкая
Рис. 2.
Зависимость между уменьшением ЧСС при применении разных бета-адреноблокаторов и частотой реин-фаркта (по данным рандомизированных клинических исследований: Pooling Project [31]).
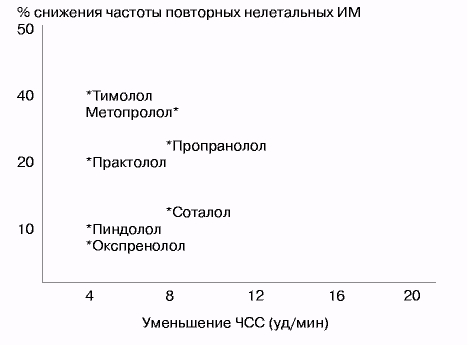
Результаты многоцентрового рандомизированного сравнительного исследования MAPHY, которое было посвящено изучению первичной профилактики атеросклеротических осложнений при лечении гипертонии метопрололом и тиазидным мочегонным у 3234 пациентов в среднем на протяжении 4,2 лет, доказали преимущество терапии селективным бета-адреноблокатором метопрололом. Общая летальность и от коронарных осложнений была достоверно ниже в группе получавших метопролол. Не связанная с сердечнососудистыми заболеваниями летальность была одинаковой в группах метопролола и мочегонного. Кроме того, в группе пациентов, получавших в качестве основного гипотензивного средства липофильный метопролол, была достоверно на 30% ниже частота внезапной смерти, чем в группе, получавших мочегонное [30].
В аналогичном сопоставительном исследовании НАРPHY большинство пациентов в качестве гипотензивного средства получали селективный гидрофильный Бета-адреноблокатор атенолол и при этом существенного преимущества бета-адреноблокаторов или мочегонных не было установлено. Тем не менее при раздельном анализе и в этом исследовании в подгруппе получавших метопролол его эффективность в профилактике сердечно-сосудистых осложнений, как летальных так и нелетальных, была достоверно выше, чем в группе получавших мочегонные [33, 34].
В табл. 5 представлена эффективность бета-адреноблокаторов, получивших документированную оценку в контролируемых клинических исследованиях при использовании для первичной профилактики сердечно-сосудистых осложнений при лечении гипертонии.
До сего времени нет полного понимания механизма антигипертензивного действия препаратов группы бета-адреноблокаторов. Однако практически важны наблюдения о том, что средний показатель ЧСС в популяции лиц с АГ выше, чем у нормотензивной популяции. Сравнение 129 588 нормотензивных лиц и с АГ в рамках Фрамингемско-го исследования позволило установить, что не только средний показатель ЧСС в группе с АГ выше, но и летальность при последующем наблюдении возрастает по мере повышения ЧСС [5, 39]. Такая закономерность наблюдается не только у молодых пациентов (18-30 лет), но и в средней возрастной группе до 60 лет, а также у пациентов старше 60 лет [39]. Повышение симпатического тонуса и снижение парасимпатического регистрируется в среднему 30% пациентов с АГ и, как правило, в ассоциации с метаболическим синдромом, гиперлипидемией и гиперинсулинемией [40, 41,42], и для таких пациентов применение бета-адреноблока-торов можно отнести к патогенетической терапии.
Гипертония сама по себе является лишь слабым предиктором риска развития ИБС для конкретного пациента, но связь с уровнем АД особенно с уровнем систолического АД независима от наличия других факторов риска [35, 43]. Зависимость между уровнем АД и риском ИБС носит линейный характер. Более того, у пациентов, у которых снижение АД в ночной период происходит менее чем на 10% (non-dippers) риск ИБС повышается в 3 раза [43-45]. Среди многочисленных факторов риска развития ИБС гипертония приобретает главную роль вследствие ее распространенности, а также вследствие общности патогенетических механизмов сердечно-сосудистых осложнений при гипертонии и ИБС. Многие факторы риска, такие как дислипидемия, ин-сулинорезистентность, сахарный диабет, ожирение, малоподвижный образ жизни, некоторые генетические факторы, имеют значение как в развитии ИБС, так и АГ [41,42]. В целом у пациентов с АГ число факторов риска развития ИБС выше, чем при нормальном АД. Среди 15% общей популяции взрослого населения с АГ ИБС является самой частой причиной смерти и инвалидизации. Повышение симпатической активности при гипертонии способствует развитию ГМЛЖ и сосудистой стенки, стабилизации высокого уровня АД и снижения коронарного резерва с повышением склонности к коронароспазму Среди пациентов с ИБС частота гипертонии составляет 25% и повышение пульсового давления является высоко агрессивным фактором риска коронарной смерти [44,46].
Снижение АД при гипертонии не устраняет полностью повышеного риска летальности от ИБС у пациентов с АГ. Метанализ по результатам лечения в течение 5 лет 37 000 пациентов с умеренной гипертонией, не страдающих ИБС, показал, что при коррекции АД коронарная летальность и нелетальные осложнения ИБС уменьшаются лишь на 14% [47]. В метанализе с включением данных по лечению гипертонии у лиц старше 60 лет было установлено снижение частоты коронарных осложнений на 19% [36,48].
Лечение АГ у пациентов с ИБС должно быть более агрессивным и более индивидуализированным, чем в ее отсутствие. Единственной группой лекарственных средств, для которых доказано кардиопротективное действие при ИБС в случае применения для вторичной профилактики коронарных осложнений, являются бета-адреноблокаторы независимо от наличия у пациентов сопутствующей гипертонии [23,49, 50].
Прогностическими критериями высокой эффективности бета-адреноблокаторов при ИБС являются высокая ЧСС до применения препарата и низкая вариабельность ритма. Как правило, в таких случаях наблюдается также низкая толерантность к физическим нагрузкам. Несмотря на благоприятные изменения перфузии миокарда вследствие уменьшения тахикардии под влиянием бета-адреноблокаторов при ИБС и гипертонии, у тяжелых пациентов с сопутствующей гипертонией и ГМЛЖ уменьшение сократимости миокарда может быть наиболее важным элементом в механизме их антиангинального действия [8, 37,40, 51].
Среди антигипертензивных средств уменьшение ишемии миокарда — свойство, присущее только бета-адреноблока-торам, поэтому их клиническая ценность при лечении гипертонии не сводится к способности корригировать АД, поскольку многие пациенты с АГ являются и пациентами с ИБС либо с высоким риском ее развития. Применение бета-адреноблокаторов — это наиболее обоснованный выбор фармакотерапии для снижения коронарного риска при гипертонии у пациентов с симпатической гиперактивностью [40, 51].
Клиническая ценность метопролола полностью доказана (уровень А) в качестве средства для первичной профилактики сердечно-сосудистых осложнений при АГ, документировано его антиаритмическое действие и снижение частоты внезапной смерти при АГ и ИБС (Гетеборгское исследование; Норвежское исследование; MAPHY; MRC; IPPPSH; ВНАТ).
К препаратам для лечения АГ в настоящее время предъявляется требование стабильности гипотензивного эффекта при однократном приеме в течение суток Фармакологические свойства липофильного селективного Бета-адренобло-катора метопролола сукцината (CR/XL) в новой лекарстве-ной форме с суточным гипотензивным эффектом полностью соответствуют этим требованиям. Лекарственная форма метопролола сукцината (CR/XL) представляет собой таблетку, разработанную на основе высоких фармацевтических технологий, содержащую несколько сотен капсул метопролола сукцината. После попадания в желудок каждая
Таблица 5.
Кардиопротективное действие бета-адреноблокаторов при длительном применении с целью профилактики сердечно-сосудистых осложнений при АГ
Первичная профилактика при АГ, исследование
Препарат
Кардиопротективное действие
Липофильность
НАРРНУ [33, 34]
Атенолол
Нет
Низкая
IPPPSH [35]
Окспренолол
Недостоверно
Умеренная
MRC [36]
Пропранолол
Установлено
Высокая
MRC [36]
Атенолол
Нет
Низкая
MAPHY [37, 38]
Метопролол
Установлено
Умеренная
капсула под воздействием желудочного содержимого распадается в заданном для нее режиме для проникновения через слизистую оболочку желудка и работает как самостоятельная система доставки препарата в кровоток. Процесс всасывания происходит в течение 20 ч и не зависит от рН в желудке, его моторики и других факторов [14].
Клиническая ценность бета-адреноблокаторов в качестве антиаритмических средств
Бета-адреноблокаторы являются средствами выбора для лечения наджелудочковых и желудочковых нарушений ритма, так как не имеют проаритмического действия, характерного для большинства специфических антиаритмических препаратов.
Суправентрикулярные аритмии при гиперкинетических состояниях, такие как синусовая тахикардия при возбуждении, тиреотоксикозе, стенозе митрального клапана, эктопические предсердные тахикардии и пароксизмаль-ные Суправентрикулярные тахикардии, нередко спровоцированные эмоциональным или физическим напряжением, устраняются бета-адреноблокаторами. При недавно развившихся предсердных фибрилляциях и трепетании бета-адре-ноблокаторы могут восстанавливать синусный ритм или замедлять ЧСС без восстановления синусного ритма вследствие повышения рефрактерного периода AV-узла. бета-адре-ноблокаторы эффективно контролируют ЧСС у больных с постоянной формой мерцательной аритмии. В плацебо-контролируемом исследовании METAFER было доказано, что метопролол CR/XL эффективно стабилизирует ритм после кардиоверсии у пациентов с мерцательной аритмией [52]. Эффективность бета-адреноблокаторов не уступает эффективности сердечных гликозидов при мерцательной аритмии, кроме того, сердечные гликозиды и бета-адренобло-каторы могут применяться в комбинации. При нарушениях ритма, возникающих вследствие применения сердечных гликозидов, бета-адреноблокаторы являются средствами выбора.
Желудочковые аритмии, такие как желудочковые экс-трасистолии, а также пароксизмы желудочковой тахикардии, развивающиеся при ИБС, физических нагрузках, при эмоциональном напряжении, обычно устраняются бета-адре-ноблокаторами. Разумеется, при фибрилляции желудочков требуется кардиоверсия, но при рецидивирующих желудочковых фибрилляциях, спровоцированных физическим напряжением или эмоциональным стрессом, особенно у детей, эффективны бета-адреноблокаторы. Постинфарктные желудочковые аритмии также поддаются терапии бета-адре-ноблокаторами. Желудочковые аритмии при пролапсе митрального клапана и синдроме удлиненного интервала Q—T эффективно устраняются пропранололом.
Нарушения ритма при хирургических операциях и в постоперационном периоде обычно носят транзитор-ный характер, но если они продолжительны, эффективно применение бета-адреноблокаторов. Кроме того, бета-адреноблокаторы рекомендуют для профилактики таких аритмий.
Клиническая ценность бета-адреноблокаторов при ХСН
Новые рекомендации Европейского общества кардиологов по диагностике и лечению ХСН и Американской ассоциации сердца опубликованы в 2001 г. [53, 54]. Принципы рационального лечения сердечной недостаточности обобщены ведущими кардиологами в нашей стране [37]. Они разработаны с учетом данных, полученных по методологии медицины, основанной на доказательствах, и в них впервые подчеркивается важная роль бета-адреноблокаторов в комбинированной фармакотерапии для лечения всех пациентов с легкой, умеренной и тяжелой сердечной недостаточностью со сниженной фракцией выброса. Длительное лечение бета-адреноблокаторами также рекомендуется при систолической дисфункции левого желудочка после перенесенного ОИМ независимо от наличия или отсутствия клинических проявлений ХСН. Официально рекомендованными препаратами для лечения ХСН являются бисопролол, метопролол в медленно высвобождающейся лекарственной форме CR/XL и карведилол. Все три бета-адреноблокатора (метопролол CR/XL, бисопролол и карведилол) обнаружили способность снижать риск летальности при ХСН независимо от причин смерти в среднем на 32-34% [55].
У пациентов, включенных в исследование MERIT-HE, получавших метопролол в лекарственной форме с медленным высвобождением летальность от сердечно-сосудистых причин снизилась на 38%, частота внезапной смерти уменьшилась на 41% и летальность от нарастающей ХСН снизилась на 49%. Все эти данные были высоко достоверными. Переносимость метопролола в медленно высвобождающей лекарственной форме была очень хорошей. Отмена препарата произошла у 13,9%, а в группе плацебо - у 15,3% пациентов. В связи с побочными явлениями прекратили прием метопролола CR/XL 9,8% пациентов, 11,7% прекратили прием плацебо. Отмена в связи с ухудшением ХСН была произведена у 3,2% в группе, получавших метопролол пролонгированного действия, и у 4,2%, получавших плацебо.
Эффективность метопролола CR/XL при ХСН была подтверждена у пациентов моложе 69,4 лет (возраст в подгруппе в среднем 59 лет) и у пациентов старше 69,4 лет (в среднем возраст в старшей подгруппе соответствовал 74 годам). Эффективность метопролола CR/XL была продемонстрирована также при ХСН с сопутствующим сахарным диабетом.
В 2003 г были опубликованы данные исследования СО-МЕТ с включением 3029 пациентов с ХСН для сравнения карведилола (целевая доза 25 мг 2 раза вдень) и метопролола тартрата в лекарственной форме с быстрым высвобождением и в низкой дозе (50 мг 2 раза в день), не соответствующей необходимому режиму терапии для обеспечения достаточной и стабильной концентрации препарата на протяжение суток Исследование, как и следовало ожидать при таких обстоятельствах, показало превосходство карведилола. Однако его результаты не представляют клинической ценности, так как в исследовании MERIT-HE была доказана эффективность по снижению летальности при ХСН метопролола сукцината в медленно высвобождающей лекарственной форме для однократного в течение суток приема в дозе в среднем 159 мг/сут (при целевой дозе 200 мг/сут).
Заключение
Задача настоящего обзора - подчеркнуть важность тщательного физикального обследования пациента и оценки его состояния при выборе тактики фармакотерапии. Для применения бета-адреноблокаторов следует делать акцент на выявление гиперсимпатикотонии, часто сопутствующей наиболее распространенным сердечно-сосудистым заболеваниям. В настоящее время недостаточно данных, чтобы валидировать показатель ЧСС в качестве первичной цели для фармакологической коррекции при ИБС, АГ и ХСН. Однако гипотеза о важности снижения ЧСС при лечении АГ и ИБС научно обоснована уже в настоящее время. Применение бета-адреноблокаторов позволяет сбалансировать повышенное потребление энергии при тахикардии, сопутствующей гиперсимпатикотонии, скорригировать патологическое ремоделирование сердечно-сосудистой системы, отдалить или замедлить прогрессирование функциональной несостоятельности миокарда вследствие нарушения функции самих бета-адренорецепторов (down-regulation) и снижения реакции на катехоламины с прогрессирующим уменьшением сократительной функции кардиомиоцитов. За последние годы было также установлено, что самостоятельным прогностическим фактором риска, особенно у больных, перенесших ОИМ с показателями сниженной сократимости левого желудочка, является сниженная вариабельность сердечного ритма. Полагают, что инициирующим фактором развития желудочковой тахикардии у данной категории больных служит нарушение баланса симпатической и парасимпатической регуляции сердца. Применение бета-адреноблокатора метопролола у больных ИБС приводит к повышению вариабельности ритма преимущественно за счет увеличения влияния парасимпатической нервной системы [56].
Причинами излишней настороженности в назначении бета-адреноблокаторов чаще являются сопутствующие заболевания (в частности, дисфункция левого желудочка, сахарный диабет, преклонный возраст). Однако установлено, что максимальная эффективность селективного Бета-адренобло-катора метопролола CR/XL была зарегистрирована именно в этих группах пациентов.
Литература
1. EUROASP1REII Study Group Lifestyle and risk factor management anduse of dnig therapies in coronary patients from 15 countries. Eur HeartJ 2001; 22: 554-72.
2. Mapeee BJO. Журн. серд. недоспшт. 2002; 4 (1): 28-30.
3. Task Force of the European Society of Cardiology and the North American Sod - ety of Pacing and Electrophysiology. Circulation 1996; 93: 1043-65. 4.KannelW,KannelC,PaffenbargerR, CupplesA. Am HeartJ 1987; 113: 1489-94.
5. Singh BN.J Cardiovascular Pharmacol Therapeutics 2 001; 6 (4): 313 -31.
6. Habib GB. CardiovascularMed 2001; 6: 25-31.
7. CndckshankJM, Prichard BNC. Beta-blockers in clinical practice. 2nd edition. Edinburgh: Churchill-Livingstone. 1994;p. 1-1204.
8. Lofdahl C-G, DaholfC, Westergren G et aL EurJ Clin Pharmacol 1988; 33 (SllppL): S25-32.
9. Kaplan JR, Manusk SB, Adams MR, Clarkson ТВ. Eur HeartJ 1987; 8: 928-44.
1 O.Jonas M, Reicher-Reiss H, Boyko Vetal.Fv} Cardiol 1996; 77: 12 73-7.
U.KjekshusJ.AmJ Cardiol 1986; 57:43F-49F.
12. ReiterMJ, ReiffelJAAmJ Cardiol 1998; 82 (4A):91-9-
13- Head A, Kendall MJ, Maxwell S. Clin Cardiol 1995; 18: 335-40.
14- Lucker P.J Clin Pharmacol 1990; 30 (siippl.): 17-24-
15- The MIAMI Trial Research Group. 1985. Metoprolol in acute myocardial infarction (MIAMI). A randomised placebo controlled international trial. Eur HeartJ 1985; 6: 199-226.
16. RobertsR, Rogers WJ, MuellerHS et al. Circulation 1991; 83: 422-37.
17. Norwegian Study Group. Timolol-induced reduction in mortality and rein - farction in patients surviving acute myocardial infarction. NEnglJ Med 1981; 304: 801-7.
18. Beta-blockers Heart Attack Trial Research Group.A randomized trial of pro -pranolol in patients with acute myocardial infarction: mortality resuUs.JAMA 1982; 247: 1707-13. 19- Olsson G, WikstrandJ, Warnoldl et al. Eur HeartJ 1992; 13: 28-32.
20. Kennedy HL, Brooks MM, Barker AH etalAmJ Cardiol 1997; 80: 29J-34J.
21. Kendall MJ, Lynch KP, HjalmarsonA, Kjekshus J.Ann Intern Med 1995; 123: 358-67.
22. Frishman WH. Postinfarction survival: Role of beta-adrenergic blocade, in Fuster V (ed): Atherosclerosis and Coronary Artery Disease. Philadelphia, Lip - pencott, 1996; 1205-14-
23. YusufS, WittesJ, Friedman L.J Am Med Ass 1988; 260: 2088-93. 24.Julian DG, Prescott RJJackson FS. Lancet 1982; i: 1142-7.
25. KjekshusJ. AmJ Cardiol 1986; 57: 43F-49F.
26. Soriano JB, Hoes AW, Meems L Prog Cardiovasc Dis 199 7; XXXIX: 445-56. 27.AbladB,Bniro T, BjorkmanJA etalJAm Coll Cardiol 1991; 17 (Suppl): 165.
28. HjalmarsonA, ElmfeldtD, HerlitzJ et al. Lancet 1981; ii: 823-7.
29. HjalmarsonA, Gupin E, Kjekshus J etal.AmJ Cardiol 1990; 65: 547-53.
30. Zuanetti G, MantiniL, Hemandesz-Bemal F et al. Eur HeartJ 1998; 19 (Suppl): F19-F26.
31. Beta-Blocker Pooling Project Research Group (BBPP). Subgroup findings from randomised trials in post infarction patients. Eur HeartJ 1989; 9: 8-16. 32.2003 European Society of Hypertension-European Society of Cardiology guidelines for the management of arterial hypertension.} Hypertension 2003; 21: 1011-53.
33.HolmeI, Olsson G, TuomilehtoJ et alJAMA 1989; 262: 3272-3.
34. Wtthelmsen L, BerghmdG, ElmfeldtDetalJHypertension 1907; 5: 561-72.
35- The IPPPSH Collaborative Group. Cardiovascular risk and risk factors in a randomised trial of treatment based on the beta blocker oxprenololj Hyperten - sion 1985; 3:379-92.
36. Medical Research Council Working Party trial of treatment of hypertension in older adults:principal results. BMJ 1992; 304:405-12.
37- Веленков ЮН., Mapeee ВЮ. Принципы рационального лечения сердеч - ной недостаточности M: Media Medica. 2000; С. 149-55-
38. WikstrandJ, Warnoldl, Olsson G et al.JAMA 1988; 259: 1976-82.
39. Gillman M, Kannel W, BelangerA, D'Agostino R.Am HeartJ1993; 125: 1148-54.
40.Julius S. Eur HeartJ 1998; 19 (suppLF): F14-F18. 41. Kaplan NM.J Hypertension 1995; 13 (suppl.2): S1-S5. 42.McInnesGT.JHypertens 1995; 13 (suppl.2):S49-S56.
43. Kannel WB.J Am Med Ass 1996;275: 1571-6.
44. Franklin SS, Khan SA, Wong ND, Larson MG. Circulation 1999; 100: 354-460.
45. Verdecchia P, Porcellatti C, Schilatti С et al. Hypertension 1994; 24:967-78.
46. Collins R, McMahon S. Br Med Bull 1994; 50:272 -98.
47. Collins R, Peto R, McMahon S et al. Lancet 1990; 335: 82 7-38.
48. McMahon S, RodgersA Clin Exp Hypertens 1993; 15: 967-78.
49. First international study of infarct survival collaborative group. Lancet 1986; 2: 57-66.
50. The beta-blocker pooling project research group. Eur HeartJ 1988; 9: 8-16.
51. Patatini P, Casiglia E, Julius S, Pesina AC. Arch Int Med 1999; 159: 585 -92.
52. Kueblkamp V, Schirdewan A, Stangl К et al. Circulation 1998; 98 Suppl. I: 1-663.
53.Remme WJ, Swedberg K. Eur HeartJ 2001; 22: 1527-260.
54. HuntSA.ACC/AHA Guidelines for the Evaluation and Management ofChron - ic Heart Failure in the Adult: Executive Summary. Circulation 2001; 104: 2996-3007.
55.Andersson B, AbergJ.J Am Сой Cardiol 1999; 33: 183A-184A.
56. BouzamondoA, HulotJS, Sanchez P et al. Eur J Heart failure 2003; 5: 281-9.
57. Keeley EC, Page RL, Lange RA et al.AmJ Cardiol 1996; 77: 557-60.
Индекс лекарственных препаратов
Метопролола сукцинат: БЕТАЛОК ЗОК (АстраЗенека)
| Июль 2006 г. |