Опубликовано в:
Информационный бюллетеньАПОПТОЗ И ВИРУСНЫЕ ГЕПАТИТЫ
А. О. Буеверов, Клиника пропедевтики внутренних болезней, гастроэнтерологии и гепатологии им. В.Х. Василенко, Московская медицинская академия им. И.М. Сеченова
Численность популяции клеток в организме связана с двумя противоположно направленными процессами: митотическим размножением и гибелью клеток. Длительное время значение гибели клеток недооценивалось, однако в последнее время интерес к механизмам ее реализации значительно повысился, и эта проблема стала одной из наиболее интенсивно изучаемых областей биологии. На сегодняшний день установлено, что нарушение контроля клеточной гибели ведет к сдвигам гомеостаза и развитию различных патологических состояний.
На клеточном уровне постоянно протекающие деление и рост должны сопровождаться альтернативным процессом удаления старых, поврежденных, мутировавших и других нежелательных для организма клеток. Высокорегулируемую форму программированной смерти клетки с характерными морфологическими и биохимическими признаками определяют как апоптоз (греческое слово, соответствующее русскому "листопаду": аро - отделение, ptosis - падение).
Апоптозу принадлежит важнейшая роль как в физиологических, так и в патологических условиях, ввиду того, что и подавление, и неадекватное усиление апоптоза ведет к патологическим изменениям органов и тканей. В то время как избыточная активация апоптоза, наблюдаемая, в частности, при инфицировании клеток печени гепатотропными вирусами, обусловливает разрушение печеночной ткани, ослабление апоптотической гибели клеток (вызванное, к примеру, мутацией гена, кодирующего проапоптогенный белок р53) служит одним из важнейших факторов канцерогенеза.
Что касается гепатита, наиболее важным диагностическим и прогностическим признаком при многих его формах считается некроз паренхимы, который, однако, значительно отличается от типичных признаков омертвения, наблюдаемых морфологом в других органах. Прежде всего в ткани печени отсутствуют некротизированные гепатоциты, а видны лишь участки печеночной дольки, замещенные мононуклеарными инфильтратами. Вторая особенность - отсутствие полиморфноядерных лейкоцитов (за исключением острого алкогольного гепатита) -стереотипной реакции на некроз во всех тканях. Следовательно, в большинстве случаев хронического поражения печени, в том числе при инфекции гепатотропными вирусами, основным механизмом гибели клеток служит апоптоз. За много лет до открытия апоптоза был описан характерный гистологический признак вирусного гепатита - округлые гомогенные эозинофильные образования, часто содержащие пикнотичное ядро. Эти образования, названные тельцами Каунсильмена, представляют собой не что иное, как гепатоциты в состоянии апоптоза [2]. Кардинальные отличия апоптоза от некроза приведены в таблице 1.
Таблица 1. Основные характеристики апоптоза и некроза
Апоптоз
Некроз
Физиологический или патологический
Только патологический
Регулируемый
Нерегулируемый или
слабо регулируемыйПлазматическая мембрана
интактна до поздней стадииПлазматическая мембрана
разрушается в начальной стадииИнфильтрация полиморфноядерными
лейкоцитами отсутствует
или минимальнаЛейкоцитарная инфильтрация
всегда присутствуетКариопикноз, кариорексис,
фрагментация ДНКНабухание (онкоз) цитоплазмы
и митохондрийОбразование апоптозных телец
с последующим их фагоцитозом
или вторичным некрозомРазрушение
и дезинтеграция клетки
Первая стадия апоптоза - лиганд-рецепторное взаимодействие. Представление о функционировании рецепторов клеточной гибели служит теоретической базой для разработки оптимальной стратегии патогенетического лечения различных заболеваний, в том числе вирусных гепатитов.
Рецепторы клеточной гибели включают Fas-peцептор (Fas-R), TNF-R1, TNF-R2, "рецептор смерти-3" (DR-3) и 4 так называемых TNF-ассоциированных апоптоз-индуцирующих лиганд-рецептора [5]. Наиболее хорошо среди них изучены Fas-R и TNF-R1.
Fas-R (APO-1/CD95) экспрессируется в печени на гепатоцитах, холангиоцитах, активированных звездчатых ретикулоэндотелиоцитах и клетках Купфера и существует в мембраноассоциированной и растворимой формах. Растворимая форма Fas-R, вероятно, служит для связывания Fas-лиганда (Fas-L) не только на СD8+-цитотоксических лимфоцитах и NK-клетках, но и СD4+-Т-лимфоцитах-хелперах 1-го типа, которые, как было недавно установлено, также могут проявлять цитотоксические свойства [I]. Связывание Fas-L растворимым Fas-R уменьшает повреждение печени цитотоксическими иммунными клетками. Это подтверждается экспериментом S. Krams по инъекции мышам антител к Fas-R, что приводило к смерти животных от фульминантной печеночной недостаточности [8].
Экспрессия Fas-R на мембране гепатоцитов индуцируется рядом провоспалительных цитокинов, таких как интерлейкины (ИЛ-1, -2, -6), интерфероны (ИФН-γ), факторы некроза опухоли (TNF-α) и др. Таким образом, вероятно, что воспаление любой природы может способствовать Fas-R-зависимому повреждению печени. Более того, цитокины стимулируют увеличение количества молекул Fas-L на Т- и NK-лимфоцитах. Интересные данные были получены в работе, в которой культура.крысиных гепатоцитов подвергалась воздействию активированных ИЛ-2 NK-клеток и экспериментальных ингибиторов каспаз. Подавление активности каспаз предотвращало апоптоз гепатоцитов, но при этом усиливалась их гибель посредством некроза, что указывает на определенный баланс между этими путями элиминации клеток, осуществляемыми иммунной системой [5].
Связывание Fas-R ведет к его олигомеризации и активации адапторного белка FADD, что в свою очередь вызывает активацию специфического протеолитического фермента каспазы 8; этот ступенчатый процесс представляет собой основной механизм инициации как физиологического,так и патологического апоптоза клеток печени. На этом этапе дальнейшее развитие апоптоза может быть заблокировано активацией ряда факторов, таких как I-FLICE (эндогенная доминантно-негативная форма каспазы 8), bcl-2 и т.н. Х-связанные ингибиторы апоптоза [1, 2, 5].
Внутриклеточный домен TNF-R1 также интенсивно экспрессируется на гепатоцитах и клетках Купфера. Его экспрессия резко повышается при гепатите любой этиологии (вирусный, алкогольный, аутоиммунный и др.). Исследования F. Su и соавторов [10] продемонстрировали, что НВх-протеин вируса гепатита В сенсибилизирует культуру гепатоцитов к TNF-α-индуцированной цитотоксичности. Персистенция HBsAg также сенсибилизирует гепатоцит к TNF-опосредованному апоптозу.
Апоптоз, индуцированный связыванием TNF-α с TNF-R1, подобно взаимодействию Fas-R - Fas-L, требует олигомеризации рецептора и может осуществляться через путь FADD - каспаза 8, а также сходный с ним белок TRADD. Интересно, что гиперэкспрессия TRADD ведет не только к запуску процессов апоптоза, но и к активации ядерного фактора кВ (NFKB), который предотвращает TNF-индуцированную гибель клетки [2, 5].
Следует заметить, что даже в здоровой печени NK- и CD8+-T-лимфoциты печеночных синусоидов содержат больше мРНК ИЛ-15, -18, TNF-α, ИФН-γ по сравнению с периферическими клетками, что свидетельствует о повышенной готовности к осуществлению апоптоза гепатоцитов в случае возникновения их изменений, например, при инфицировании вирусом [7].
Экспрессия Fas-R существенно повышена на мембране гепатоцитов, инфицированных вирусами В и С, и тесно коррелирует с их гистологической активностью [б]. При вирусном гепатите апоптоз может быть как результатом прямого воздействия вируса, так и опосредованным иммунной реакцией. Запуск процессов апоптоза при проникновении в гепатоцит вируса следует рассматривать как своего рода защитный механизм, так как в мертвой клетке репликация вируса становится невозможной. Поэтому "в интересах" вируса - подавить апоптоз и сохранить клетки жизнеспособными. И действительно, некоторые кодируемые вирусами белки обладают антиапоптозной активностью, которая осуществляется подавлением функции проапоптогенного белка р53, инактивацией каспаз, а также усиленной экспрессией мощного ингибитора апоптоза bcl-2. Интересно, что в норме bcl-2 обнаружен в печени только в эпителии желчных протоков, постоянно контактирующих с желчью, но не в гепатоцитах [2].
Однако чаще причиной апоптоза при инфекции гепатотропными вирусами служит не прямое цитотоксическое действие вируса, а иммунная реакция NK- и Т-лимфоцитов на его антигены, расположенные на поверхности инфицированных гепатоцитов.
Т-лимфоциты могут вызывать апоптоз в клетках печени двумя путями. Первый реализуется за счет выброса из Т-клеток перфорина, который образует поры в плазматических мембранах гепатоцитов. Через них в клетки проникают гранзимы - протеазы Т-лимфоцитарных гранул, вызывающие расщепление ряда внутриклеточных ферментов, в том числе каспаз, запускающих апоптозный каскад.
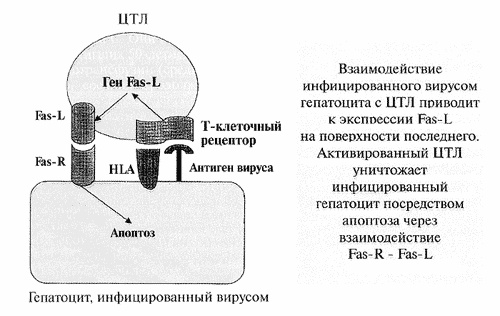
Второй путь осуществления апоптоза под воздействием активированных Т-лимфоцитов связан с рассматривавшимся выше взаимодействием Fas-R -Fas-L (см. рисунок). Как уже упоминалось, Fas-R усиленно экспрессируется на мембране инфицированных гепатотропными вирусами гепатоцитов, но особенно часто их обнаруживают на гепатоцитах, окруженных лимфоцитами на границе ступенчатого некроза и паренхимы [6]. В свою очередь, на соответствующих лимфоцитах выявляется повышенная экспрессия Fas-L. О связи экспрессии Fas и последующего апоптоза с действием вируса гепатита С свидетельствует и то, что после успешного лечения а-интерфероном количество Fas-положительных клеток резко уменьшается и коррелирует как со снижением активности трансаминаз, так и с уменьшением выраженности портальной и лобулярной лимфоидной инфильтрации ткани печени [9]. Наконец, продуцируемый преимущественно макрофагами в избыточных количествах TNF-α также ведет к апоптозу клеток путем взаимодействия с соответствующим рецептором.
Рис. 1. Элиминация инфицированного гепатоцита цитотоксическим Т-лимфоцитом.
(ЦТЛ- цитотоксический Т-лимфоцит)
Понимание механизмов, ведущих к апоптозу клеток печени, в том числе при хроническом вирусном гепатите, позволит разработать новые методы терапии, в частности, уменьшающие избыточную гибель гепатоцитов. Одним из направлений в этой области может служить разработка ингибиторов т.н. проксимальных каспаз (2, 8, 10).
В заключение хотелось бы отметить, что, являясь универсальным биологическим механизмом, апоптоз при вирусных гепатитах может приводить к избыточной гибели не только гепатоцитов, но и других клеточных популяций, отражая либо системный иммуновоспалительный ответ на инфекцию, либо внепеченочную персистенцию вируса. В связи с этим определенный интерес представляют наши исследования апоптоза периферических лейкоцитов при хроническом гепатите. У больных хроническими гепатитами В и С и у здоровых доноров определялось количество лимфоцитов и гранулоцитов периферической крови в состоянии апоптоза непосредственно после выделения и после 24-часовой инкубации в культуральной среде методом проточной цитофлюориметрии, а также повреждение ДНК по скорости щелочной денатурации. Даннные исследования показали, что апоптоз как лимфоцитов, так и гранулоцитов был достоверно выше у больных ХГВ по сравнению с контролем как непосредственно после выделения, так и после суточной инкубации. Более интенсивный переход клеток в апоптоз наблюдался в подгруппе больных гепатитом С, хотя здесь следует учитывать роль разного количества пациентов в подгруппах (12с гепатитом В, 22 с гепатитом С). Выявлена также корреляция между степенью повреждения ДНК лимфоцитов и гранулоцитов и накоплением клеток в состоянии апоптоза после инкубации [3]. Помимо этого, после суточной инкубации количество лейкоцитов обеих популяций в апоптозе достоверно коррелировало с сывдроточной концентрацией TNF-α [4].
Полученные результаты свидетельствуют об усилении программированной гибели клеток периферической крови у больных хроническим вирусным гепатитом, что может отражать как повреждающее действие гепатотропных вирусов на лейкоциты (или их костномозговые предшественники), так и влияние системного действия провоспалительных цитокинов. Косвенным подтверждением последнего механизма служит корреляция интенсивности апоптоза с сывороточным уровнем TNF-α - наиболее мощного цитокина с проапоптогенным эффектом.
Литература
1. Аббасова С.Г., Липкин В.М., Трапезников Н.Н., Кушлинский Н.Е. Система FAS - FASL в норме и патологии // Вопр. биол., мед., фарм. химии. - 1999. - №3.-С.3-17.
2. Аруин Л.И. Апоптоз и патология печени // Росс. ж. гастроэнтерол., гепатол., колопроктол. - 1998. - №2. - С. 6-10.
3. Буеверов А.О., Тихонина Е.В., Москалева Е.Ю. и др. Апоптоз периферических лейкоцитов при хронических вирусных гепатитах // Росс. ж. гастроэнтерол., гепатол., колопроктол. - 2000. - №6. - С. 30-33.
4. Boueverov A.O., Mammaev S.N., Tikhonina E.V. et al. Enchanced apoptosis of peripheral blood leucocytes in chronic viral hepatitis // Gut. - 2000. - Vol.47 (suppl. 3). - A 181.
5. Faubion W.A., Gores G.J. Death receptors in liver biology and pathobiology // Hepatology. - 1999. - Vol.29. - P. 1-4.
6. Hayashi N., Mita E. Fas system and apoptosis in viral hepatitis//J. Gastroenterol. Hepatol. - 1997.-Vol.l2. - S.223-226.
7. Jonsson J.R., Edwards-Smith C.J., Catania S.C. et al. Expression of cytokines and factors modulating apoptosis by human sinusoidal leucocytes // J. Hepatol. - 2000. - Vol.32. -P.392-398.
8. Krams S.M., Fox S.K., Beatty P.R. et al. Human hepatocytes produce an isoform of FAS that inhibits apoptosis // Transplantation. - 1998. - Vol.65. - P.713-721.
9. Okazaki M., Hino K., Fujii К et al. Hepatic Fas-antigen expression before and after interferon therapy in patients with chronic hepatitis С // Dig. Dis. Sci. - 1996. - Vol.41. - P.2453-2458.
10. Su F, Schneider R.J. Hepatitis В virus HBx protein sensitizes cells to apoptotic killing by tumor necrosis factor alpha // Proc. Nat. Acad. Sci. USA. - 1997. - Vol.94. - P.8744-9.
| Март 2003 г. |