Опубликовано в журнале:
«ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ», 2009, №11; Вып. 2, с. 70-77Изменения ЭЭГ в процессе лечения эпилепсии леветирацетамом (Кеппра)
Д.м.н., проф. Л.Р. Зенков
Клиника нервных болезней им. А.Я. Кожевникова; Лаборатория клинико-электрофизиологических исследований Московской медицинской академии им. И.М. СеченоваEEG changes during the treatment of epilepsy with levetiracetam (Keppra)
L.R. Zenkov
Обследовали 43 больных эпилепсией в возрасте от 1 года до 43 лет (средний возраст 21,19±1,67 года) с разными формами эпилепсии и типами припадков. Кеппрой в режиме монотерапии лечились 15 пациентов, 28 — в комбинации с другими препаратами. Начальная доза кеппры назначалась в соответствии с массой тела и возрастом больных, а также с учетом частоты и тяжести приступов, составляя в среднем 988,4±58,2 мг в сутки; финальная доза составляла в среднем 1625±298,7 мг в сутки. Проводили запись ЭЭГ до и в процессе терапии и ее анализ ручным и компьютерным методами с вычислением соответствующих статистических показателей. Получили достоверные данные о высокой клинической эффективности кеппры: среднее снижение частоты припадков — на 69,6%; число больных с терапевтической ремиссией — 56%; высокий процент респондеров (67,7) и ремиссий (54,8) в группе ранее резистентных к терапии больных. Леветирацитам оказывал выраженное подавляющее действие на эпилептиформную и другие виды патологической активности на ЭЭГ.
Ключевые слова: эпилепсия, лечение, леветирацетам (кеппра), ЭЭГ.
Forty-three patients with epilepsy, aged from 1 to 43 years (mean age 21,19 years) with different forms of epilepsy and types of seizures were studied. Fifteen patients received keppra as a monotherapy and 28 — in combination with other drugs. The initial prescription dose of keppra (988,4±58,2 mg/day) was based on the patient’s age and body mass as well as on the frequency and severity of seizures. The final dose was 1625±298,7 mg/day. EEG was recorded before and during the therapy. Its analysis was performed using manual and computer methods with calculating correspondent statistics. The results revealed the high clinical effectiveness of keppra: the average reduction of seizures by 69,6% and the number of patients with therapeutic remission — by 56%, high percentage of responders (67,7%) and remissions (54,8%) in the group of previously drug-resistant patients. Levetiracetam had a marked inhibiting effect on epileptic and other types of pathological EEG activities.
Key words: epilepsy, treatment, levetiracetam (keppra), EEG.
Леветирацетам (кеппра) является одним из наиболее широко применяемых новых препаратов при лечении эпилепсии. Он позиционируется как препарат первого выбора для большинства форм эпилепсий и эпилептических синдромов [5, 6]. Эффективность лечения зависит от правильного подбора дозы в пределах терапевтического диапазона, представляющего собой интервал между минимальной обеспечивающей лечебный эффект, и максимальной переносимой, без токсических побочных явлений. Леветирацетам имеет в этом отношении благоприятные характеристики: рекомендуемые дозы (включая детей младшего возраста) варьируют от 20 до 60 мг/кг в сут. В ряде публикаций сообщается о безопасном применении дозировок до 313 мг/кг в сутки у детей и суммарных доз до 6000 мг/кг в сутки и более у взрослых [8, 13]. Однако эта же особенность леветирацетама создает трудности в первоначальном подборе эффективной дозы и ее коррекции в ходе лечения в зависимости от течения заболевания. Широкий интервал терапевтических концентраций леветирацетама, представляющий несомненные клинические преимущества, делает измерение его уровня в плазме для целей подбора дозы мало полезным [1, 14]. Наиболее обоснованными являются электроэнцефалографические данные, учитывая непосредственную патофизиологическую связь эпилептического процесса с эпилептической активностью нейронов мозга. На этом пути лежат трудности, связанные с не зависящим от противосудорожного эффекта влиянием препаратов на ЭЭГ. К примеру, применение карбамазепина может сопровождаться усилением эпилептиформной активности, иногда в противоречие к клиническому улучшению [14]. В эксперименте показано, что леветирацетам подавляет эпилептиформную активность более эффективно, чем вальпроаты и этосуксимид [4]. Достаточно полных клинических исследований влияния леветрацетама на ЭЭГ, охватывающих разные формы эпилепсии, нет. В настоящем проспективном прагматическом открытом исследовании изучалось влияние леветирацетама на электроэнцефалограмму в ходе подбора терапевтической дозы препарата.
Целью исследования было определение принципов контроля эффективности лечения эпилепсии леветирацетамом на основе данных электроэнцефалографии.
Материал и методы
Наблюдали 43 больных эпилепсией [19 мужчин и 24 женщины, в возрасте от 1 года до 43 лет (средний возраст 21,19±1,67 года)]. Длительность наблюдения была 6—48 мес (средняя 23,58±1,38 мес); у 95% она превышала 1 год.
В 31 случае обращение больных за помощью было связано с резистентностью к предыдущему лечению. До назначения кеппры 20 пациентов получали политерапию карбамазепином, фенобарбиталом, вальпроатами, фенитоином, ламотриджином, топираматом, окскарбазепином, этосуксимидом, клоназепамом (от 2 до 4 препаратов) в разных комбинациях. Наиболее часто предшествующая терапия проводилась карбамазепином (21 наблюдение) и вальпроатами (21).
В числе наблюдавшихся пациентов были 15 больных с симптоматической фокальной эпилепсией, 16 — с криптогенной фокальной эпилепсией, 2 — с идиопатической фокальной эпилепсией, 2 — с юношеской эпилепсией с абсансами и генерализованными тонико-клоническими припадками, 2 — с детской эпилепсией с абсансами, 4 — с юношеской миоклонической эпилепсией, 2 — с тяжелыми эпилептическими энцефалопатиями детского возраста (1 больной с синдромом Уэста и 1 — с синдромом Леннокса—Гасто). По типам припадков у 4 больных были типичные абсансы, у 4 — миоклонические генерализованные припадки, у 2 — первично-генерализованные тонико-клонические припадки, у 2 — эпилептические спазмы, у 16 — простые фокальные припадки, у 26 — комплексные парциальные и у 29 — вторично-генерализованные тонико-клонические припадки. У большинства пациентов с фокальными эпилепсиями припадки разных типов комбинировались.
Стартовая доза кеппры назначалась и титровалась соответственно массе тела и возрасту, а также с учетом частоты и тяжести приступов и составляла 500—2000 мг/сут (в среднем 988,4±58,211 мг/сут; 31 пациенту проведено дальнейшее увеличение дозы по поводу возникновения припадка на начальной дозе или при обнаружении эпилептиформной активности при первом контрольном исследовании ЭЭГ, которое проводилось при следующем посещении врача в интервале 0,5—12 нед от дня достижения начальной целевой дозы. Скорректированные дозы, на которых проводилась финальная оценка влияния лечения кеппрой на ЭЭГ всем 43 пациентам, составляли 500—4000 мг/сут (в среднем 1625,0±298,7 мг/сут).
Здесь и далее разброс представлен средней ошибкой (М±m).В режиме монотерапии 15 пациентов получали кеппру (12 в качестве начального лечения, 3 переведены на монотерапию с предшествовавших препаратов); 28 получали кеппру в комбинации с другими препаратами (12 — ламотриджин, 8 — вальпроаты, 7 — карбамазепин, 1 — топирамат, 1 — окскарбазепин), в 25 случаях в дуотерапии, в 3 — в тритерапии. Во всех случаях кеппра присоединялась к принимавшемуся ранее препарату.
Регистрацию ЭЭГ проводили на электроэнцефалографе Нейро КМ фирмы «Статокин» (Москва), оснащенном программным комплексом полной статистической обработки непосредственно регистрируемых ЭЭГ и представления индивидуальных и статистических параметров и данных в виде карт распределения по скальпу Брейн—Сис (разработчик А.А. Митрофанов). У всех пациентов проводили ручной анализ «сырой» ЭЭГ и оценку мощности основных спектральных полос активности. Записывали не менее 10 мин фоновой активности, 1—3 мин гипервентиляции в зависимости от очевидности эпилептиформной активности в ЭЭГ, не менее 2 мин после гипервентиляции от 16 отведений по системе 10/20.
При ручном анализе ЭЭГ количественную оценку выраженности эпилептиформной активности проводили по ранее использованной в аналогичных исследованиях с карбамазепином и вальпроатом методике [14]. За все время записи ЭЭГ по экрану монитора определяли в пересчете на 1 мин записи количество следующих графоэлементов в ЭЭГ: паттернов эпилептического припадка, разрядов эпилептиформной активности, комплексов спайк-волна, спайков, билатерально синхронных вспышек α, τ-, δ-волн, фокальных патологических феноменов. Каждому из феноменов присваивался в соответствии с его диагностической значимостью определенный диагностический вес — наибольший, равный 32, соответствовал паттерну эпилептического припадка в ЭЭГ, наименьший — 1 — фокальным нарушениям независимо от их типа (таблица). Этот вес умножался на количество данных феноменов в мин. Сумма этих произведений составляла индекс эпилептической активности (ИЭА) соответственно формуле:
ИЭА = ∑ N P/T (мин),
где, N — число феноменов за все время записи, P — диагностический вес данного феномена, T — время записи в мин.
Диагностический вес графоэлементов и паттернов в ЭЭГ
ЭЭГ феномен, или графоэлемент Диагностический вес Паттерн эпилептического припадка 32 Разряд эпилептиформной активности 16 Спайк-волна 8 Острая волна, спайк 4 Билатерально-синхронные вспышки
α-, δ-, θ-активности2 Фокальные изменения 1 При компьютерном анализе ЭЭГ анализировали 3 мин фоновой записи после предварительного удаления артефактов вручную. С помощью быстрого преобразования Фурье определяли суммарную спектральную мощность и мощность в полосе α (8— 13 Гц), β (13—30 Гц), δ (0,5—4 Гц), θ (4—8 Гц). Для аппроксимации к нормальному распределению цифровые значения мощности преобразовывали в их натуральные логарифмы — ln (Power).
Статистический анализ. Исходя из показанного ранее факта высокой спектральной мощности по всем диапазонам у больных эпилепсией и уменьшения ее под влиянием лечения [14], в предположении наличия связи между клиническим улучшением под влиянием леветирацетама и уменьшением выраженности эпилептических изменений в ЭЭГ, проверялась гипотеза об уменьшении выраженности ИЭА в результатах ручного анализа и об уменьшении логарифма спектральной мощности в данных компьютерного анализа под влиянием терапевтических доз леветирацетама.
Результаты ручного анализа ЭЭГ обрабатывали с помощью пакета программ Биостатистика — Windows. Для оценки влияния леветирацетама на ИЭА использовали программу сравнения сопряженных данных для пар наблюдений (до начала лечения леветирацетамом и на терапевтических дозах леветирацетама), а также программу для оценки коэффициента корреляции между изменениями ИЭА и частоты припадков в месяц. Кроме того, с целью возможного выявления фактора предсказания резистентности к леветирацетаму проводили сравнение средних ИЭА в группе, достигшей ремиссии, и в группе, в которой не удалось достичь прекращения припадков до лечения леветирацетамом, на начальной дозе и на конечной стабилизированной дозе препарата.
Данные спектрального анализа ЭЭГ далее обрабатывали с помощью пакета программ, входящих в программное обеспечение электроэнцефалографа Нейро КМ.
Статистическая значимость оценивалась как разность (1–p) со знаком (p — вероятность ошибки гипотезы по t-критерию Стьюдента). Знак « – » означал уменьшение мощности ЭЭГ в результате лечения, а модуль при знаке — значимость этого уменьшения, причем величины модуля ≥0,95 соответствовали статистической значимости этого уменьшения. Динамику изменений логарифма мощности по основным отведениям ЭЭГ отображали на картах поверхности головы. К примеру, значение для отведения Fp2=–0,995 означает, что мощность в этом отведении ЭЭГ под влиянием леветирацетама высоко значима (p=0,005) уменьшилась.
Сравнивали групповые средние логарифма мощности ЭЭГ до лечения и на фоне стабилизированной терапевтической дозы леветирацетама с оценкой знака и достоверности различий: 1) по всей группе, 2) у пациентов на монотерапии, 3) у пациентов на политерапии, 4) у респондеров (уменьшение числа припадков ≥67%), 5) у резистентных к кеппре пациентов.
Результаты
До начала лечения частота припадков у обследованных больных варьировала от 1—3 до 600 в мес (в среднем 60,24±17,42 припадков в мес). Высокая средняя частота припадков была обусловлена наличием в группе 6 пациентов с начальной частотой припадков 125—600 в мес, в том числе с синдромом Леннокса—Гасто, синдромом инфантильных спазмов, псевдосиндромом Леннокса—Гасто, абсансной эпилепсией детского возраста, симптоматической височно-долевой эпилепсией с частыми — до 20 в день — комплексными фокальными припадками.
В период, когда использовалась конечная стабильная доза кеппры, средняя частота припадков по группе статистически значимо (p<0,02) уменьшилась до 18,28±8,08. Среднее снижение частоты припадков по группе — 69,6%. Не было значимого различия по снижению частоты припадков между пациентами на моно- и политерапии кеппрой. Учитывая, что в прагматических исследованиях критерий 50% снижения припадков, не удовлетворяющий ни пациента, ни врача, подвергается справедливой критике [11], мы в качестве показателя эффективности препарата выбрали критерий снижения числа припадков не менее чем на 2/3 (≥67%) и соответствующие пациенты обозначались как респондеры. Число их составило 31. Ремиссии ≥6 мес на момент последнего наблюдения удалось достичь у 23 (56%) пациентов. Количество ремиссий на монотерапии было больше — у 11 (73,3%) из 15 пациентов, чем на политерапии — у 12 (43%) из 28. Из пациентов, резистентных к предшествовавшей терапии, респондерами оказались 21 (67,7%) из 35 пациентов, причем у 17 (54,8%) из 31 была достигнута ремиссия.
Средние стабилизированные дозы леветирацетама составляли на начальном этапе у респондеров 1000±70,9 мг в сутки, на заключительном — 1617,0±165,6 мг в сут. У больных с резистентными к леветирацетаму припадками соответствующие дозы составляли 954,5±125,3 и 1818,0±101,6 мг в сутки соответственно и не отличались значимо от доз у респондеров.
Средняя частота припадков в 1 мес у респондеров и оказавшихся резистентными к кеппре до начала лечения статистически значимо не различалась и составляла 57,07±22,97 и 73,58±28,08 соответственно (p=0,689). На начальной стабилизированной дозе кеппры у респондеров достоверно уменьшилось количество припадков в 1 мес до 5,67±2,23 (p=0,03), у резистентных количество припадков в 1 мес составило 68,27±22,97 и не отличалось значимо от исходной частоты. На окончательной стабилизированной дозе кеппры у респондеров количество припадков в 1 мес уменьшилось до 1,9±1,44, у резистентных оно составило 70,36±28,35 и практически не отличалось от частоты припадков на предыдущей дозе.
Данные ручного анализа ЭЭГ. До лечения у всех пациентов отмечались те или иные патологические изменения в ЭЭГ, варьировавшие от умеренных признаков снижения порога судорожной готовности до грубой эпилептиформной активности. У 12 пациентов ЭЭГ была грубо изменена по эпилептическому типу с генерализованными и фокальными разрядами эпилептиформной активности, паттернами эпилептического припадка, гисаритмии и эпилептического статуса с соответствующим клиническим сопровождением.
Средний ИЭА до лечения по всей группе составил 87,8±17,9, на конечной стабилизированной дозе он статистически значимо уменьшился до 42,41±11,6 (p=0,002). В группе 29 пациентов, которым проводилось 3 исследования, получены следующие значения ИЭА: до лечения кеппрой — 100,3±25,06, на начальной дозе — 37,45±14,59 и на конечной дозе — 26,46±9,24. Разница между исходными значениями ИЭА и значениями на терапии кеппрой высоко статистически значима: p<0,001 и p=0,003 соответственно для первой и для второй дозы.
Выраженная эпилептиформная активность сохранялась у всех 11 пациентов с резистентностью к кеппре. У них значимых различий между ИЭА до лечения и на обеих дозах кеппры не выявлено: до лечения кеппрой — 85,09±21,52, на начальной дозе — 91,64±26,46 и на конечной дозе — 126,06±60,31.
До лечения кеппрой не было значимых различий между ИЭА резистентных к ней пациентов (85,09±21,52) и ИЭА респондеров (90,35±23,77). У респондеров уже на начальной дозе кеппры отмечалось статистически высоко значимое уменьшение ИЭА до 26,16±11,82 (p<0,001). На конечной дозе кеппры отмечалось дальнейшее статистически не значимое снижение ИЭА до 11,87±2,41 (p=0,20). Различия между респондерами и резистентными на начальной и конечной дозах кеппры были высоко статистически значимы: p=0,013 и p=0,002 соответственно (рис. 1).
Рис. 1. Динамика ИЭА в ходе титрования дозы леветирацетама (ЛЕВ) у респондеров и резистентных пациентов: статистически значимое снижение ИЭА у респондеров уже на начальной дозе и незначимое статистически увеличение ИЭА в случаях, резистентных к леветирацетаму.

Наконец, сравнение ИЭА у пациентов на монотерапии и политерапии показало совпадение общей динамики: индексы уменьшились на конечной дозе соответственно на 76,28±34,54 (p=0,041) и 44,25±16,86 (p=0,015).
Корреляционный анализ отношения изменения ИЭА к динамике частоты припадков при лечении кеппрой выявил достоверную положительную корреляцию (r=0,595, p<0,00001).
Данные компьютерного анализа ЭЭГ показали следующее. Сравнение групповых средних по всем 43 пациентам выявило, что уже на начальных дозах кеппры логарифм спектральной мощности во всем диапазоне от 0,5 до 30 Гц статистически значимо уменьшился (1–p <–0,95) по всем отведениям. Также статистически значимо уменьшился логарифм мощности патологических диапазонов δ (1–p <–0,98—0,99) и θ-активности по всем отведениям (1–p<–0,95—0,99). Статистически значимо уменьшился логарифм мощности β-активности (13—20 Гц), отражающий активность спайков и острых волн, в отведениях F8, T3, C3, P3 и P4.
На монотерапии кеппрой статистически значимое уменьшение мощности (1–p<–0,95—0,99) наблюдалось как во всей полосе частот, так и в отдельных диапазонах δ, θ, α и β по всем отведениям, за исключением дельта в отведениях T3 и T6,α в C3, C4, T4, T6, P4, O1 и β в отведениях O1 и O2.
При политерапии кеппрой статистически значимое уменьшение мощности (1–p <–0,95—0,99) наблюдалось во всей полосе частот по всем отведениям, кроме затылочных и правовисочных, в диапазоне δ во всех отведениях, θ — во всех отведениях, кроме правого затылочного, в диапазонах α и β — только в отведениях T3, T5, P3 и P4.
При исследовании спектральной мощности у респондеров уже на начальных дозах кеппры отмечалось статистически значимое уменьшение логарифма мощности по всей полосе 0,5—30 Гц (1–p <–0,97—0,99), патологической d (1–p <–0,99) и t-активности (1–p <–0,96—0,99) по всем отведениям, статистически значимое уменьшение α-актив-ности (1–p <–0,97—0,99) в отведениях F7, F8, T3, T6, и β-активности в диапазоне 13—20 Гц (1–p <–0,95—0,99) в отведениях F8, T3, C3, P3, P4 .
В отличие от респондеров исследование пациентов с резистентностью к леветирацетаму не выявило уменьшения спектральной мощности ни по всей полосе 0,5—30 Гц, ни по отдельным диапазонам, ни на начальной дозе, ни при дальнейшем ее увеличении, что соответствовало отсутствию у них значимого уменьшения эпилептиформной активности при ручном обсчете.
Обсуждение
Прежде всего следует отметить высокую клиническую эффективность леветирацетама. Среднее снижение частоты припадков по группе составило 69,6%, причем одинаково значительное улучшение получено как при моно-, так и при политерапии кеппрой. Обращает внимание большое количество (56%) пациентов с достигнутой ремиссией. Большее количество ремиссий на монотерапии (73,3%), чем на политерапии (43%) объясняется тем, что на политерапии оказывались пациенты с наиболее резистентными формами эпилепсии. Очень показателен высокий процент респондеров (67,7), и ремиссии (54,8%) при терапии кеппрой у больных, резистентных к ранее проводимой терапии, причем большинство из них (64,5%) до этого получали 2 и более противоэпилептических препарата в моно- и/или политерапии. Известно, что частота ремиссии на втором препарате при неэффективности первого оценивается в 10—20%, а при неэффективности второго только в 0—9% [3, 7, 9, 10].
Таким образом, леветирацетам по этим показателям занимает совершенно выдающееся положение — 54,8% ремиссии у пациентов, резистентных к предшествовавшей терапии.
Данные оценки ИЭА при ручном анализе показывают, что лечение леветирацетамом приводит к нормализации ЭЭГ, причем клиническая успешность лечения достоверно коррелирует с уменьшением не только эпилептиформной, но и других видов патологической активности в ЭЭГ. Важно отметить, что улучшение параметров ЭЭГ возникает скачкообразно уже на начальном этапе подбора дозы препарата. Подчеркнем, что при исходном отсутствии различий между резистентными пациентами и респондерами уже на начальных дозах выявляется достоверное различие между пациентами с хорошим клиническим прогнозом и пациентами, которые в дальнейшем окажутся резистентными к ле-ветирацетаму. У последних значительного уменьшения эпилептиформной активности и другой патологической активности в ЭЭГ не происходит. Это позволяет использовать ИЭА в ЭЭГ на начальной дозе леветирацетама как предиктор резистентности или хорошего прогноза и избежать бесполезного наращивания доз препарата в неуспешных попытках улучшить состояние больного в тех случаях, когда уменьшение эпилептиформной активности на начальных дозах не происходит. Высоко достоверная положительная корреляция между уменьшением ИЭА и снижением частоты припадков при лечении кеппрой делает ЭЭГ-контроль удобным показателем для подбора эффективной и одновременно неизбыточной дозы препарата на самом раннем этапе лечения, не дожидаясь «контрольного» припадка, что важно в случаях нечастых припадков. Следует отметить, что нормализация ЭЭГ в равной мере наблюдалась у больных при моно- и политерапии. Большие абсолютные значения снижения ИЭА при монотерапии объясняются тем, что в группу пациентов с политерапией вошли 7 и 11 пациентов с резистентностью к кеппре, которые, как показано выше, не дали снижения ИЭА при лечении этим препаратом.
Данные компьютерного анализа полностью соответствуют результатам ручного анализа как по всей группе, так и отдельно при политерапии и монотерапии кеппрой. Уменьшение как общей мощности ЭЭГ, так и отдельных ее полос по всем или большинству отведений свидетельствует о снижении амплитуды как острых, так и медленных патологических компонентов в ЭЭГ, характерных для активного эпилептического процесса, т.е. об общей синхронизации. Особый интерес представляет особенность динамики α- и β-активности, статистически значимое уменьшение мощности которых наблюдалось, главным образом, в передних отведениях, что отражает уменьшение острых волн и спайков в «сырой» ЭЭГ. Отсутствие значимых изменений α-и β-активности в задних отведениях является следствием двух противоположно направленных ее изменений под влиянием лечения. При успешном лечении эпилепсии уменьшение эпилептиформной активности сочетается с восстановлением доминирующих нормальных α- и β-ритмов в соответствующих отделах мозга [14]. Таким образом, мощность этих двух полос в ЭЭГ определяется, с одной стороны, подавлением спайковой и островолновой эпилептиформной активности в диапазоне α и β, с другой — восстановлением под влиянием леветирацетама нормальной α- и β-активности вследствие высвобождения нейронов в результате прекращения патологической активности. В результате суммарный логарифм мощности по группе статистически значимо не меняется, в отличие от патологических форм активности, которые снижаются под действием леветирацетама. Подавление эпилептиформной активности, очевидно, лежит в основе психической реабилитации больных при лечении леветирацетамом. Занятость нейронов эпилептической активностью нарушает возможность их включения в адаптивные информационные процессы, а их высвобождение под влиянием лечения способствует восстановлению нормального психического и социального функционирования [1, 2, 14]. Эффективное подавление эпилептиформной активности подтверждает перспективность применения кеппры в лечении эпилептических энцефалопатий, включая «катастрофические», при которых постоянная грубая эпилептиформная активность ведет к психомоторной деградации пациента [2, 12, 14]. В настоящем исследовании лечение кеппрой 2 пациентов с синдромом Уэста и с синдромом Леннокса—Гасто, как продолжения синдрома Уэста, позволило получить не только прекращение припадков, но и значительное улучшение моторных и психических функций (рис. 2).
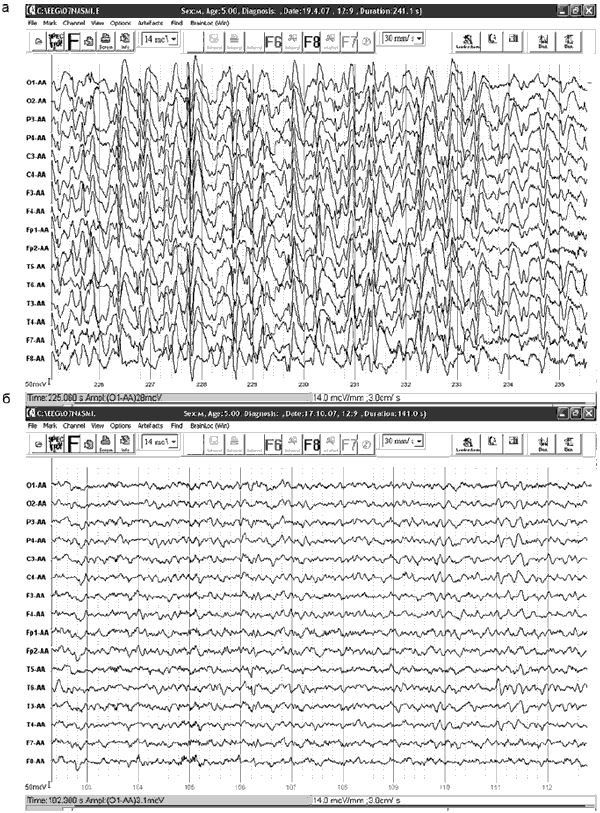
Рис. 2. ЭЭГ мальчика 5 лет с синдромом Леннокса—Гасто как продолжения некурабельного синдрома инфантильных спазмов.
а: ЭЭГ на политерапии: вальпроаты 750 мг в сутки + ламотриджин 125 мг в сутки + топирамат 100 мг в сутки + клоназепам 2 мг в сутки. Постоянная гипсаритмия; 600 мг в сутки эпилептических спазмов в день, 2—10 атипичных абсансов в день, 1—5 тонических припадков каждую ночь, 5—8 генерализованных тонико-клонических припадков ежемесячно. Непрерывное состояние бессудорожного эпилептического статуса атипичных абсансов в период записи ЭЭГ, астазия, абазия, алалия, апраксия, отсутствие контакта. б: ЭЭГ при терапии леветирацетамом 1000 мг в сутки + ламотриджин 75 мг в сутки. Полное прекращение эпилептиформной и восстановление нормальной по возрасту активности. Припадков нет 6 мес. Самостоятельно встает, ходит с поддержкой, владеет речью в пределах домашнего обихода, используя короткие фразы, называет все буквы печатного текста. Сознательно оперирует предметами обихода и игрушками, адекватный эмоциональный контакт.
Аналогично данным ручного анализа, данные спектрального анализа выявили статистически значимое различие динамики спектральной мощности в процессе лечения между респондерами и резистентными пациентами. У пациентов с резистентностью не отмечалось значимого уменьшения логарифма мощности в процессе лечения, в то время как у респондеров наблюдалось высоко достоверное его снижение по большинству отведений как в общей полосе, так и в диапазоне патологической и эпилептиформной активности. Эти данные позволяют использовать компьютерный анализ для отслеживания динамики изменений ЭЭГ под влиянием терапии, а также для предикции возможной резистентности.
При лечении эпилепсии помимо прекращения припадков преследуется не менее важная стратегическая задача подавления субклинических эпилептических разрядов в мозге, которые не только являются непосредственной причиной поведенческих и психических интериктальных расстройств, но и способствуют по механизму киндлинга поддержанию и распространению эпилептического процесса в мозге [1, 2]. Поэтому оптимальным подходом является подбор такой индивидуальной дозы препарата, которая не только прекращает припадки, но и нормализует работу мозга. Идеальным решением представляется отслеживание влияния препарата на эпилептический процесс и подбор его дозы нейрофизиологическими методами, поскольку эпилептические разряды нейронов являются не только непосредственной причиной припадков и многих интериктальных проявлений, но и механизмом развития эпилептического процесса [2, 14]. Результаты настоящего исследования дают основание считать, что кеппра является препаратом, в отношении которого использование электроэнцефалографических критериев позволяет оптимизировать лечение, индивидуально подбирая минимальную и при этом достаточно эффективную дозу препарата. Для оценки эффекта препарата можно воспользоваться как методом традиционного ручного анализа, сравнивая ЭЭГ до лечения и в процессе подбора дозы, так и автоматического, оценивая количественно значимость изменения спектральной мощности в ЭЭГ. Процесс индивидуального подбора дозы препарата может выглядеть следующим образом. 1) Перед началом лечения регистрируется цифровая ЭЭГ. 2) Через 2—6 дней (учитывая быстрое достижение стабильной концентрации в крови, характерное для кеппры) приема минимальной рекомендуемой дозы для данного возраста регистрируется ЭЭГ и проводится визуальное и компьютерное сравнение ее по ИЭА и/или спектральной мощности, выраженной в ln (Power), с предыдущей. Уменьшение ИЭА и мощности по большинству отведений и спектральных полос со значимостью ≥95% по критерию t Стьюдента свидетельствует о правильности выбора препарата. 3) При сохранении в ЭЭГ остаточной эпилептиформной активности суточная доза увеличивается на 250 мг и через 2—6 дней приема повторяется та же процедура оценки ЭЭГ. Процедура может повторяться до тех пор, пока данные анализа ЭЭГ не нормализуются или стабилизируются. Обычно достаточно 1—3 оценок ЭЭГ на фоне лечения для первоначального подбора дозы. После стабилизации параметров ЭЭГ целесообразно повторить через несколько недель процедуру оценки ЭЭГ и, если данные не изменились, возможно уменьшение дозы леветирацетама до предшествующего уровня также под контролем ЭЭГ. Как видно из описания методики исследования, именно этот алгоритм применялся к пациентам в обследованной группе. Средние дозы леветирацетама соответствуют нижней границе ориентировочных рекомендуемых доз, что свидетельствует о целесообразности данного подхода, позволяющего вести пациента на минимальной и вместе с тем эффективной дозе, удовлетворяя одновременно 2 основным требованиям лечения: оптимальным отношениям эффективность/безопасность и эффективность/стоимость.
Изложенное выше дает основание сделать следующие выводы. Леветирацетам — высокоэффективный препарат в лечении эпилепсии как в отношении подавления припадков, так и в нормализации когнитивных и психических нарушений при использовании режима моно- и политерапии. Этот препарат подавляет эпилептиформную и другие виды патологической активности на ЭЭГ. Изменения ЭЭГ на начальной дозе леветирацетама являются предиктором успеха терапии или возможной резистентности. Значимая положительная корреляция между изменениями ЭЭГ и частотой припадков позволяет по динамике ЭЭГ подобрать эффективную дозу. Подавление эпилептиформной активности и восстановление нормальной активности способствует психической, эмоциональной и поведенческой реабилитации больных.
ЛИТЕРАТУРА
1. Зенков Л.Р. Клиническая эпилептология (с элементами нейрофизиологии). М: МИА 2001.
2. Зенков Л.Р. Непароксизмальные эпилептические расстройства. М: МЕДпресс-информ 2007.
3. Arts W.F.M., Brouwer O. F., Peters A. C. B. et al. Course and prognosis of childhood epilepsy: 5-year follow-up of the Dutch study of epilepsy in childhood. Brain 2004;127:8:1774—1784.
4. Bouwman B.M., van Rijn C.M. Effects of levetiracetam on spike and wave discharges in WAG/Rij rats. Seizure 2004;13:591—594.
5. Drugs for Epilepsy. Treatment guidelines. Med Letter 2008;6:70:37—50.
6. Glauser T., Ben-Menachem E., Bourgtois B. et al. ILAE treatment guidelines: evidence-based analysis of antiepileptic drug efficacy and effectiveness as initial monotherapy for epileptic seizures and syndromes. Epilepsia 2006;47:1094—1120.
7. Kelso Andrew R.C., Cock Hannah R. Advances in epilepsy. Br Med Bull 2005;72:135—148.
8. Koukkari M.W., Guarino E.J. Retrospective study of the use of levetiracetam in childhood seizure disorders. J Child Neurol 2004;19:944—947.
9. Kwan P., Brodie M.J. Early identification of refractory epilepsy. N Engl J Med год? ;342:314—319.
10. Löscher W. , Potschka H. Natural history of treated childhood-onset epilepsy: prospective, long-term population-based study. J Pharmacol Exp Ther 2002;301:7—14.
11 . Marson A.G., Chadwick D.W. New dr ug treatm ents for epilep sy. J Neurol Neurosurg Psychiat 2001;70:143—147.
12. Mintz M., LeGoff D., Scornaienchi J. et al. The Underrecognized Epilepsy Spectrum: The Effects of Levetiracetam on Neuropsychological Functioning in Relation to Subclinical Spike Production. J Child Neurol 2009;24:807—815.
13. Rossetti A.O., Bromfield E.B. Determinants of success in the use of oral leve-tiracetam in status epilepticus. Epilepsy Behav 2006;8:3:651—654.
14. Zenkov L.R. Znaczenie zapisu eeg w leczeniu padaczki kwasem walproinow-ym i karbamazepiną. Epileptologia 2003;11:339—354.
| Ноябрь 2013 г. |