Опубликовано в журнале:
Клинические перспективы гастроэнтерологии, гепатологии № 5, 2006
Современные принципы ведения пациентов с хронической инфекцией вирусом гепатита В: клиническое значение уровня вирусной нагрузки
В.Т. Ивашкин, М.В. Маевская (Московская медицинская академия им. И.М. Сеченова, Москва)
Алгоритм ведения пациентов с HBV-инфекцией в клинической практике разработан на согласительной конференции Европейского общества по изучению печени в 2002 г. и Американской ассоциацией по изучению печени в 2001 г. В 2004 г. в США советом экспертов в этой области обновлены рекомендации практическим врачам. Тем не менее к настоящему времени появились новые достижения в изучении этой проблемы. Они обсуждались на совещании Рабочей группы Национального института здоровья США, одним из аспектов деятельности которой стало совершенствование методов ведения пациентов с HBV-инфекцией.
Ключевые слова: хронический гепатит В, цирроз печени, гепатоцеллюлярная карцинома, вирусная нагрузка, противовирусное лечение.
Modern principles of management of patient with chronic hepatitis B virus infection: Clinical value of the viral load level
V.T. Ivashkin, M.V. Mayevskaya
The algorithm of management of patient with HBV-infection in clinical practice has been developed at consensus conference of the European society on study of liver in 2002 and the American association on study of liver in 2001. On 2004 in USA guidelines to practical doctors were re-established by the council of experts. Nevertheless, new advances in studying of this problem have appeared by present time, which were discussed at the meeting of working group of USA National institute of health. Improvement of patient with HBV-infection management methods became one of the aspects of its activity.
Keywords: chronic hepatitis B, liver cirrhosis, hepatocellular carcinoma, viral load, antiviral therapy.
Инфекция вирусом гепатита В (HBV) представляет собой одну из актуальных проблем здравоохранения во всем мире, поскольку более чем 350 млн. человек являются ее хроническими носителями. В отсутствие лечения приблизительно у 20% больных формируется цирроз печени (ЦП) с последующим развитием его осложнений. Еще у 20% пациентов с компенсированным ЦП в последующие 5 лет развивается декомпенсация болезни [4].
Противовирусное лечение может изменить естественное течение инфекции и уменьшить риск развития ЦП, декомпенсации заболевания и гепатоцеллюлярной карциномы (ГЦК).
Алгоритм ведения пациентов с HBV-инфекцией в клинической практике разработан на согласительной конференции Европейского общества по изучению печени в 2002 г. [3] и Американской ассоциацией по изучению печени в 2001 г. [7]. В 2004 г. в США советом экспертов в этой области были обновлены рекомендации практическим врачам [6].
Тем не менее появились новые достижения в изучении указанной проблемы: FDA (Food and Drag Administration) одобрено два новых антивирусных препарата для лечения хронического гепатита В (ХГ В) - и пегинтерферон а-2а, получены новые данные о значении вирусной нагрузки в течении болезни, улучшены тесты для диагностики этой инфекции.
Достигнутый клинический прогресс явился основанием для прошедшего в апреле 2006 г. совещания Рабочей группы Национального института здоровья США. Одним из аспектов ее деятельности стало совершенствование методов ведения пациентов с HBV-инфекцией [2].
Основные вопросы, обсуждавшиеся на конференции:
- первичное обследование пациентов с HBV-инфекцией;
- критерии назначения лечения больным ХГ В;
- разработка руководства для врачей по наблюдению за пациентами с ХГ В;
- оптимизация лечения (сравнение монотерапии, последовательного и комбинированного лечения ХГ В, его длительность).Обсуждались также и другие нерешенные вопросы:
- какова роль генотипа HBV в течении болезни?;
- какой из методов количественного определения HBV DNA следует считать наиболее точным?;
- роль биопсии печени.Первичное исследование пациента с HBV-инфекцией
Клиническое исследование пациента с предполагаемым диагнозом ХГ В включает следующие мероприятия:
- подтверждение диагноза;
- определение степени активности (тяжести воспаления) и стадии болезни (слабый, умеренный или выраженный фиброз);
- решение вопроса о необходимости противовирусного лечения.В стандартной практике для решения этих задач выполняются физикальное исследование пациента параллельно с анализом истории болезни и ряд лабораторных и инструментальных тестов. Привычные для нас биохимические показатели, такие, как активность аланинаминотрансферазы (АлАТ), служат суррогатными маркерами активности болезни (повреждения) печени и обычно тесно коррелируют с гистологической картиной.
Однако эти тесты не всегда надежны, поэтому пациентам рекомендуется биопсия печени, представляющая вспомогательный диагностический тест. Другие биохимические параметры, такие, как уровни сывороточного альбумина, билирубина, протромбиновое время, отражают функциональную активность печени и больше коррелируют со стадией болезни, то есть со степенью выраженности фиброза по гистологическим данным.
Исследование серологических тестов для определения антигенов HBV (HBsAg и HBeAg) и антител (anti-HBs, anti-HBc IgM и IgG, anti-HВe) к нему представляет собой рутинную лабораторную процедуру при диагностике ХГ В. Кроме того, важно помнить, что для правомочности термина "хронический" необходимо присутствие HBsAg в сыворотке крови не менее 6 мес.
Наиболее надежный тест вирусной репликации - количественное определение HBV DNA в сыворотке крови пациента.
В настоящее время отсутствует универсально принятый во всех лечебно-профилактических учреждениях метод количественного определения ДНК при первичном исследовании пациента. Ранее (2000 г.) Рабочая группа по ведению пациентов с хронической инфекцией вирусом гепатита В Национального института здоровья США рекомендовала рассматривать пациентов в качестве кандидатов для лечения, если у них уровень ДНК составлял более 105 копий/мл при использовании метода гибридизации.
В настоящее время рабочая группа рекомендует использовать для количественного определения HBV DNA методы, основанные на полимеразной цепной реакции (ПЦР), в частности метод ПЦР в реальном времени (real-time PCR). Нет единогласного соглашения о том, какой уровень вирусной нагрузки следует считать показанием к назначению противовирусного лечения.
Более того, единица измерения вирусной нагрузки должна быть стандартизована и сопоставима при исследовании этого показателя в различных лабораториях. Рекомендуется измерять уровень HBV DNA в международных единицах (МЕ). Одна МЕ приблизительно эквивалентна 5,6 копии/мл.
На основании биохимических, вирусологических и гистологических параметров пациенты с ХГ В распределяются на пять категорий (табл. 1).
Таблица 1. Варианты течения инфекции вирусом гепатита В [2]
Вариант течения инфекции HBV Лабораторные и гистологические признаки HBeAg+, активная форма гепатита HBeAg+, HBV DNA >105 копий/мл, персистирующее или интермиттирующее повышение активности АлАТ, различная степень активности и фиброз гистологически Иммунотолерантные пациенты HBeAg+, HBV DNA >105 копий/мл, нормальная активность АлАТ, минимальная гистологическая активность НВеАg-негативный хронический гепатит В HBeAg-, anti-HBe+, флюктуирующее, небольшое или умеренное повышение активности АлАТ и уровня HBV DNA, гистологическая активность Неактивные носители HBV HBeAg-, anti-HBe+, уровень HBV DNA - от неопределяемого до <104 копий/мл стойко нормальная активность АлАТ*** Разрешение хронического гепатита В
HBeAg-, HBsAg-, anti-HBs, anti-HBe, HBV DNA-, активность АлАТ - нормальная *** Дифференциальный диагноз с HBeAg-негативным ХГВ.Представленная в табл. 1 классификация служит основой для выбора лечебной тактики. Следовательно, все ее составляющие должны быть стандартизованы.
Целесообразность измерения уровня вирусной нагрузки в широкой клинической практике
Наиболее аргументированное обоснование необходимости измерения вирусной нагрузки в широкой клинической практике - данные о том, что этот показатель представляет собой независимый фактор риска развития ГЦК и ЦП.
В этом аспекте следует отметить проспективное когортное исследование C.J. Chen и соавт. [1]. В нем изучалось взаимоотношение между уровнем HBV DNA в сыворотке крови и риском развития ГЦК. Когорту составили жители 7 тайваньских городов. Согласно критериям включения (отсутствие anti-HCV и признаков ГЦК, положительный HBsAg в момент включения в исследование) были отобраны 3653 больных, не получавших противовирусного лечения в период наблюдения (1991-2004). Средний срок наблюдения составил 11,4 года.
В период наблюдения зарегистрировано 164 впервые выявленных случая ГЦК. Методом унивариантного анализа выделены факторы риска развития ГЦК: мужской пол, старший возраст, курение сигарет, употребление алкоголя, наличие HBeAg-антигена, повышенный уровень активности АлАТ (более 45ед./л), ЦП, уровень HBV DNA > 10 000 копий/мл. При мультивариантном анализе подтверждена достоверность влияния всех указанных факторов риска, за исключением курения сигарет и повышения активности АлАТ.
Суть важного результата исследования C.J. Chen и соавт. состоит в том, что сама по себе высокая вирусная нагрузка у НВеАg-негативных пациентов, имеющих нормальный уровень активности АлАТ, вне зависимости от наличия ЦП является фактором высокого риска развития ГЦК (рис. 1,2).
Рис. 1. REVEAL (The Risk Evaluation of Viral Load Elevation and Associated Liver Disease/Cancer): высокий уровень вирусной нагрузки взаимосвязан с увеличением частоты гепатоцеллюлярной карциномы (по C.J. Chen et al. [1])
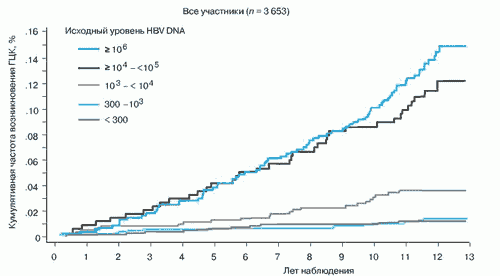
Рис. 2. REVEAL: высокий уровень вирусной нагрузки взаимосвязан с увеличением частоты гепатоцеллюлярной карциномы (по C.J. Chenetal. [1])
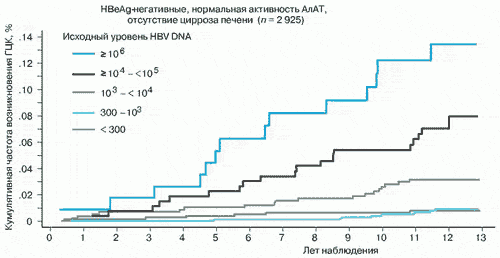
Другой аспект исследования касается связи между уровнем вирусной нагрузки и риском прогрессирования ХГ В в ЦП. Показано, что риск развития ЦП достоверно увеличивается с повышением количества циркулирующей HBV DNA [5] и не зависит от наличия или отсутствия НВеАg и активности сывороточной АлАТ (рис. 3).
Рис. 3. REVEAL: высокий уровень вирусной нагрузки взаимосвязан с увеличением риска развития цирроза печени (по U.H. Iloejeetal. [5])
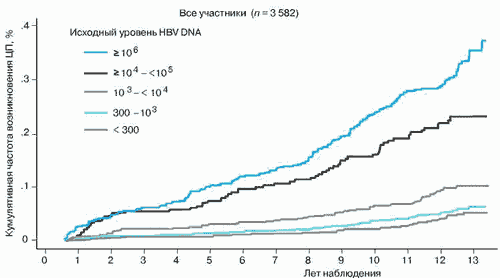
Мы не можем полностью экстраполировать эти данные на европейскую популяцию. Тем не менее они должны быть использованы при разработке рекомендаций практическим врачам, занимающимся ведением пациентов с хронической HBV-инфекцией.
Есть ли необходимость исследования генотипа HBV в широкой врачебной практике?
HBV имеет 8 генотипов (от А до Н). Каждый генотип имеет особенности своего географического распределения.
Так, генотип А более характерен для Северной Америки, Северо-запада Европы и Центральной Африки. Генотипы В и С распространены в Китае, Японии и южной Азии, генотип D - в Средиземноморье, России, на Среднем Востоке и в Индии, генотип Е - в Западной Африке, генотип F- на Аляске и в Полинезии. Генотип G независимо регистрируется во Франции и в Северной Америке, в то время как генотип Н обнаружен в Центральной Америке.
Получены данные о клиническом значении генотипов HBV. Показано, что генотип может коррелировать с ключевыми клиническими особенностями болезни, например, с частотой спонтанной сероконверсии по HBeAg, прогрессированием печеночного процесса, ответом на лечение, частотой клинически значимых мутаций вируса (табл. 2).
Таблица 2. Географическое распределение генотипов HBV и их клиническое значение [2]
Генотип HBV Географическое распределение Клиническое значение (в сравнении с другими генотипами) А Центральная Африка, Европа Северная Америка Лучший ответ на введение пегилированного интерферона В Kитай, Индонезия, Тайвань, Вьетнам Ниже активность гепатита. Более низкий риск развития ГЦK. Лучший ответ на лечение С Kитай, Япония, Kорея, Полинезия, Тайвань Вьетнам Более тяжелое течение болезни с худшим прогнозом D Индия, Средиземноморье, Россия Средний Восток Частые мутации в ргесог-регионе Е Западная Африка Нигерия и др. Не известен F Аляска, Полинезия - " - G Франция, Северная Америка - " - Н Центральная Америка - " - Большинство исследований в этой области выполнено в Азии. Необходимо отметить, что эффективность лечения больных ом и пегилированным интерфероном а-2а не зависит от генотипа HBV.
В целом можно заключить, что определение генотипа HBV облегчает ведение пациентов с ХГ В, однако рекомендовать его в широкую практику врачей еще рано, в первую очередь потому, что метод генотипирования HBV еще не стандартизован.
Кому необходимо противовирусное лечение?
Ближайшие цели лечения ХГ В включают снижение вирусной нагрузки, нормализацию активности сывороточной АлАТ и уменьшение некровоспалительной активности в печени. При достижении ближайших целей замедляется развитие печеночного фиброза.
К долгосрочным целям лечения относят предотвращение развития ЦП и ГЦК.
Благодаря реализации долгосрочных целей улучшается показатель выживаемости пациентов.
Современные методы лечения вполне обеспечивают достижение ближайших целей лечения. Что касается долгосрочных целей, то их достижению препятствуют развитие вирусной резистентности и побочные эффекты используемых препаратов. Следовательно, лечение должно проводиться пациентам с риском прогрессирования болезни.
Отбор пациентов для лечения проводится с учетом полного спектра результатов биохимических и вирусологических исследований.
В спорных случаях в решении помогают результаты биопсии печени. Группой наибольшего риска прогрессирования болезни считаются пациенты с высокими уровнями вирусной нагрузки и активности АлАТ. Они же являются основными кандидатами для противовирусного лечения.
Терапевтические рекомендации, основанные на НВеАg-статусе, уровнях HBV DNA и активности АлАТ, указаны в табл. 3.
Таблица 3. Терапевтические рекомендации, основанные на НВеАg-статусе, активности АлАТ и уровне HBV DNA
АлАТ HBV DNA Терапевтические рекомендации HBeAg-позитивный хронический гепатит В < 2 * ЛВН Определяется Мониторирование (1-2) * ЛВН - " - "Серая зона": биопсия печени, лечение при умеренной - высокой активности или выраженном фиброзе >2 * ЛВН - " - Наблюдение 3-6 мес Лечение, если нет спонтанной НВеАg-сероконверсии НВеАg-негативный хронический гепатит В < 2 * ЛВН < 106 копий/мл Мониторирование (1-2) * ЛВН 104-106 копий/мл "Серая зона": биопсия печени, лечение при умеренной - высокой активности или выраженном фиброзе > 2 * ЛВН > 106 копий/мл Лечение Решение о назначении противовирусного лечения
FDA одобрены пять препаратов для лечения ХГ В, в России в настоящее время их три. Все они относятся к препаратам первой линии при компенсированном заболевании печени (табл. 4, 5).
Таблица 4. Лекарственные средства лечения хронического гепатита В
Режим Используется в России Ожидается Интерферон/пегилированный интерферон Ламивудин Адефовир Показания НВеАg+ Да Да Да Да НВеАg- Да Да Да Да Декомпенсированный ЦП Нет Нет Да Нет Путь введения Инъекции Per os Per os Per os Эффективность при НВеАg+ HBeAg-сероконверсия, % 22-33 15-17 11 21 Элиминация HBV DNA, % 25 36 21 67 Уменьшение количества HBV DNA, log10, копий/мл 4,5 5,6 3,6 6,9 Таблица 5. Лекарственные средства лечения хронического гепатита В [2]
Режим Используется в России Ожидается Интерферон/пегилированный интерферон Ламивудин Адефовир Эффективность при HBeAg- Элиминация HBV DNA, % 63 65-72 51 90 Уменьшение количества HBV DNA, log10, копий/мл 4,1 4,5 3,9 5,0 Устойчивость ответа НВеАg+, % 22-33 15-17 12 21 НВеАg-, % 20-30 < 10 8 Нет Резистентность Нет 1-й год - 25%
4-й год - 70%1 -й год - 0%
4-й год - 29%1 -й год - 0%
4-й год - 0%Активность при ламивудинорезистентности Да Нет Да Да Новые лекарственные средства в данный период проходят третью фазу клинических испытаний.
Ламивудин был первым пероральным лекарственным агентом, одобренным для лечения ХГ В. Основной его недостаток - высокая частота развития мутаций, что может нивелировать первично достигнутый клинический эффект лечения как у НВеАg-позитивных, так и у НВеАg-негативных пациентов. Другой его недостаток - высокая частота рецидивов болезни после окончания лечения.
- новый аналог нуклеотидов, по данным клинических исследований, способен более эффективно снижать вирусную нагрузку (на 6 log) по сравнению с ламивудином на 48-й неделе лечения у НВеАg-позитивных больных. О частоте развития резистентности в сроки использования препарата более 2 лет данных еще нет. Очень важно, что энтекавир активен против ламивудинорезистентных штаммов HBV [The New England Journal of Medicine, March 9, 2006 Vol. 354 N 10; 1001-1009].
Адефовир сходен с ламивудином по механизму действия. Главное его преимущество - низкий уровень резистентности у первично пролеченных больных и эффективность у пациентов, резистентных к ламивудину.
Нефротоксичность относится к отрицательным качествам адефовира, который должен осторожно применяться у пациентов с пограничной функцией почек.
Пегилированный (стандартный) интерферон а-2а вызывает высокую частоту НВеАg-сероконверсии при диком штамме HBV и не приводит к развитию резистентности. Длительность лечения этим препаратом определена четко. Однако он не может использоваться при декомпенсированном заболевании печени.
Решение о назначении противовирусного лечения должно быть аргументированным и взвешенным из-за его высокой стоимости, побочных эффектов и (в случае аналогов нуклеозидов/нуклеотидов) неопределенной продолжительности курса терапии.
Выбор противовирусного препарата проводится индивидуально. Во внимание принимаются возраст пациента, НBeAg-статус, стадия болезни, вероятность противовирусного ответа, потенциал побочных действий и осложнений. Важно также помнить о ранее проведенном лечении, первичном ответе на него и лекарственной резистентности.
Когда заканчивать лечение?
Лечение НВеАg-позитивных больных стандартным и пегилированным интерфероном а-2а длится 4-6 мес и 1 год соответственно. Исчезновение НВеАg - оправданное обоснование окончания терапии для этой группы.
Лечение может быть завершено ранее запланированного срока, если исчезновение HBeAg определяется и сохраняется при двух последовательных визитах пациента к врачу, по крайней мере с интервалом в 1 мес.
Для аналогов нуклеозидов/нуклеотидов рекомендуемая продолжительность лечения - 1 год. Однако только у небольшого процента больных к этому сроку исчезает НВеАg. Если однажды зарегистрировано исчезновение НВеАg, то лечение продолжается не менее 6 мес для уверенности в стойкости полученного результата. Если НВеАg сохраняется, то лечение продолжается неопределенно долго.
Для НВеАg-позитивных пациентов критерием окончания терапии считается элиминация HBsAg (встречается очень редко).
Для HBeAg-негативных пациентов "конечная точка" терапии - достижение неопределяемого в сыворотке крови уровня HBV DNA методом ПЦР и нормализация активности АлАТ. Оптимальная длительность терапии не установлена. Надежный критерий окончания лечения - только элиминация HBsAg, что и в этой популяции происходит очень редко.
Исследование резистентности
Лекарственная резистентность - основная причина неудачи длительного лечения аналогами нуклеозидов/нуклеотидов. Три определения лекарственной резистентности сформулированы Рабочей группой Национального института здоровья США.
1. Генотипическая резистентность - определение мутаций, обнаруживающихся во время антивирусного лечения конкретным препаратом (например, YMDD-мутации, ассоциированные с лечением ламивудином).
2. Вирусологический прорыв - повышение уровня сывороточной HBV DNA во время терапии (следует за появлением генотипической резистентности). Обычно это подтверждается повышением уровня вирусной нагрузки на 1 log копий/мл в сравнении с предыдущими значениями (за исключением случаев, когда пациент не следует рекомендациям врача и не соблюдает необходимого режима приема препарата).
3. Клиническая резистентность- клиническая манифестация вирусологического прорыва. Проявляется повышением активности сывороточной АлАТ и ухудшением клинического течения болезни.Для подтверждения развития резистентности используются ПЦР в реальном времени, исследование полиморфизма длинных рестрикционных фрагментов или прямое секвенирование.
В настоящее время не уточнены преимущества каждого из указанных методов. Определение вирусной резистентности представляет четкое научное направление, которое может оказать значительную помощь клиницисту.
Рекомендации клиницистам
1. ДЛЯ классификации пациентов с хронической HBV-инфекцией (в пять категорий болезни - от 1-й до 5-й) обычно используются тесты: биохимические (активность сывороточной АлАТ) и вирусологические (HBV DNA, HBsAg, HBeAg, anti-HBe) с (без) биопсий печени.
2. В настоящее время доступно несколько методов количественного определения HBV DNA в сыворотке крови. Методом выбора может служить ПЦР в реальном времени. Однако в этой области необходимы дальнейшие исследования. Уровень HBV DNA целесообразно измерять в МЕ/мл, чем в копиях/мл, поскольку возможна интернациональная стандартизация этой единицы.
3. Определение генотипа HBV может облегчить ведение пациентов, но еще не рекомендуется для внедрения в рутинную клиническую практику до завершения научных исследований и стандартизации методов.
4. Лечение пациентов проводится согласно международным стандартам. Выбирать лекарство необходимо для каждого пациента индивидуально с учетом клинических особенностей болезни, планируемой эффективности выбранного препарата, продолжительности вирусологического ответа, частоты развития резистентности, побочных действий и стоимости лечения.
5. Ближайшие цели противовирусного лечения: снижение вирусной нагрузки, нормализация активности сывороточной АлАТ, уменьшение печеночного воспаления и прогрессирования фиброза.
Отдаленные цели лечения - предупреждение развития ЦП и ГЦК, избавление пациента от необходимости трансплантации печени, улучшение показателя выживаемости.
Современные терапевтические средства дают возможность достичь ближайшие цели лечения у большинства пациентов. Однако достижение отдаленных целей терапии сдерживается развитием вирусной резистентности и побочных действий лекарств.
6. Пациенты с персистирующим повышением активности АлАТ и позитивным тестом на HBV DNA на протяжении 6 мес и более рассматриваются в качестве кандидатов для противовирусного лечения.
7. HBeAg-позитивные пациенты с постоянно нормальным уровнем активности АлАТ и умеренной или высокой вирусной нагрузкой обычно подлежат наблюдению. Лечение им назначается тогда, когда повышается активность АлАТ.
8. Пациенты из "серой зоны" (АлАТ менее 2 норм) должны подвергаться биопсии печени. Лечение назначается тем больным, у которых имеются умеренное или тяжелое воспаление и выраженный фиброз (METAVIR > 2, индекс гистологической активности Knodell или Ishak > 3). 9. Неактивным носителям HBV лечение не назначается до тех пор, пока не появятся клинические признаки обострения болезни.
10. Будущие исследования помогут оценить необходимость комбинированной терапии в сравнении с последовательным лечением и выбрать оптимальные режимы лечения ХГ В.
Список литературы
1. Chen C.J., Yang H.I., Su J. et al. (the REVEAL-HBV Study Group). Risk of Hepatocellular Carcinoma Across a Biological Gradient of Serum Hepatitis B Virus DNA Level // JAMA. - 2006. - Vol 295. -P. 65-73.
2. Clinical Care Options Management of Hepatitis B Virus 2006 National Institutes of Health Workshop, April 6-8, 2006, Bethesda, Maryland.
3. EASL International Consensus Conference on Hepatitis B, 13-14 Sept., 2002, Geneva, Switzerland.
4. Fung S.K., Lock A.S. Management of patients with hepatitis В virus-induced cirrhosis // Hepatology. - 2005. - Vol. 42. - S 54-S64.
5. Noeje U.H., Yang H.I., Su J. et al. (the REVEAL-HBV Study Group) Predicting Cirrhosis Risk Based on the Level of Circulating Hepatitis B Viral Load // Gastroenterology. - 2006. - Vol.130. - P. 678-686.
6. Keeffe E.B., Dieterich D.T., Han S.H. et al. Treatment Algorithm for the Management of Chronic Hepatitis B Virus Infection in the Unated States: an Update // Clin. Gastroenterol. Hepatol. - 2006. - Vol. 4. -N 8.- P.
7. Lock A., McMahon B. Chronic Hepatitis В // AASLD. - Practical Guidelines, Oct. 2002.-P.1 225-1241.
Статья подготовлена по материалам Рабочей группы по ведению пациентов с хронической инфекцией вирусом гепатита В Национального института здоровья США, Бетезда, 6-8 апреля 2006 г. при поддержке компании "Bristol-Myers Squibb"
| Сентябрь 2007 г. |