Стадия IV НМРЛ: разработка плотнодозовых недельных графиков применения Таксола (паклитаксел) для инъекций индивидуально и в сочетании с карбоплатином
Ч. П. Белани и М. А Сосински
Институт Онкологии Питтсбургского Университета
Питтсбург, Пенсильвания и
Программа Торакальной Онкологии
Университет Северной Каролины
Чепел Хилл, Северная Каролина
ВВЕДЕНИЕ
В недавно опубликованных Американским обществом клинических онкологов (ASCO) и Национальной Онкологической Сетью (NCCN) материалах комбинированная химиотерапия на основе препаратов платины рекомендуется для лечения первой линии и последующего лечения соответствующих больных с метастатическим немелкоклеточным раком легкого (НМРЛ) [1, 2]. Такая химиотерапия является наиболее подходящей для больных с хорошим функциональным статусом (функциональный статус по ECOG/Zubrod 0-1 или возможно 2), поскольку у таких больных выше вероятность объективной ремиссии, они дают более высокий процент выживаемости и у них меньше вероятность наступления побочных эффектов, связанных с лечением. Кроме того, вышеупомянутые правила-рекомендации признают, что опыт химиотерапии у больных с удовлетворительным функциональным статусом является ограниченным, поскольку такие больные обычно исключаются из клинических испытаний [1]. NCCN также рекомендует химиотерапию для лечения второй линии у больных с хорошим функциональным статусом при рецидиве или повторном обострении заболевания [2].
Оптимальный режим комбинированной химиотерапии на основе препаратов платины для больных с распространенной формой НМРЛ пока не определен [1]. В ряде недавних клинических испытаний, проводившихся по Фазе II и III, внимание было сосредоточено на комбинации полусинтетического Таксола (паклитаксел) для инъекций и карбоплатина [3-5]. Результаты показали, что эта комбинация эффективна и обычно хорошо переносится больными при проведении лечения первой линии по поводу распространенного НМРЛ. В этих исследованиях комбинация Таксол/карбоплатин воспроизводимо давала годичную выживаемость в интервале от 27 до 54% (Таблица 1) [3, 5, 6]. В одном исследовании с достаточно длительным сроком наблюдения выживаемость на протяжении 2 лет составляла 10% [9].
Таблица 1. Испытания полусинтетического Таксола (паклитаксел) для инъекций/карбоплатин в рамках Фазы II/III при распространенном НМРЛ: результаты по выживаемости
Исследование
ФазаСхема
Кол-во больных Выживаемость Годичная выживаемость (%) Belani et al. (1998)* Фаза III Таксол 225 мг/м2 3-ч ВВ, д1 Карбоплатин AUC 6 ВВ, д1 каждые 3 недели
Цисплатин 75 мг/м2 ВВ, д1
Этопозид 100 мг/м2 ВВ, д1-3, каждые 3 неделиKosmidis et al (1997) Фаза III Таксол 175 мг/м2 24-ч ВВ, д1 Карбоплатин AUC 6 ВВ, д1 каждые 3 недели Таксол 225 мг/м2 3-ч ВВ, д1 Карбоплатин AUC 6 ВВ, д1 каждые 3 недели Langer et al (1995) Фаза II Таксол 135-215 мг/м2 24-ч ВВ, д1 Карбоплатин AUC 7,5 ВВ, д1 каждые 3 недели Hainsworth et al (1998) Фаза II Таксол 225 мг/м2 1-ч ВВ, д1 Карбоплатин AUC 6 ВВ, д1 каждые 3 недели Gatzemeier et al (1999) Фаза III Таксол 200 мг/м2 3-ч ВВ, д1 Карбоплатин AUC 6 ВВ, д1 каждые 3 недели Таксол 200 мг/м2 3-ч ВВ, д1 Цисплатин 80 мг/м2 ВВ, д1 каждые 3 недели НМРЛ=немелкоклеточный рак легкого; ВВ=внутривенно; AUC=площадь под кривой концентрация в плазме/время
1) Токсические эффекты степени 3/4, описанные для обоих вариантов лечения, включали нейтропению (включая фебрильную нейтропению), рвоту, понос, миалгию/артралгию (только группа Таксол/карбоплатин), периферическую нейропатию и ототоксичность (только группа цисплатин/этопозид).
2) Доза карбоплатина рассчитывалась по формуле Кальверта: общая доза (мг)=(желаемая AUC) х (СГФ+25). При использовании формулы Кальверта общая доза карбоплатина рассчитывается в миллиграммах, а не в мг/м2 (СГФ=скорость гломерулярной фильтрации).
3) Токсические эффекты степени 3/4 включали анемию, нейтропению, тромбоцитопению, алопецию и нейротоксичность (только степени 3; описана только для более высокой дозы).
4) Токсичность включала анемию степени 3/4, гранулоцитопению, тромбоцитопению, а также рвоту степени 3, анорексию, чувство усталости, миалгию/артралгию и парестезии.
5) Токсичность включала лейкопению и тромбоцитопению степени 3/4, токсические эффекты степени 4 в отношении сердца и кожи, а также анемию степени3, миалгию/артралгию, периферическую нейропатию, мукозит и тошноту/рвоту.
6) За исключением нейтропении, тромбоцитопении, тошноты/рвоты и нейротоксичности, проценты тяжелых токсических эффектов были низкими и сходными для двух вариантов лечения.Результаты недавних испытаний по Фазе III, описанные группами SWOG и ECOG, показывают меньший процент серьезных токсических эффектов для комбинации Таксол/карбоплатин по сравнению с другими схемами лечения на основе цисплатина [10, 11]. Группа SWOG приняла решение, что комбинация полусинтетический Таксол (паклитаксел) для инъекций/карбоплатин является предпочтительной схемой лечения для будущих испытаний в связи с более благоприятным профилем токсичности, лучшей переносимостью, а также лучшими условиями выполнения протокола. В исследовании группы ECOG частота токсических эффектов степени 3-5 в случае комбинации Таксол/карбоплатин была меньшей, чем в случае трех других, использованных для сравнения схем лечения на основе цисплатина у больных с функциональным статусом 2 (Таблица 2) [11]. Аналогичным образом в исследовании SWOG частота нейтропении, лейкопении 4-й степени и рвоты 3-й степени была меньшей у больных, получавших схему Таксол/карбоплатин, по сравнению с больными, получавшими комбинацию винорелбин/цисплатин, в то время как частота миалгий/артралгий и нейропатии была более высокой (Таблица 3) [10, 12]. Недавно проведенный анализ клинической практики в США позволил определить, что комбинация Таксол/карбоплатин является предпочтительной схемой для онкологов, занимающихся лечением больных с распространенной формой НМЛР 14].
Таблица 2. Исследование ECOG 1594: побочные эффекты степени 3-5 (промежуточный анализ) [11]
ФС=функциональный статус; ПЭ=побочные эффекты степени 3-5; AUC=внутривенно; AUC=площадь под кривой концентрация в плазме/время
n (%)
n (%)Таксол 135 мг/м2 24-ч ВВ, д1
Цисплатин 75 мг/м2 ВВ, д2
3-недельный курсГемцитабин 1000 мг/м2/д, д1, 8, 15
Цисплатин 100 мг/м2 ВВ, д1
4-недельный курс
Доцетаксел 75 мг/м2 ВВ, д1
Цисплатин 75мг/м2 ВВ, д1
3-недельный курсТаксол 225 мг/м2 3-ч ВВ, д1
Карбоплатин AUC 6 ВВ, д1
3-недельный курс
1)Токсические эффекты не указаны
2) В рамках отдельного анализ токсические эффекты, описанные более чем в одном варианте лечения, были следующими: лейкопения степени 4, нейтропения и тромбоцитопения; инфекции степени 4/5; тошнота и рвота степени 3/4, понос, стоматит, токсическое действие на печень, легочная токсичность, гипотензия, аллергия и артралгия; токсические эффекты степени 3-5 на мочеполовую систему, сердце и неврологические токсические эффекты [13]
3) Доза карбоплатина рассчитывалась по формуле Кальверта: общая доза (мг)=(желаемая AUC) х (СГФ+25). При использовании формулы Кальверта общая доза карбоплатина рассчитывается в миллиграммах, а не в мг/м2 (СГФ=скорость гломерулярной фильтрации).Таблица 3. Исследование SWOG 9509: токсические эффекты степени 3/4 [10]
НД=недостоверно.
Таксол 225 мг/м2 + карбоплатин AUC 6 каждые 3 недели (n=204) Винорелбин 25 мг/м2 + цисплатин 100 мг/м2 каждые 4 недели (n=196) Гематологические
Лейкопения Нейтропения Негематологические
Тошнота Нейропатия Рвота Смерть от токсичес-ких эффектов
Доза карбоплатина рассчитывалась по формуле Кальверта: общая доза (мг)=(желаемая AUC) х (СГФ+25). При использовании формулы Кальверта общая доза карбоплатина рассчитывается в миллиграммах, а не в мг/м2 (СГФ=скорость гломерулярной фильтрации).В исследованиях, приведенных в Таблице 1, Таксол использовался в относительно стандартной дозе, составлявшей 175-225 мг/м2, и вводился по стандартному графику, т.е. раз в 3 недели. Однако оптимальная доза и график введения Таксола у больных с распространенной формой НМРЛ все еще являются предметом исследования. Одним из наиболее обнадеживающих подходов к оптимизации терапевтических преимуществ Таксола является введение этого агента еженедельно. В ранних клинических испытаниях еженедельное применение Таксола оценивалось в форме монотерапии у больных с рецидивировавшим в предыдущей или новой локализации заболеванием после химиотерапии первой линии [15, 16]. В последующих испытаниях Таксол, вводившийся по схеме один раз в неделю, применялся индивидуально или в комбинации с карбоплатином в рамках терапии первой и второй линии у больных с распространенной формой НМРЛ [16-21]. В настоящей статье обсуждается роль комбинированной химиотерапии при условии введения Таксола по схеме один раз в неделю в лечении метастатической формы НМРЛ.
Обоснование еженедельного применения полусинтетического Таксола (паклитаксел) для инъекций
Обоснование еженедельного применения Таксола связано с гипотезой, что продолжительное кумулятивное воздействие и плотнодозовая терапия могут повысить терапевтическую активность данного агента [22].
Доклинические данные указывают на то, что продолжительность воздействия препарата является важным фактором в отношении определения цитотоксичности Таксола, и при продолжительной экспозиции может достигаться цитотоксическое действие в отношении клеток при относительно низких концентрациях Таксола (0,01 мкМ/л) [22-24]. Такие концентрации относительно легко достигаются у человека путем вливания Таксола на протяжении продленного 96-часового периода [23, 26, 27] или путем введения его часто и повторно, т.е. по схеме один раз в неделю. Поскольку продолжительные вливания могут вызывать неудобство у больных и приводить к серьезным организационным проблемам для клиник, в которых проводится лечение, более частое повторное введение является предпочтительным подходом [22].
Хотя при введении Таксола по схеме один раз в неделю достигаются максимальные (пиковые) концентрации, сходные с теми, которые создаются при применении препарата по схеме раз в 3 недели, частота и тяжесть обычных токсических эффектов, связанных с лечением, таких как миелосупрессия и нейропатия, может быть меньше. В результате еженедельное применение препарата обеспечивает большую непрерывную экспозицию Таксолу и приводит к тому, что интенсивность дозы оказывается более высокой [22]. Относительное отсутствие миелосупрессии, отмечающееся в условиях применения Таксола по схеме один раз в неделю, делает этот график применения перспективной основой для комбинированных схем лечения [22, 28].
Путем сокращения периода между введениями Таксола с трех недель до одной недели повышается плотность дозы и, соответственно, интенсивность дозы Таксола. Теория плотнодозовой терапии основанана на математической модели динамики развития опухоли Гомперца. В соответствии с этой моделью, доля клеток, которые гибнут, возрастает по мере уменьшения общего количества клеток; однако последующий рост опухоли происходит быстрее, если общее число клеток снижено. Поэтому частое воздействие цитотоксическим агентом за счет укорочения интервалов между введениями может подавлять повторный рост опухоли между курсами лечения и ограничивать появление устойчивых к лекарственному препарату линий клеток [29].
Кроме того, исследования in vitro показали, что Таксол обладает антиангиогенными свойствами [30, 31] и способствует апоптозу [22, 33]. Эти свойства зависят от фазы клеточного цикла и могут также вносить вклад в противоопухолевое действие Таксола [30, 32, 33]. В случае некоторых линий опухолевых клеток противоопухолевая активность Таксола коррелирует со способностью препарата индуцировать апоптоз, а не с его активностью в отношении остановки митоза [32]. Предполагается, что Таксол индуцирует апоптоз за счет стимулирования треониновой протеинкиназы (Raf-1), которая фосфорилирует и, соответственно, инактивирует антиапоптозный белок Bcl-2 в ряде линий опухолевых клеток [33].
Введение полусинтетического Таксола (паклитаксел) для инъекций по схеме один раз в неделю оценивалось в ряде испытаний по Фазе II, проводившихся у больных с распространенной или метастатической формой рака молочной железы [34, 41] и при рецидивах рака яичника [28, 42, 43]. Результаты этих испытаний показывают, что Таксол, применяемый по схеме один раз в неделю, как правило, хорошо переносится [28, 35-43], причем профиль его токсичности представляется более благоприятным, чем в случае стандартного применения по схеме один раз в 3 недели [28, 38, 41, 42].
Рак молочной железы
У больных с метастатической формой рака молочной железы Таксол, применяемый по схеме один раз в неделю, обладает активностью и обычно хорошо переносится как в виде химиотерапии первой линии, так и у ранее леченых больных. В самом крупном испытании, проводимом по Фазе II, Таксол вводили по схеме один раз в неделю в дозе 80 мг/м2 путем 1-часового вливания 212 больным с метастатической формой рака молочной железы до прогрессии заболевания или появления неприемлемых токсических эффектов. Хотя большинство больных ранее подвергались лечению, Таксол, применявшийся по схеме один раз в неделю, хорошо переносился больными; токсические эффекты степени 3/4 включали нейтропению (13%), анемию (9%), фебрильную нейтропению (1%) и тромбоцитопению (1%). Нейропатия 3-й степени наблюдалась у 8% больных в среднем через 4,3 цикла Таксола, применявшегося по схеме один раз в неделю. Явлений негематологической токсичности 4-й степени не наблюдалось. При промежуточном анализе ремиссии были отмечены у 23% больных, причем полные ремиссии наблюдались в 2% случаев, а частичные ремиссии в 21%. Стабилизация заболевания была отмечена еще у 32% больных. Анализ подгрупп показал, что общий процент ремиссий составлял 33% среди женщин, получавших Таксол по схеме один раз в неделю в качестве терапии первой линии, и 20% среди тех, кто ранее уже получал лечение таксанами [34].
В других испытаниях Фазы II еженедельный Таксол применялся в дозах до 100 мг/м2 у больных с распространенной или метастатической формой рака молочной железы. В этих исследованиях участвовали больные с рецидивирующей формой заболевания после предшествующей терапии антрациклинами и/или таксанами [35-39]; в двух исследованиях участвовали больные, которые ранее получали высокодозовую химиотерапию в сочетании с поддержкой стволовыми клетками [37, 39]. Общий процент ремиссий составлял от 40 до 92% [35, 39], в большинстве этих испытаний нейтропения степени 3/4 отмечалась лишь в редких случаях [35, 37-39].
Недавнее исследование, проведенное на 155 больных с метастатическим раком молочной железы, ранее не получавших лечения, было посвящено оценке комбинированной химиотерапии, включавшей еженедельное применение Таксола. Таксол в дозе 80 мг/м2 применялся в сочетании с лейковорином (20 мг/м2) и 5-фтороурацилом (5-ФУ) в дозе 425 мг/м2 еженедельно. Поскольку полную дозу препарата оказалось возможным использовать только в 37% курсов лечения, схема была изменена с тем, чтобы включить недельный отдых (в рамках курса, когда препарат применяется в течение 3 недель подряд, а на протяжении 4-й недели не используется). В результате частота токсических эффектов степени 3/4 была снижена; наиболее частыми токсическими эффектами были нейтропения (6%), нейропатия только 3-й степени (8%), понос (9%) и астенические явления (9%). Полнодозовый и модифицированный режимы дали полные ремиссии у 5% и 4% больных, соответственно, а частичные ремиссии наблюдались у 59% и 49% больных, соответственно [40]. В другом исследовании, также проведенном по Фазе II, полусинтетический Таксол (паклитаксел) для инъекций применялся еженедельно в дозе 80 мг/м2 совместно с лейковорином (10 мг/м2) и 5-ФУ (300 мг/м2) каждую неделю. На 2-й и 4-й дни вводили гранулоцитный колониестимулирующий фактор (G-CSF). Частичные ремиссии наблюдались у 6 из 10 больных, пригодных для оценки. Токсические эффекты носили легкий характер; среди 15 больных, включенных в испытание, не наблюдалось токсических эффектов степени 3/4 [41].
Рак яичника
Применение Таксола по схеме один раз в неделю подвергалось подробной оценке в испытаниях по Фазе I и II на больных с рецидивирующим раком яичника, включая женщин, у которых рецидив отмечался после стандартной комбинированной химиотерапии схемой Таксол/препарат платины [28, 42, 43]. В самом крупном испытании 208 больных с распространенной формой рака яичника, ранее получавших лечение максимум одной схемой, содержащей препарат платины, рандомизировали на получение лечения Таксолом еженедельно в дозе 67 мг/м2 или на стандартное введение Таксола в дозе 200 мг/м2 один раз в 3 недели. Интересно отметить, что токсические эффекты степени 3/4 были более частыми в случае стандартной схемы применения Таксола по сравнению со схемой, когда Таксол применялся по схеме один раз в неделю (нейтропения 43 и 19%, соответственно, нейропатии 25 и 10%, соответственно, артралгии/миалгии 7 и 5%, соответственно) (Рисунок 1). Чувство недомогания и усталости и изменения в ногтях были более частыми в том варианте схемы, когда Таксол применялся по схеме один раз в неделю. Проценты клинических ремиссий были сходными для двух вариантов лечения: 31 (включая 11% полных ремиссий) при применении Таксола по схеме один раз в неделю и 32% (включая 14% полных ремиссий) на стандартной схеме применения Таксола [42].
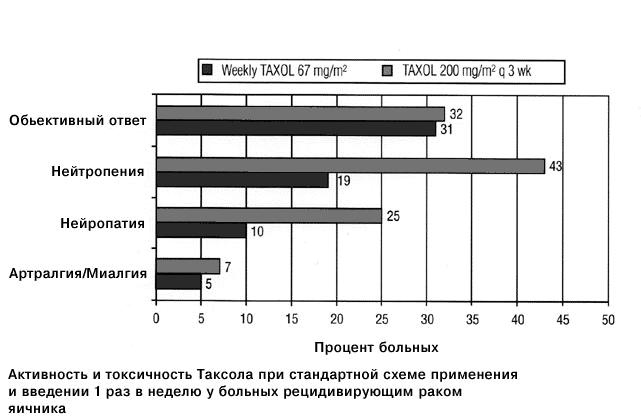
Рисунок 1. Активность и токсические эффекты 3/4 степени при введении Таксола один раз в неделю по сравнению со стандартным режимом его применения при рецидивирующих формах рака яичников [41].
В исследовании, проведенном по Фазе I, применение полусинтетического Таксола (паклитаксел) для инъекций по схеме один раз в неделю в дозе 50 или 100 мг/м2 проводили у 18 больных с рецидивировавшими формами эпителиального рака яичника; этих больных ранее лечили схемами, содержащими цисплатин, и они получали одну или несколько схем лечения, содержащих Таксол. В этой группе ранее интенсивно леченных больных не отмечалось токсических эффектов степени 3/4. Хотя эти исследования не были запланированы для определения эффективности лечения, частичные ремиссии наблюдались у 4 (31%) из 13 больных, пригодных для оценки, причем у 2 больных на стандартной схеме лечения Таксолом наблюдалось прогрессирование заболевания [28].
Сходные результаты были получены при ретроспективном рассмотрении историй болезни 45 больных с распространенной рецидивирующей формой эпителиального рака яичника, которых лечили Таксолом по схеме один раз в неделю в дозе от 60 до 100 мг/м2. Как и в исследовании по Фазе I, этих женщины ранее интенсивно лечили несколькими схемами системной химиотерапии, включавшими Таксол. Процент ремиссий в ответ на еженедельное применение Таксола составил 29%, причем для достижения ремиссии потребовалось в среднем (медиана) семь курсов лечения. Эта схема обычно хорошо переносилась, причем только в одном случае потребовалась госпитализация больного по поводу нейтропенической лихорадки [43]. Примечательно, что относительное отсутствие миелосупресии при данной схеме введения сделало еженедельную схему применения Таксола ценным вариантом для больных с недостаточными резервами костного мозга, а также для престарелых больных, которые считаются слишком слабыми для комбинированной химиотерапии [43, 44].
Разработка схем лечения, включающих еженедельное применение полусинтетического Таксола (паклитаксел)
для инъекций индивидуально или в сочетании с карбоплатином, для лечения стадии IV НМРЛ
Лечение второй линии и лечение больных с удовлетворительным функциональным статусом
Исследование по Фазе I/II, проведенное Чангом и соавт.
Монотерапия Таксолом по схеме один раз в неделю оценивалась у больных со стадией IV НМРЛ в рамках исследования по Фазе I/II, проведенного Чангом и соавт. Таблица 4 содержит характеристику больных для обеих фаз. В рамках оценки 17 больных по Фазе I Таксол применялся в дозах от 50 до 100 мг/м2 путем 1-часового внутривенного вливания в 1-й, 8-й и 15-й дни 4-недельного курса лечения. Средний возраст больных составлял 72 года (интервал 57-91), а 12 больных в прошлом получали химиотерапию. У 9 больных функциональный статус по ECOG составлял 2, а еще у 8 больных функциональный статус по ECOG составлял 0 или 1. Общий процент ремиссий составлял 35%, включая одного больного (6%), у которого отмечалась полная ремиссия, и пять больных (29%) с частичными ремиссиями. Средняя (медиана) продолжительность ремиссии составляла более 6 месяцев (интервал от 3,5 до 18 месяцев). Средняя выживаемость составляла 23 дня, а годичная выживаемость 35%. Максимальная переносимая доза (МПД) Таксола при введении по схеме один раз в неделю составляла 90 мг/м2 [16].Таблица 4. Испытание (Фазы I/II) применения Таксола по схеме один раз в неделю при стадии IV НМРЛ: характеристики больных [16]
Фаза I (n=17) Фаза II (n=27) Средний возраст, лет (интервал) Мужчины/женщины, n ФС по ECOG, n Предшествующая химиотерапия, n Метастазы в мозг, n В исследовании по Фазе II 27 больным Таксол в дозе 80 мг/м2 вводили путем 1-часового внутривенного вливания в 1-й, 8-й и 15-й дни 4-недельного курса лечения. Средний возраст больных составлял 72 года (интервал 44-85 лет); большинство больных (85%) не получали в прошлом химиотерапии. Из 27 больных 13 (48%) имели функциональный статус 2, а у остальных больных функциональный статус был равен 1. Процент общих ремиссий составлял 30%, сюда относилось восемь больных с частичными ремиссиями со средней продолжительностью (медиана) 5 месяцев (интервал от 1+ до 12 месяцев). Средний срок выживания составлял 184 дня, а годичная выживаемость 33% [16].
Среди 44 больных, участвовавших в этих двух испытаниях, общий процент ремиссий составлял 30%, а годичная выживаемость 35% (Таблица 5). Предшествовавшая химиотерапия заметно не влияла на выживаемость; однако мужской пол, плохой функциональный статус и преклонный возраст предсказывали худший прогноз. Полусинтетический Таксол (паклитаксел) для инъекций при введении по схеме один раз в неделю обычно хорошо переносился больными. Наиболее частыми тяжелыми токсическими явлениями в этих исследованиях были лейкопения (4-й степени - 2%, 3-й степени - 5%), инфекции (5-й степени - 2%, 3-й степени - 5%), анемия (3-й степени - 11%) и чувство недомогания и усталости степени 3 (5%). Двое больных скончались от инфекционных осложнений. Периферической нейропатии степени 3 не отмечалось, а периферическая нейропатия степени 1/2 отмечалась у 4 больных [16]. О связи между этими токсическими эффектами и дозой Таксола при применении по схеме один раз в неделю не сообщается.
Таблица 5. Комбинированные данные по лечению 44 больных в рамках исследования по Фазе I/II. Ремиссии и выживаемость в зависимости от характеристик больных [16]
ОР=общие ремиссии; МВ=медианная выживаемость; ФС=функциональный статус
Все больные Предшествующая химиотерапия Пол Мужчины Женщины Возраст ФС по ECOG Опыт Греческого института онкологии
Исследователи в Греческом институте онкологии (Hellenic Cancer Institute) провели исследование по Фазе I/II с использованием еженедельного графика применения полусинтетического Таксола (паклитаксел) для инъекций у 17 больных со стадией IV НМРЛ. Все больные ранее получали лечение по схеме МИП (митомицин, ифосфамид, цисплатин) в сочетании с гемцитабином или без него. Средний возраст (медиана) составлял 46 лет (интервал 37-55 лет). В исследование были включены больные с функциональным статусом по ECOG от 1 до 3. Таксол вводили путем 1-часового внутривенного вливания по схеме один раз в неделю на протяжении 6 недель, после чего следовал 2-недельный интервал без лечения. Исходная доза Таксола составляла 60 мг/м2, затем дозу увеличили до 90 мг/м2, поскольку схема обычно хорошо переносилась у первых шести больных. Дозу Таксола снижали в случае абсолютного содержания нейтрофилов менее 1500 клеток/мм3 или при нейропатии степени 2 или выше. Больные продолжали получать еженедельные вливания Таксола до прогрессии заболевания [15].Больных оценивали на ремиссию через 6 недель лечения. Вливания Таксола по схеме один раз в неделю дали частичные ремиссии у 8 из 17 больных. Все эти восемь больных получали дозу препарата 90 мг/м2; у шести из этих больных отмечалось улучшение функционального статуса от 3 до 1. У пяти больных, включая одного больного, получавшего дозу 90 мг/м2, и четырех больных, получавших дозу 60 мг/м2 отмечалась стабилизация заболевания в условиях еженедельных вливаний Таксола. У остальных четырех больных (23%) на меньшей дозе Таксола отмечалась прогрессия заболевания [15].
Исследователи указывают, что Таксол при применении по схеме один раз в неделю обычно хорошо переносился; токсических эффектов степени 3/4 не отмечалось. На протяжении 149 курсов лечения в ходе семи курсов отмечалась лейкопения 2-й степени тяжести, которая заставила отложить следующее введение препарата на одну неделю. Нейропатия 2-й степени наблюдалась у двух больных на 9-ом и 12-ом циклам, соответственно. Исследователи пришли к выводу, что Таксол при применении по схеме один раз в неделю дает высокий процент ремиссий и заслуживает дальнейшей оценки при распространенной форме НМРЛ [15].
Исследование Университета Северной Каролины
Исследователи в Онкологическом центре Лайнбергер Университета Северной Каролины провели исследование по Фазе III (LCCC 9719) для оценки влияния продолжительности лечения стандартной схемой Таксол/карбоплатин, применявшейся в качестве терапии первой линии, у больных с распространенной формой НМРЛ. Цель исследования заключалась в оценке роли Таксола при применении по схеме один раз в неделю в качестве терапии последнего выбора у больных с прогрессированием заболевания после стандартной схемы применения Таксол/карбоплатин первой линии. Больные с НМРЛ на стадии IIIB/IV и функциональным статусом по Карновскому 70% или выше были рандомизированы на получение Таксола в дозе 200 мг/м2 в сочетании с карбоплатином в дозе, дающей AUC=6, на протяжении четырех циклов или на получение аналогичной дозы и графика комбинации Таксол/карбоплатин до прогрессии заболевания (Рисунок 2). При прогрессии заболевания больных лечили полусинтетическим Таксолом (паклитаксел) для инъекций в дозе 80 мг/м2, который применяли по схеме один раз в неделю. Ответ на применение Таксола по схеме один раз в неделю будет оцениваться в трех группах больных: (1) больные, у которых прогрессия заболевания наблюдалась после исходных двух циклов стандартной схемы лечения первой линии Таксол/карбоплатин; (2) у больных, получивших четыре курса терапии первой линии, у которых перед началом прогрессии заболевания был период, когда лечение не проводили; (3) больных, у которых прогрессия заболевания отмечалась в ходе непрерывного лечения первой линии [45].
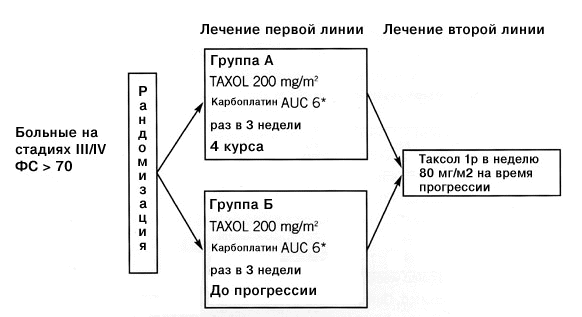
Рисунок 2. План испытания LCCC 9719, идущего в настоящее время по Фазе III по оценке еженедельного применения Таксола в качестве лечения второй линии при распространенной форме НМРЛ. ФС=функциональный статус; доза карбоплатина рассчитывалась по формуле Кальверта: общая доза (мг)=(желаемая AUC) х (СГФ+25). При использовании формулы Кальверта общая доза карбоплатина рассчитывается в миллиграммах, а не в мг/м2 (СГФ=скорость гломерулярной фильтрации) [12].
Применение полусинтетического Таксола (паклитаксел) для инъекций по схеме один раз в неделю в качестве терапии первой линии у больных с хорошим функциональным статусом
Опыт Университета Браун
Исследователи в Университете Браун провели исследование по Фазе I, используя Таксол по схеме один раз в неделю у больных, которым ранее не проводилась химиотерапия с НМРЛ на стадии IIIB/IV. Исследовали возможность проведения 3-часовых вливания Таксола в еженедельных дозах 100-200 мг/м2 по схеме 6 недель лечения, 2 недели отдыха. Максимальная переносимая доза составляла 175 мг/м2; токсическим эффектом, ограничивающим дозу, была нейтропения в условиях острой терапии, а в условиях длительной терапии таким эффектом была нейропатия [17]. Для оценки в последующем испытании по Фазе II была выбрана доза, равная 175 мг/м2.Для Фазы II этого исследования были выбраны ранее не леченные больные с НМРЛ на стадии IIIB/IV и функциональным статусом по ECOG от 0 до 2. В исследование также включали больных с метастазами в мозг. Больных с неудовлетворительным функциональным статусом и больных с метастазами в мозг включали, чтобы точнее отразить ситуацию с больными в обычных условиях. Схема исследования позволяла снижать дозу в случае высокой гематологической или неврологической токсичности. Дозу снижали на 50% при содержании гранулоцитов ниже 1500 клеток/мм3 или при нейропатии степени 2 и выше. Лечение прекращали в случае падения содержания гранулоцитов до значения менее 1000 клеток/мм3 или при нейропатии степени 3 и выше [18].
Всего в Фазу II этого испытания было включено 30 больных с НМРЛ, 29 больных на стадии IV и один больной на стадии IIIB. Четырнадцати больным ранее проводилась лучевая терапия, включая 11 больных, получавших лучевую терапию по поводу метастазов в мозг. В этом исследовании по Фазе II общий процент ремиссий составлял 48%. Выживаемость через 1 год и 2 года составляла 53 и 16%, соответственно. Четыре больных продолжили лечение в течение сроков более 2 лет, а двое больных продолжали лечение приблизительно в течение 3 лет [46].
На протяжении первого и второго курса продолжительностью по 8 недель еженедельное введение полусинтетического Таксола (паклитаксел) для инъекций было реализовано на уровне 83% и 75% по отношению к запланированной дозе, соответственно. На протяжении третьего-пятого курсов, однако, удалось использовать лишь приблизительно 50% от запланированной дозы [18, 46]. Ко второму курсу периферическая нейропатия степени 2/3 развилась приблизительно у трети больных и присутствовала почти у всех больных к третьему или четвертому курсу [18]. Нейропатия обычно уменьшалась на протяжении 2-недельного периода, когда терапии не проводили; эти данные указывают, что данные токсический эффект может иметь обратимый характер. Имела место тенденция к улучшению состояния в плане нейропатии при снижении дозы Таксола до 87,5 мг/м2 при графике лечения, когда препарат вводился в течение 6 последовательных недель с последующим 2-недельным периодом без введения препарата [46].
Содержание тромбоцитов увеличивалось на 17000/мм3 в неделю на протяжении первых 6 недель лечения, на основании чего можно считать, что Таксол, применяемый по схеме один раз в неделю, может быть приемлемой формой лечения даже у больных, содержание тромбоцитов у которых исключает лечение другими агентами (например, когда содержание тромбоцитов составляет менее 25000/ мм3) [46].
Опыт группы CALGB
Группа CALGB провела подтверждающее исследование по Фазе II (CALGB 9731), в котором больные с НМРЛ на стадии IIIB/IV, ранее не получавшие химиотерапии, получали лечение полусинтетическим Таксолом (паклитаксел) для инъекций, применявшимся по схеме один раз в неделю в дозе 150 мг/м2 по графику: 6 последовательных недель введения препарата, 2 недели отдыха [19]. Модификации дозировок были следующими: 50%-ное снижение дозы при общем содержании нейтрофилов менее 1500 клеток/мм3 и нейротоксичности степени 2 или выше на протяжении второго курса лечения или в последующем; пропуск дозы при содержании нейтрофилов меньше 1000 клеток/мм3 или нейротоксичности степени 3/4. Всего в этом исследовании принимало участие 38 пригодных для оценки больных. Средний возраст составлял 64,7 года (интервал 31-81 год), и у всех больных функциональный статус составлял от 0 до 1 (Таблица 6) [47]. У большинства больных (86%) отмечалась стадия IV НМРЛ, наиболее частым гистологическим типом была аденокарцинома [19]. У двух больных отмечались метастазы в мозг [47].Таблица 6. Исследование группы CALGB 9731: характеристики больных [19, 47]
Средний возраст, лет (интервал) 64,5 (31-81) Пол, n (%) Мужчины 21 (55) Женщины 17 (45) Функциональный статус, n (%) 0 17 (45) 1 21 (55) Стадия заболевания, n (%) IIIB 6 (16) IV 31 (86) Гистология, n (%) Аденокарцинома 25 (66) Плоскоклеточная карцинома 7 (18) Крупноклеточная карцинома 4 (11) Недифференцированный рак 2 (5) Метастазы в мозг, n (%) 2 (5) Общая токсичность была умеренной, но приемлемой (Таблица 7). Нейтропения степени 3/4 отмечалась у 26 и 13% больных, соответственно; нейропатия степени 2/3 наблюдалась у 29 и 24% больных, соответственно. Другие токсические эффекты 4-й степени включали одышку (5%) и понос (3%) [47].
Таблица 7. Исследование группы CALGB 9731: токсические эффекты степени 3/4 [19, 47]
*Глюкоза>250 мг/дл.
Нейтропения Инфекция Рвота Понос Анорексия Одышка Нейропатия Гипергликемия* Применение полусинтетического Таксола (паклитаксел) для инъекций по схеме один раз в неделю дало частичные ремиссии у 16 из 38 больных, а общий процент ремиссий составил 42% (Таблица 8). Еще у девяти больных (24%) отмечалась стабилизация заболевания; у восьми больных (21%) имела место прогрессия заболевания во время лечения. Среднее время выживания (медиана) составляло 12,3 месяца, причем на момент последнего сообщения 12 больных (32%) были еще живы [47].
Таблица 8. Оценка применения полусинтетического Таксола (паклитаксел) для инъекций по схеме один раз в неделю в исследовании CALGB 9731: данные по ремиссиям и выживаемости
[19, 46]
Ответ
ПР, % ЧР, % (95% CI) Стабильное заболевание, % Прогрессирующее заболевание, % Не оцениваются, % Выживаемость Медианная выживаемость, мес (95% CI) Годичная выживаемость, % (95% CI) Медианная выживаемость до прогрессии заболевания, мес (95% CI) Медианная годичная выживаемость до прогрессии заболевания, % (95% CI) CI=доверительный интервал; ПР=полная ремиссия; ЧР=частичная ремиссия. *Двенадцать из 38 больных живы на момент составления последнего отчета.
Применение полусинтетического Таксола (паклитаксел) для инъекций по схеме один раз в неделю в комбинации с карбоплатином
Профиль активности и токсичности Таксола, применяемого по схеме один раз в неделю, побудил исследователей включить такой способ его применения в режимы комбинированной химиотерапии. При НМРЛ Таксол, применяемый по схеме один раз в неделю, был включен в схемы комбинированной химиотерапии, содержащей карбоплатин, для лечения стадии IV заболевания [12, 20, 21, 45].
Химиотерапия с использованием комбинированных схем на основе препаратов платины продолжает оставаться стандартной формой лечения НМРЛ на стадии IV; однако, существующие на данный момент рекомендации не говорят о том, какой из препаратов платины является лучшим [1, 2]. Карбоплатин обладает активностью, сходной с активностью цисплатина, однако профиль токсичности этого препарата является предпочтительным по сравнению с профилем токсичности родительского соединения. В частности, почечная токсичность, неврологическая токсичность, ототоксическое действие и способность вызывать рвоту заметно ниже по сравнению с таковыми у цисплатина. Основным ограничивающим дозу токсическим эффектом карбоплатина является тромбоцитопения, однако степень этой токсичности оказывается заметно сниженной, когда препарат используется в сочетании с Таксолом [49, 50]. Высказывалось предположение, что Таксол может обладать протективным действием в отношении тромбоцитопении, индуцируемой карбоплатином [49]. Кроме того, поскольку дозовая схема применения карбоплатина определяется системной экспозицией этому препарату (выражаемая в форме площади под кривой концентрация в плазме по отношению к времени [AUC], а не токсичностью, можно применять полные дозы платины. Необходимое значение AUC можно рассчитать путем простого использования формулы Кальверта, которая соотносит желательную AUC с функцией почек больного [общая доза (мг) = желательная AUC х скорость гломерулярной фильтрации [СГФ]+25)] [51]. Далее, карбоплатин можно применять в условиях поликлиники [48]. По этим причинам карбоплатин является хорошим кандидатом для включения в схемы комбинированной химиотерапии совместно с полусинтетическим Таксолом (паклитаксел) для инъекций.
Опыт Онкологического института Питтсбургского Университета (Фаза I)
Возможность применения комбинированной химиотерапии с введением Таксола один раз в неделю и в сочетании с карбоплатином оценивалась в рамках испытания по Фазе I в Онкологическом институте Питтсбургского Университета. Повышающиеся дозы Таксола, применявшегося один раз в неделю (100, 125 и 135 мг/м2), использовали совместно с карбоплатином в рамках двух различных 8-недельных графиков. В соответствии с вариантом А, Таксол вводили в течение 6 недель, после чего следовал 2-недельный период отдыха, а карбоплатин (AUC=6) вводили в 1-й и 22-й дни. Во втором варианте (вариант В) Таксол вводили в течение 3 недель, начиная в 1-ю и 5-ю недели цикла, а карбоплатин (AUC=6) вводили в 1-й и 29-й дни. В случае каждого из этих вариантов лечение продолжали до прогрессирования заболевания и/или появления неприемлемых токсических эффектов [20].
В данное испытание, проводившееся по Фазе I, было включено 23 больных с различными солидными опухолями (Таблица 9). Средний возраст больных составлял 66 лет (интервал 39-78), у всех больных за исключением одного отмечался хороший функциональный статус (ФС=0 или 1). Большинство больных ранее не получали химиотерапии или лучевой терапии. Среди 23 включенных больных у 8 (35%) был рак легкого, наиболее часто встречающийся тип опухоли в данном испытании [20].
Таблица 9. Испытание по Фазе I Таксола, применяемого по схеме один раз в неделю, и карбоплатина: характеристики больных* [20]
*В испытание были включены больные с различными типами опухолей; наиболее частым типом опухоли был рак легкого (8 больных) и рак пищевода (5 больных).
Средний возраст (лет) Мужчины/женщины (n) Функциональный статус (n) Проводившаяся ранее химиотерапия (n) Проводившаяся ранее лучевая терапия (n) В общем и целом, оба варианта комбинированной химиотерапии с использованием полусинтетический Таксол (паклитаксел) для инъекций по схеме один раз в неделю совместно с карбоплатином хорошо переносились больными. Для каждой из схем больные получили 89% или более запланированных доз (Таблица 10). На сегодняшний день максимальная продолжительность лечения составляет 14 месяцев. У одного из больных отмечалась серьезная реакция гиперчувствительности, потребовавшая прекращения терапии. В результате прогрессирования заболевания имело место три ранних летальных исхода. Наиболее частым токсическим эффектом степени 3/4 была нейтропения, однако эпизодов, связанных с лихорадкой, не отмечалось. У одного больного развилась эритематозная сыпь степени 3 при получении самой высокой дозы Таксола в рамках варианта А. Примечательно, что в данном исследовании не было отмечено серьезных артралгий и миалгий. На основании этих результатов рекомендованная доза Таксола, применяемого по схеме один раз в неделю, т.е. в плотнодозовом режиме, для дальнейших исследований составляет от 100 до 125 мг/м2 в сочетании с карбоплатином, применяющемся в дозе, обеспечивающей AUC=6, как в рамках варианта А, так и в рамках варианта Б [20].
Таблица 10. Испытание по Фазе I Таксола, применяемого по схеме один раз в неделю, и карбоплатина: результаты по токсичности [20]
Таксол мг/м2 Таксол График А
В
4
4
89
89
3/1
3/1
01/0
00
00
А
В
3
4
93
100
1/1
0
00
00
00
А
В
5
3
91
93
3/1
2/0
00
1/00
00
AСН=абсолютное содержание нейтрофилов
*Вариант А: Таксол применялся по схеме один раз в неделю на протяжении 6 недель с последующим 2-недельным периодом отдыха; карбоплатин (AUC=6) вводили в 1-й и 22-й дни. Вариант В: Таксол применяли по схеме один раз в неделю на протяжении 3 недель, начиная в недели 1 и 5 8-недельного цикла; карбоплатин (AUC=6) вводили в 1-й и 29-й дни. Доза карбоплатина рассчитывалась по формуле Кальверта: общая доза (мг)=(желаемая AUC) х (СГФ+25). При использовании формулы Кальверта общая доза карбоплатина рассчитывается в миллиграммах, а не в мг/м2 (СГФ=скорость гломерулярной фильтрации).
**Эритематозная сыпь
Рандомизированные испытания комбинации полусинтетического Таксола (паклитаксел) для инъекций, используемого по схеме один раз в неделю, в сочетании с карбоплатином
После оценки схемы плотнодозового еженедельного введения Таксола в сочетании с карбоплатином (Фаза I) Онкологический институт Питтсбургского Университета и связанная с ним сеть онкологических центров предприняли рандомизированное многоцентровое испытание по индукционной плотнодозовой химиотерапии Таксолом, применяемым по схеме один раз в неделю, и карбоплатином, после чего следовала поддерживающая терапия Таксолом по схеме один раз в неделю у больных со стадией IIIB и IV НМРЛ [12]. Это испытание было предназначено для определения оптимальной дозы и графика еженедельного применения Таксола у больных с НМРЛ и снижения общего токсического эффекта, связанного с комбинированной химиотерапией. Оценка применения Таксола для поддерживающей терапии основана на результатах испытаний по Фазе I/II, о которых сообщали Чанг и соавт. (см. выше), которые показали возможность применения Таксола по схеме один раз в неделю в дозах 50 и 100 мг/м2 на протяжении длительных промежутков времени [16]. Основная задача испытания на этот момент заключалась в увеличении среднего срока до прогрессии заболевания [12].
В этом испытании больных подвергали стратификации в соответствии со стадией заболевания (IIIB и IV) и функциональным статусом (0/1 или 2) и рандомизировали на один из трех вариантов лечения (Рисунок 3).
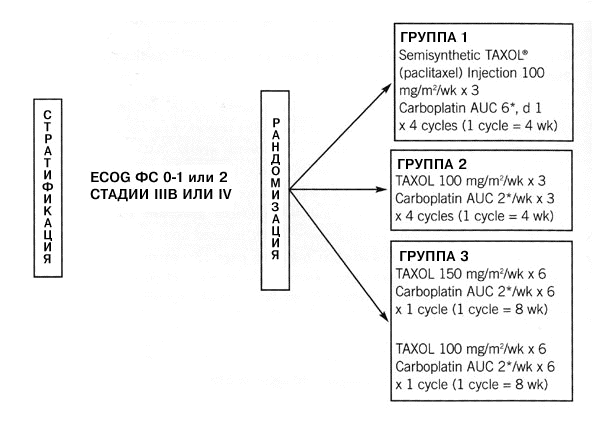
Рисунок 3. Схема рандомизированного многоцентрового испытания плотнодозового применения Таксола по схеме один раз в неделю в сочетании с карбоплатином у больных с распространенным НМРЛ: схема индукционной фазы. ECOG= Восточная корпоративная онкологическая группа; ФС=функциональный статус; *доза карбоплатина рассчитывалась по формуле Кальверта: общая доза (мг)=(желаемая AUC) х (СГФ+25). При использовании формулы Кальверта общая доза карбоплатина рассчитывается в миллиграммах, а не в мг/м2 (СГФ=скорость гломерулярной фильтрации) [12].
В группе, соответствующей первому варианту, Таксол применяли в дозе 100 мг/м2 еженедельно на протяжении 3 недель, а карбоплатин вводили до AUC 6 на 1-й день. Общая продолжительность курса лечения составляла 4 недели, и всего проводили четыре таких курса. В группе, соответствующей второму варианту схемы лечения, Таксол в дозе 100 мг/м2 и карбоплатин (AUC 2) вводили один раз в неделю на протяжении 3 недель 4-недельного курса лечения. Всего проводили четыре таких курса. В группе, соответствующей третьему варианту, Таксол в дозе 150 мг/м2 и карбоплатин (AUC 2) вводили еженедельно на протяжении 6 недель, после чего следовал 2-недельный период отдыха. На протяжении второго 8-недельного курса лечения еженедельную дозу Таксола уменьшали до 100 мг/м2 с тем, чтобы избежать развития нейропатии. В каждой из групп лечения индукционную фазу завершали через 16 недель. Больных, давших клинический ответ (полная ремиссия, частичная ремиссия или стабилизация заболевания), рандомизировали на прием Таксола в дозе 70 мг/м2 по схеме один раз в неделю путем 1-часового вливания или на обсервацию (Рисунок 4). В качестве клинических критериев использовали средний (медиана) срок до прогрессии заболевания и переносимость лечения. К данному моменту набор больных в группы происходит быстрыми темпами [12].
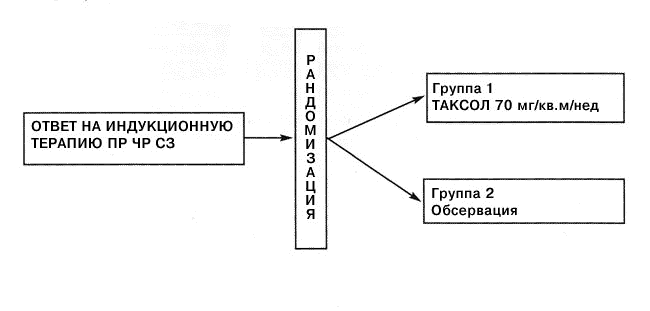
Рисунок 4. Схема рандомизированного многоцентрового испытания использования Таксола в плотнодозовом режиме по схеме один раз в неделю в сочетании с карбоплатином у больных с распространенным НМРЛ: схема поддерживающей фазы лечения. ПР=полная ремиссия; ЧР=частичная ремиссия; СЗ=стабилизация заболевания.[12].
Исследование по Фазе I/II полусинтетического Таксола (паклитаксел) для инъекций, используемого по схеме один раз в неделю, в сочетании с карбоплатином: опыт, полученный в Италии
С целью повысить дозовую интенсивность стандартной дозовой схемы и стандартного временного графика применения комбинации Таксол/карбоплатин итальянские исследователи провели исследование применения Таксола по схеме один раз в неделю в сочетании с карбоплатином в рамках испытания по Фазе I/II. Главными задачами этого исследования было определение максимальной переносимой дозы и анализ активности схемы Таксол/карбоплатин в условиях применения по схеме один раз в неделю. Токсические эффекты, ограничивающие дозу, определялись как общее содержание нейтрофилов менее 500/мм3 или тромбоцитов менее 25 000/мм3 более чем в течение 7 дней, общее содержание нейтрофилов менее 100/мм3 более чем в течение 3 дней, фебрильная нейтропения и негематологическая токсичность степени 4 у 2 из 4 больных при любой дозе. Карбоплатин применяли в постоянной дозе (AUC 6) в 1-й и 28-й дни. Таксол использовали в повышающихся дозах путем 1-часового вливания в 1-й, 8-й, 15-й и 28-й дни. Было запланировано шесть различных доз для применения Таксола по схеме один раз в неделю, начиная с дозы 50 мг/м2 с последующим наращиванием по 10 мг/м2 за каждый этап, на каждом этапе лечили 4 больных [21].
Всего в Фазу I испытания было включено 24 больных. Средний возраст больных составлял 58 лет, функциональный статус был оценен как хороший, и большинство из них имело стадию IV заболевания (Таблица 11). Комбинированная терапия Таксолом по схеме один раз в неделю и карбоплатином обычно хорошо переносилась при использовании каждой из шести доз, которые подвергались оценке в данной фазе исследования. Тяжелых негематологических токсических эффектов не наблюдалось; тошнота степени 2/3 и рвота наблюдались в немногих курсах лечения при некоторых дозах (Таблица 12). Гематологическая токсичность также носила легкий характер; нейтропения степени 3 и афебрильная нейтропения степени 4 отмечались в 15 и 8% курсах лечения, соответственно, при дозе Таксола 70 мг/м2. Однако в то же время тяжелой нейтропении не отмечалось при использовании высоких доз. Токсические эффекты, ограничивавшие дозу, не были достигнуты, и наращивание дозы продолжается. Предварительные результаты по активности Таксола при схеме один раз в неделю в сочетании с карбоплатином являются обнадеживающими, поскольку у 5% больных достигнута полная ремиссия, а у 40% частичная ремиссия [21].
Таблица 11. Итальянское исследование применения полусинтетического Таксола (паклитаксел) для инъекций по схеме один раз в неделю в сочетании с карбоплатином: характеристики больных (только Фаза I) [21]
Количество участвующих больных Средний возраст, лет (интервал) Функциональный статус по ECOG Стадия заболевания Таблица 12. Итальянское исследование применения полусинтетического Таксола (паклитаксел) для инъекций по схеме один раз в неделю в сочетании с карбоплатином: данные по токсичности (только Фаза I) [21]
Негематол. токсичность
ст. 3/4Гематол. токсичность
ст. 3/4Степени 2/3
тошнота/рвота
Нет Нет Нет Нет Нейтропения ст. 3
Афебрильная нейтропения ст. 4
8Тошнота/рвота ст. 2/3 Нет Нет Тошнота/рвота ст. 2/3 Нет
Использование полусинтетического Таксола (паклитаксел) для инъекций по схеме один раз в неделю индивидуально или в сочетании с карбоплатином для лечения больных с НМРЛ на стадии IV
На основании результатов описанных клинических испытаний [12, 15, 21, 45] представляется, что Таксол, применяемый по схеме один раз в неделю индивидуально или в сочетании с карбоплатином, может увеличить терапевтические возможности для больных с распространенной формой НМРЛ. Лечение должно быть индивидуализировано для больных в зависимости от их возраста, функционального статуса и ранее проводившегося лечения.
Ранее нелеченые больные с хорошим функциональным статусом
Опубликованные рекомендации в отношении клинического опыта и лечения подчеркивают важную роль стандартной химиотерапии схемами на основе препаратов платины при лечении больных с метастатической формой НМРЛ с хорошим функциональным статусом (ФС 0 или 1 по ECOG) [1, 2]. Сочетание применения Таксола по схеме один раз в неделю и карбоплатина является доступной схемой с обнадеживающей эффективностью и переносимостью [12, 20, 21, 45]. Схемы лечения, приведенные в Таблице 13, иллюстрируют подходы, используемые для включения Таксола, применяемого по схеме один раз в неделю, в комбинированную терапию на основе карбоплатина.
Таблица 13. Таксол, применяемый по схеме один раз в неделю, в сочетании с карбоплатином при распространенном НМРЛ: дозовые схемы*
НМРЛ=немелкоклеточный рак легкого; AUC=внутривенно; AUC=площадь под кривой концентрация в плазме-время.
Испытание
Схема Ramanath et al (1999) [20] Таксол 100-125 мг/м2 ВВ раз в неделю х 6 недель
Карбоплатин AUC 6 ВВ, д1, 22
каждые 8 недель
или
Таксол 100-125 мг/м2 ВВ раз в нед. х 3 недели, начиная с нед.1, 5
Карбоплатин AUC 6ВВ, д1, 29 каждые 8 недельFabi et al (1999) [21] Таксол 100 ВВ раз в неделю х 3 недели
Карбоплатин AUC 6, д1
каждые 4 недели
*Схемы, перечисленные в этой таблице, были опробованы в клинических испытаниях Фазы I. Другие схемы применения Таксола по схеме один раз в неделю в сочетании с карбоплатином подвергаются оценке в настоящее время в исследованиях Фазы II.
**Доза карбоплатина рассчитывалась по формуле Кальверта: общая доза (мг)=(желаемая AUC) х (СГФ+25). При использовании формулы Кальверта общая доза карбоплатина рассчитывается в миллиграммах, а не в мг/м2 (СГФ=скорость гломерулярной фильтрации).**Более высокие дозы Таксола, применяемого по схеме один раз в неделю, в настоящее время подвергаются оценке в продолжающихся испытаниях Фазы I, проводящихся в Италии. Эта схема используется также в качестве одного из вариантов в продолжающемся исследовании Фазы II в Онкологическом центре Питтсбургского Университета.
Ранее нелеченые больные с удовлетворительным функциональным статусом
В соответствии с клиническими рекомендациями ASCO комбинированная химиотерапия может рассматриваться как вариант лечения отдельных больных с функциональным статусом 2 [1]. Схемы лечения, приведенные в Таблице 13, также могут быть вариантом для применения у этой группы больных. На основании результатов исследования ECOG 1594 [11], стандартная схема полусинтетический Таксол (паклитаксел) для инъекций/карбоплатин также является разумным подходом для ранее не леченых больных с удовлетворительным функциональным статусом. Для больных, считающихся неподходящими для комбинированной химиотерапии, режим, оценивавшийся Чангом и соавт. у больных с удовлетворительным функциональным статусом и/или престарелых больных (Таксол, применяемый по схеме один раз в неделю в дозе 80 мг/м2 в 1-й, 8-й и 19-й дни 4-недельно курса лечения) является возможным вариантом [16].
Больные с рецидивом заболевания в прежней или новой локализации
Рекомендации NCCN по лечению метастатического НМРЛ рекомендуют химиотерапию второй линии для больных с рецидивом заболевания в той же локализации или новой локализации при функционом статусе категории "хороший" [2]. Для больных, не подходящих для комбинированной химиотерапии, использование Таксола в форме монотерапии по схеме один раз в неделю может быть подходящей альтернативой [44].
Престарелые больные с распространенным НМЛР
Более 30% всех случаев рака легкого отмечается у больных в возрасте более 70 лет. В результате в расчете на 1 год средняя популяция престарелых больных с раком легкого в США по численности превосходит 74 000 человек. Врачи могут обладать предвзятым мнением о том, что престарелые больные НМРЛ в меньшей степени способны переносить химиотерапию и, как правило, непригодны для использования агрессивных схем химиотерапии на основе препаратов платины. Однако имеющиеся данные не говорят о том, что возраст является важным прогностическим фактором в отношении таких моментов, как ответ на лечение, выживаемость или переносимость лечения [52].
Престарелые больные с НМРЛ на стадии IV обычно имеют широкий спектр симптомов. У некоторых больных функциональный статус оказывается ненарушенным или нарушен лишь в минимальной степени, и, несмотря на распространенное заболевание, отмечается лишь минимальная потеря веса; другие больные являются симптоматическими больными с выраженными функциональными ограничениями ил серьезными сопутствующими заболеваниями. Критическим фактором для отбора больных на химиотерапию является функциональный статус [52].
В своем ретроспективном анализе испытаний по применению Таксола/карбоплатина в рамках Фазы II у больных с НМРЛ стадии IIIB/IV Лэнгер и соавт. обнаружили, что клинические признаки у больных в возрасте 70 лет и старше хорошо сопоставимы с таковыми у больных в возрасте до 70 лет. В двух этих возрастных группах среднее время выживания (медиана) составляло 42 недели и 53 недели, соответственно, а годичная выживаемость составляла 44% и 54%, соответственно. Кроме того, негематологические токсические эффекты обычно не ограничивали применявшейся дозы, а нейтропения степени 3/4 наблюдалась у сходного процента больных в обеих возрастных группах (68% и 70%, соответственно) [52, 53].
Как показано в испытании ECOG 1594, стандартная в плане доз и графика введения терапия с использованием полусинтетического Таксола (паклитаксел) для инъекций в сочетании с карбоплатином представляет собой режим лечения, переносимый, чем комбинации на основе цисплатина с одновременным использованием доцетаксела или гемцитабина [11]. Аналогичным образом испытание SWOG 9509 показало, что стандартная схема Таксол/карбоплатин обладает преимуществом в плане переносимости по сравнению с комбинацией цисплатин/винорелбин [10]. Хорошая переносимость, отмечающаяся в испытаниях по Фазе I/II с использованием Таксола по схеме один раз в неделю в сочетании с карбоплатином, показывает, что этот график лечения также может рассматриваться для указанной группы больных [20, 21]. Монотерапия умеренными дозами Таксола по схеме один раз в неделю также обладает благоприятным профилем безопасности и клинической активностью [16]. Эта схема может представлять собой приемлемый вариант лечения для престарелых больных, которые не являются кандидатами на комбинированную химиотерапию [44].
Напротив, недавно описанный предварительный анализ исследования комбинации гемцитабин/винорелбин по сравнению с винорелбином в форме монотерапии по Фазе III (обе схемы применялись по графику по схеме один раз в 3 недели) показывает, что ни одна из них не является пригодной для лечения престарелых больных или больных с удовлетворительным функциональным статусом. Запланированный анализ включал 103 престарелых больных (старше 70 лет) с функциональным статусом по ECOG 2 или ниже и 35 больных более молодого возраста (возраст не сообщается) с функциональным статусом по ECOG 2 (всего 138 больных, 70 получали лечение комбинацией гемцитабин/винорелбин, и 68 только винорелбином). При среднем сроке наблюдения (медиана), составлявшем 13 месяцев (интервал 1-19 месяцев), среднее время выживания составляло 25 недель и 23 недели для вариантов, получавших гемцитабин/винорелбин и только винорелбин, соответственно). Для группы только престарелых больных среднее время выживания составляло 23 недели и 18 недель, соответственно. Исследователи пришли к выводу, что ни один из этих режимов лечения не представляет собой эффективной схемы лечения для этих групп больных, поскольку среднее время выживания для обоих вариантов лечения не было существенно большим, чем время выживания в условиях применения оптимальной поддерживающей терапии без химиотерапии (21 неделя) [54].
На Рисунке 5 приведены потенциальные ситуации, при которых Таксол, применяемый индивидуально по схеме один раз в неделю в форме монотерапии или в сочетании с карбоплатином может оказаться полезным.
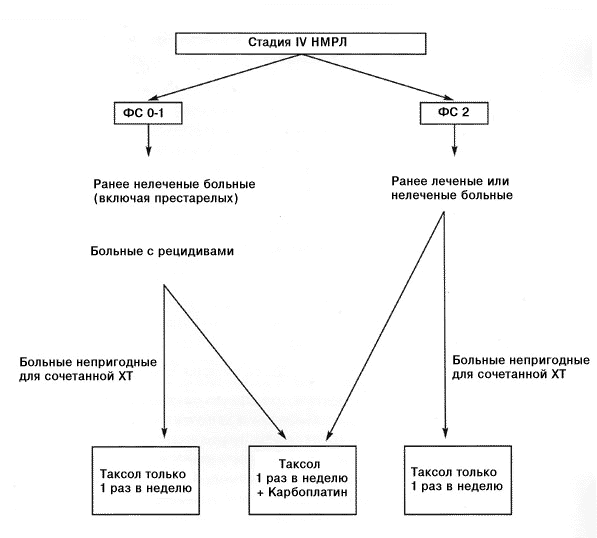
Рисунок 5. Полусинтетический Таксол (паклитаксел) для инъекций по схеме один раз в неделю индивидуально или в комбинации с карбоплатином: потенциальное использование для лечения НМРЛ. НМРЛ=немелкоклеточный рак легкого; ФС=функциональный статус [12, 43]
ВЫВОДЫ
Комбинированная химиотерапия схемами на основе препаратов платины представляет собой стандартную форму лечения, рекомендованную как ASCO, так и NCCN для лечения больных с распространенными формами НМРЛ. Рекомендации по лечению, однако, не определяют оптимальной схемы с использованием препарата платины [1, 2]. Результаты серии испытаний в рамках Фазы II и III показывают, что полусинтетический Таксол (паклитаксел) для инъекций в сочетании с карбоплатином, применяющиеся по схеме один раз в 3 недели, является эффективной и обычно хорошо переносимой формой лечения для терапии первой линии распространенного НМРЛ; при этом годичная выживаемость больных варьирует от 27 до 54% [3, 5, 6]. Кроме того, результаты двух последних испытаний в рамках Фазы III показывают меньший процент серьезных токсических эффектов на комбинации Таксол/карбоплатин по сравнению с другими схемами, в которых использовался цисплатин [10, 11]. Таким образом, SWOG высказывается в плане предпочтительности схем Таксол/карбоплатин в будущих исследованиях за счет более благоприятного профиля токсичности и лучшей переносимости таких схем больными и, соответственно, лучшего соблюдения назначенных условий лечения [10].
Применение Таксола по схеме один раз в неделю позволяет дозоинтенсивное применение этого препарата [17-19, 22, 29] причем в таких условиях препарат хорошо переносится без клинически выраженных гематологических или не гематологических токсических эффектов [15-19, 22]. Кроме того, в отношении целого ряда солидных опухолей, включая НМРЛ, получены обнадеживающие данные в плане клинической активности [15-19]. Клинически достоверные ремиссии отмечались в целом ряде клинических ситуаций. Ремиссии отмечались и у больных, которые ранее подвергались интенсивной химиотерапии, включая применение схемы на основе препаратов платины [15, 16]. Переносимость Таксола, применяемого по схеме один раз в неделю, делает этот препарат ценным для лечения больных, не подходящих для комбинированной химиотерапии, включая больных с удовлетворительным функциональным статусом [16].
Рекомендации в отношении клинической практики и существующие стандарты лечения подчеркивают роль форм лечения с использованием препаратов платины у больных со стадией IV НМРЛ [1, 2]. Терапевтический индекс, достигающийся при применении Таксола по схеме один раз в неделю, делает его привлекательной основой для комбинированной терапии в сочетании с карбоплатином [12, 20, 21, 45]. Большой интерес для клиницистов и исследователей представляет возможность того, что применение Таксола по схеме один раз в неделю позволит дальнейшее исследование действия этого препарата на апоптоз и антиангиогенного эффекта, которые наблюдались in vitro [30-33].
ЛИТЕРАТУРА
1. American Society of Clinical Oncology. Clinical practice guidelines for the treatment of unresectable non-small-cell lung cancer. J Clin Oncol. 1997:15:2996-3018.
2. Ettinger DS, Cox JD, Ginsberg RJ, et al. NCCN non-small-cell lung cancer clinical practice guidelines. Oncology. 1996:10(suppl):81-111.
3. Belani CP, Natale RB, Lee JS, et al. Randomized phase III trial comparing cisplatin/etoposide versus carboplatin/paclitaxel in advanced and metastatic non-small cell lung cancer (NSCLC). Proc Am Soc Clin Oncol. 1998;17:455a. Abstract 1751. Slides presented at: The Thirty-Fourth Annual Meeting of the American Society of Clinical Oncology; May 16-19, 1998; Los Angeles, CA.
4. Kosmidis P, Mylonakis N, Fountzilas G, et al. Paclitaxel (175 mg/m2) plus carboplatin versus paclitaxel (225 mg/m2) plus carboplatin in non-small cell lung cancer: a randomized study. Semin Oncol. 1997;24 (suppl 12):S12-30-S12-33.
5. Langer CJ, Leighton JC, Comis RL, et al. Paclitaxel and carboplatin in combination in the treatment of advanced non-small-cell lung cancer: a phase II toxicity, response, and survival analysis. J Clin Oncol. 1995:13:1860-1870.
6. Kosmidis PA. Paclitaxel (175)/carboplatin (AUC 6) versus paclitaxel (225)/carboplatin (AUC 6) in non-small cell lung cancer. Slides presented at: The Fox Chase Cancer Center and Free University Hospital Paclitaxel Investigators' Workshop and Consensus Conference; March 26-28, 1998; St. Thomas, US Virgin Islands.
7. Hainsworth JD, Urba WJ, Hon JK, et al. One-hour paclitaxel plus carboplatin in the treatment of advanced non-small cell lung cancer: results of a multicentre, phase II trial. Eur J Cancer. 1998:34:654-658.
8. Gatzemeier U. Resell R, Betticher D, et al. Randomized Pan-European trial comparing paclitaxel (TAX)/carboplatin (CAR) versus paclitaxel/cisplatin (CIS) in advanced non-small cell lung cancer (NSCLC). Eur J Cancer. 1999;35(suppl4):S246. Abstract 973.
9. Data on file. Bristol-Myers Squibb Oncology; 1999.
10. Kelly K, Crowley J, Bunn PA, et al. A randomized phase III trial of paclitaxel plus carboplatin (PC) versus vinorelbine plus cisplatin (VC) in untreated advanced non-small cell lung cancer (NSCLC):
a Southwest Oncology Group (SWOG) trial. Proc Am Soc Clin Oncol. 1999; 18:461 a. Abstract 1777 and slides presented at: Thirty-Fifth Annual Meeting of the American Society of Clinical Oncology; May 15-18, 1999; Atlanta, GA.
11. Schiller J. Update of E1594; four-arm trial in metastatic non-small cell lung cancer. Slides presented at: The Fox Chase Cancer Center and Free University Hospital Paclitaxel Investigators' Workshop and Consensus Conference; March 26-28, 1998; St. Thomas, US Virgin Islands.
12. Belani C. Personal communication. October 1999; December 1999.
13. Johnson DH, Zhu J, Schiller J, et al. E-1594-a randomized phase III trial in metastatic non-small cell lung cancer (NSCLC)-outcome of PS 2 patients (pts): an Eastern Cooperative Oncology Group trial (ECOG). Pro Am Soc din Oncol. 1999; 18:461 a. Abstract 1779 and slides presented at: Thirty-Fifth Annual Meeting of the American Society of Clinical Oncology; May 15-18, 1999; Atlanta, GA.
14. Shyr Y, Choy H, Cmelak A, et al. Pattern of practice survey: non-small cell lung cancer (NSCLC) in US. Proc Am Soc din Oncol. 1998;17:463a. Abstract 1778.
15. Koumakis G, Barbounis V, Vassilomanolakis M, et al. Phase l-ll trial of weekly paclitaxel in advanced non small cell lung cancer (N.S.C.L.C.): a preliminary report. Lung Cancer. 1999;25(suppl 1):S31.
16. Chang AY, Asbury RF, Boros L, et al. Stage IV NSCLC: weekly Taxol and beyond. Slides presented at: The Fox Chase Cancer Center and Free University Hospital Paclitaxel Investigators' Workshop and Consensus Conference; March 4-6, 1999; Lana'i, HI.
17. Akerley W, Glantz M, Choy H, et al. Phase I trial of weekly paclitaxel in advanced lung cancer. J Clin Oncol. 1998:16:153-158.
18. Akerley W, Choy H, Safran H, et al. Weekly paclitaxel in patients with advanced lung cancer: preliminary data from a phase II trial. Sem/n Oncol. 1997;24(suppl 12):S12-10-S12-13.
19. Akerley W, Herndon J, Egorin MJ, et al. CALGB 9731: phase II trial of weekly paclitaxel for advanced non-small cell lung cancer (NSCLC). P roc Am Soc Clin Oncol. 1999;18:462a. Abstract 1783.
20. Ramanath RK, Capozzoli MJ, Trump DL, et al. Escalating doses of weekly paclitaxel in combination with carboplatin: a phase I study in advanced malignancies. Proc Am Soc Clin Oncol. 1999;18:166a. Abstract 638.
21. Fabi A, Barduagni M, De Marco S, et al. A phase l-ll study with carboplatin (C) and weekly paclitaxel (P) in advanced NSCLC. Eur J Cancer. 1999;35(suppl 4):S263-S264. Abstract 1049.
22. Seidman AD, Hudis CA, Albanel J, et al. Dose-dense therapy with weekly 1-hour paclitaxel infusions in the treatment of metastatic breast cancer. J Clin Oncol. 1998:16:3353-3361.
23. Lopes NM, Adams EF, Pitts TW, et al. Cell kill kinetics and cell cycles effects of Taxol on human and hamster ovarian cell lines. Cancer Chemother Pharmacol. 1993:32:235-242.
24. Jordan MA, Wendell K, Gardiner S, et al. Mitotic block induced in HeLa cells by low concentration of paclitaxel (Taxol) results in abnormal mitotic exit and apoptotic cell death. Cancer Res. 1996:56:816-825.
25. Kearns CM, Glanni L, Egorin MJ. Paclitaxel pharmacokinetics and pharmacodynamics. Sem/n Oncol. 1995;22(suppl 6):16-23.
26. Seidman AD, Hochhauser D, Gollub M, et al. Ninety-six-hour paclitaxel infusion after progression during short taxane exposure: a phase III pharmacokinetic and pharmacodynamic study in patients with metastatic breast cancer. J Clin Oncol. 1996:14:1877-1884.
27. Chang AY, Boros L, Garrow R, et al. Paclitaxel by 3-hour infusion followed by 96-hour infusion on failure in patients with refractory malignant disease. Sem/n Oncol. 1995;22(suppl 6): 124-127.
28. Fennelly D, Aghajanian C, Shapiro F, et al. Phase I and pharmacologic study of paclitaxel administered weekly in patients with relapsed ovarian cancer. J Clin Oncol. 1997:15:187-192.
29. Norton L. Evolving concepts in the systemic drug therapy of breast cancer. Semin Oncol. 1997;24(suppl 10):S10-3-S10-S01-9.
30. Belotti D, Vergani V, Drudis T, et al. The microtubule-affecting drug paclitaxel has antiangiogenic activity. Clin Cancer Res. 1996:2:1843-1849.
31. Klauber N, Parangi S, Flynn E, et al. Inhibition of angiogenesis and breast cancer in mice by the microtubule inhibitors 2-methoxyestradiol and Taxol. Cancer Res. 1997:57:81-86.
32. Milross CG, Mason KA, Hunter NR, et al. Relationship of mitotic arrest and apoptosis to antitumor effect of paclitaxel. J NatI Cancer Inst. 1996:88:1308-1314.
33. Blagosklonny MV, Schulte T, Nguyen P, et al. Taxol-induced apoptosis and phosphorylation of Bcl-2 protein involves c-Raf-1 and represents a novel c-Raf-1 signal transduction pathway. Cancer Res. 1996:56:1851-1854.
34. Perez EA, Irwin DH, Patel R, et al. A large phase II trial of paclitaxel administered as a weekly one hour infusion in patients with metastatic breast cancer. Poster presented at: Thirty-Fifth Annual Meeting of the American Society of Clinical Oncology; May 15-18, 1998; Atlanta, GA. Abstract 480 (updated).
35. Mickiewicz E, Alvarez AM, Brosio C, et al. A promising second line treatment with weekly Taxol (T) in anthracycline recurrent, advanced breast cancer (ABC) patients (pts). Proc Am Soc Ctin Oncol. 1999;18:135a.Abstract515.
36. Seidman AD. Paclitaxel via weekly 1-hour infusion: dose dense therapy for metastatic breast cancer. Slides presented at: The Fox Chase Cancer Center and Free University Hospital Paclitaxel Investigators' Workshop and Consensus Conference; March 26-28, 1998; St. Thomas, US Virgin Islands.
37. Sola C, Lluch A, Garcia-Conde J, et al. Phase II study of paclitaxel (P) in recurrent breast cancer after high-dose chemotherapy (HDC). Proc Am Soc Clin Oncol. 1998;17:174a. Abstract 669.
38. Breier S, Lebedinsky C, Ayiviri C, et al. Long-term weekly paclitaxel (P) in metastatic breast cancer (MBC): a phase II trial in pretreated patients (pts). Proc Am Soc Clin Oncol. 1998;17:192a. Abstract 740 and poster presented at: The Thirty-Fourth Annual Meeting of the American Society of Clinical Oncology; May 16-19, 1998; Los Angeles, CA.
39. Waintraub SE, Cantwell S, DeVries J, et al. Phase II study to evaluate the efficacy of weekly paclitaxel (P) in patients with metastatic breast cancer (MBC) who have failed prior anthracycline (A) ± taxane (T) therapy. Proc Am Soc Clin Oncol. 1999;18:138a. Abstract 530.
40. Loesch D, Robert N, Dakhil S, et al. Phase II trial of a weekly Taxol (T), 5-fluorouracil (FU) and leucovorin (LV) regimen in patients (pts) with metastatic cancer: an update. Proc Am Soc Clin Oncol. 1999; 18:117a. Abstract 445.
41. Nistico C, Vaccaro A, Frontini L, et al. Weekly combination of Taxol, 5-fluorouracil and leucovorin (TFL) in advanced pretreated breast cancer patients (pts). Proc Am Soc Clin Oncol. 1999;18:136a. Abstract 519.
42. Rosenberg P, Andersson H, Boman K, et al. A randomized multicenter study of single agent paclitaxel (TAXOL®) given weekly versus every three weeks to patients (PTS) with ovarian cancer (OC) previously treated with platinum therapy. Proc Am Soc Clin Oncol. 1999;18:368a. Abstract 1420.
43. Abu-Rustum NR, Aghajanian C, Barakat RR, et al. Salvage weekly paclitaxel in recurrent ovarian cancer. Semin Oncol. 1997;24(suppl 15):S15-62-S15-67.
44. David Spriggs. Personal communication. June 1999.
45. Socinski M. Personal communication. April 1999; November 1999.
46. Akerley W. Personal communication. March 1999.
47. Akerley W. CALGB 9731 study. Slides presented at: The First International Chicago Symposium on Malignancies of the Chest and Head & Neck; October 1-2, 1999; Chicago, IL.
48. Perez EA, Hartmann LC. Paclitaxel and carboplatin for advanced breast cancer. Sem/n Oncol. 1996;23(suppl 11):41-45.
49. Huizing MT, van Warmerdam LJC, Rosing H, et al. Phase I and pharmacologic study of the combination paclitaxel and carboplatin as first-line chemotherapy in stage III and IV ovarian cancer. J Clin Oncol. 1997; 15:1953-1964.
50. Kearns CM, Belani CP, Erkmen K, et al. Reduced platelet toxicity with combination carboplatin & paclitaxel: pharmacodynamic modulation of carboplatin associated thrombocytopenia. Proc Am Soc Clin Oncol. 1995:14:170. Abstract 364.
51. Calvert AH, Newell DR, Gumbrell LA, et al. Carboplatin dosage: prospective evaluation of a simple formula based on renal function. J Clin Oncol. 1989:7:1748-1756.
52. Langer C, Evans W. Issues in the contemporary chemotherapy of metastatic non-small-cell lung cancer. From Research to Practice. 1999:1:29-37.
53. Rosvold E, Langer CJ, McAleer C, et al. Advancing age does not exacerbate toxicity or compromise outcome in non-small cell lung cancer (NSCLC) patients (pts) receiving paclitaxel-carboplatin (P-C). Proc Am Soc Clin Oncol. 1999;18:478a. Abstract 1846.
54. Frasci G, Lorusso V, Panza N, et al. Gemcitabine + vinorelbine (GV) vs vinorelbine (V) alone in elderly or frail non-small cell lung cancer (NSCLC) patients. Interim analysis of SICOG phase III trial. Eur J Cancer. 1999;35 (suppl 4):S249. Abstract 987.
| Май 2003 г. |